
- •1. Экзаменационные вопросы
- •Ферменты. Номенклатура. Классификация ферментов.
- •Уровни организации ферментов.
- •Механизм действия ферментов. Понятие об активном центре фермента, этапы ферментативного катализа.
- •Кинетика ферментативных реакций. Зависимость скорости ферментативной реакции от различных факторов. Уравнение Михаэлиса-Ментен, роль Кm и Vmax в характеристике фермен- тов.
- •Ингибиторы ферментов. Типы ингибирования. Графическое представление зависимости скорости ферментативной реакции от присутствия ингибиторов различных типов.
- •Механизмы регуляции активности ферментов. Примеры.
- •Аллостерические ферменты. Регуляция их активности. При- меры.
- •Введение в обмен веществ. Биологическое окисление
- •Важнейшие признаки живой материи. Особенности живых организмов, как открытых термодинамических систем.
- •1 Закон термодинамики:
- •2 Закон термодинамики:
- •Обмен углеводов
- •1 Схема-
- •2 Схема-
- •3 Этап оу – промежуточный обмен
- •Роль фосфорилазы при мобилизации гликогена
- •Обмен аминокислот, белков и нуклеотидов
- •Глюкозо-аланиновый цикл
- •Реакции глюкозо-аланинового цикла (выделен рамкой). Реакции, связанные с транспортными формами аммиака
- •Обмен липидов и липопротеидов
- •Гидролиз эфиров холестерина
- •Стеаторея
- •Процесс β- окисления: локализация, последовательность реакций, ферменты. Биологическое значение. Регуляция процесса β-окисления. Энергетический эффект окисления вжк (на примере пальмитиновой кислоты).
- •Этапы биосинтеза желчных кислот
- •Регуляция синтеза желчных кислот
- •Образование вторичных желчных кислот. Энтерогепатический цикл.
- •Метаболизм кетоновых тел при голодании
- •Биологические мембраны. Перекисное окисление липидов
- •1. Основные мембраны клетки и их функции.
- •2. Строение и состав мембран: структура и свойства липидов,белков, углеводов мембран. Общие свойства мембран и их функции.
- •3. Трансмембранный перенос малых молекул. Типы переноса веществ через мембрану. Трансмембранный перенос макромолекул и частиц. Механизмы мембранного транспорта
- •Проницаемость плазматической мембраны
- •Пассивный транспорт
- •Простая диффузия
- •Облегченная диффузия
- •Особенности облегченной диффузии
- •Активный транспорт
- •Ионные каналы
- •Эндоцитоз
- •Экзоцитоз
- •Функции биологических мембран
- •4. Механизмы трансмембранной передачи гормонального сигнала в клетку.
- •5. Активные формы кислорода (афк). Биологическое действие афк. Ферментативные и неферментативные системы, генерирующие афк.
- •6. Стадии свободно-радикального окисления липидов.
- •7. Повреждающее действие первичных и вторичных продуктов пероксидного окисления на мембраны и другие структуры клетки.
- •8. Ферментативные системы антирадикальной защиты. Катализируемые реакции.
- •9. Неферментативные системы антирадикальной защиты и их физиологическое значение.
- •10. Роль афк в механизме фагоцитоза. Кислородзависимые и кислороднезависимые механизмы фагоцитоза. Роль афк в антимикробной защите грудного молока.
- •11.Роль пероксидного окисления при гипоксии (ишемии). Факторы гипоксии, инициирующие пол. Понятие о «кислородном» и «кальциевом» парадоксах.
- •12. Простагландины и лейкотриены: схема синтеза и их биологические функции.
- •Гормоны. Гормональная регуляция метаболических процессов
- •Регуляция синтеза и секреции
- •Механизм действия
- •Мишени и эффекты
- •Патология Гипофункция
- •Биохимия питания и печени. Нервная, мышечная и соединительная ткани. Биохимия крови
- •Метаболизм скелетных мышц ( поперечно-полосатые мышцы)
- •Метаболизм скелетных мышц ( поперечно-полосатые мышцы)
- •Двойственная роль креатинфосфата
- •Пути генерации атф и восстановление атф в мышечных клетках миокарда
- •Механизм мышечного сокращения
- •Этапы цикла мышечного сокращения
- •Миозиновая регуляция сокращения
- •Сравнение актин-миозинового взаимодействия в 2-х видах мышц
- •Механизм расслабления поперечнополосатого мышечного волокна
- •Метаболические нарушения при инфаркте миокарда
- •Лабораторная диагностика инфаркта миокарда
- •Обмен железа: основные функции, пул железа в организме, всасывание в жкт, «ферритиновый блок».
- •Поступление экзогенного железа в ткани из кишечника
- •Нарушение метаболизма железа
Кинетика ферментативных реакций. Зависимость скорости ферментативной реакции от различных факторов. Уравнение Михаэлиса-Ментен, роль Кm и Vmax в характеристике фермен- тов.
Кинетика ферментативных реакций – наука о скоростях ферментативных реакций, их зависимости от различных факторов. Скорость ферментативной реакции определяется химическим количеством прореагировавшего субстрата или образовавшегося продукта реакции в единицу времени в единице объема при определенных условиях:
![]() ,
,
где
v – скорость ферментативной реакции, ![]() –
изменение концентрации субстрата или
продукта реакции, t – время.
–
изменение концентрации субстрата или
продукта реакции, t – время.
Скорость ферментативной реакции зависит от природы фермента, которая определяет его активность. Чем выше активность фермента, тем выше скорость реакции. Активность фермента определяют по скорости реакции, катализируемой ферментом. Мерой активности фермента является одна стандартная единица активности фермента. Одна стандартная единица активности фермента – это такое количество фермента, которое катализирует превращение 1 мкмоль субстрата за 1 минуту.
В процессе ферментативной реакции фермент (Е) взаимодействует с субстратом (S), в результате образуется фермент-субстратный комплекс, который затем распадается с высвобождением фермента и продукта (Р) реакции:
![]()
Скорость ферментативной реакции зависит от многих факторов: от концентрации субстрата и фермента, температуры, рН среды, наличия различных регуляторных веществ, способных увеличивать или снижать активность ферментов.
Влияние концентрации субстрата и фермента на скорость ферментативной реакции
Рассмотрим влияние концентрации субстрата на скорость ферментативной реакции (рис. 30.). При низких концентрациях субстрата скорость прямо пропорциональна его концентрации, далее с ростом концентрации скорость реакции увеличивается медленнее, а при очень высоких концентрациях субстрата скорость практически не зависит от его концентрации и достигает своего максимального значения (Vmax). При таких концентрациях субстрата все молекулы фермента находятся в составе фермент-субстратного комплекса, и достигается полное насыщение активных центров фермента, именно поэтому скорость реакции в этом случае практически не зависит от концентрации субстрата.
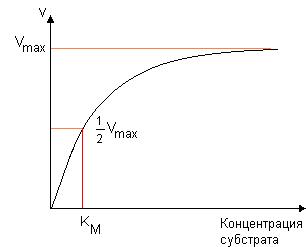
Рис. 30. Зависимость скорости ферментативной реакции от концентрации субстрата
График зависимости активности фермента от концентрации субстрата описывается уравнением Михаэлиса – Ментен, которое получило свое название в честь выдающихся ученых Л.Михаэлиса и М.Ментен, внесших большой вклад в исследование кинетики ферментативных реакций,
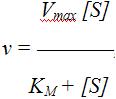
где v – скорость ферментативной реакции; [S] – концентрация субстрата; KM – константа Михаэлиса.
Рассмотрим физический смысл константы Михаэлиса. При условии, что v = ½ Vmax, получаем KM = [S]. Таким образом, константа Михаэлиса равна концентрации субстрата, при которой скорость реакции равна половине максимальной.
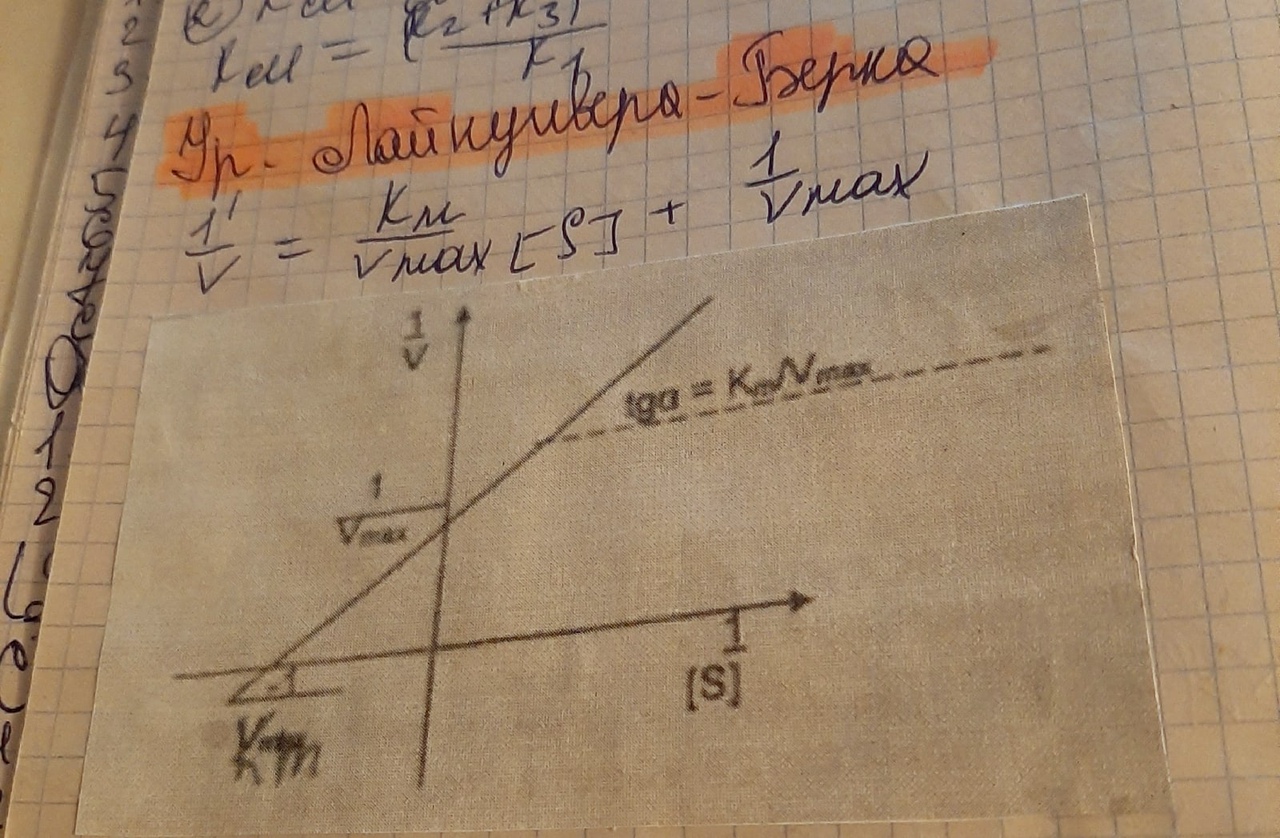
Скорость ферментативной реакции зависит и от концентрации фермента (рис. 31). Эта зависимость носит прямолинейный характер.
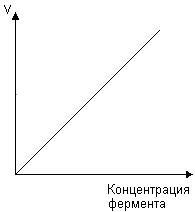
Рис. 31. Зависимость скорости ферментативной реакции от концентрации фермента
Влияние температуры на скорость ферментативной реакции
Зависимость скорости ферментативной реакции от температуры представлена на рис. 32.
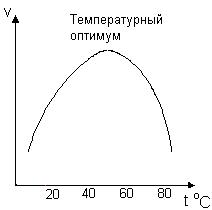
Рис. 32. Зависимость скорости ферментативной реакции от температуры.
При низких температурах (приблизительно до 40 – 50 оС) повышение температуры на каждые 10 оС в соответствии с правилом Вант-Гоффа сопровождается увеличением скорости химической реакции в 2 – 4 раза. При высоких температурах более 55 – 60 оС активность фермента резко снижается из-за его тепловой денатурации, и, как следствие этого, наблюдается резкое снижение скорости ферментативной реакции. Максимальная активность ферментов наблюдается обычно в пределах 40 – 60 оС. Температура, при которой активность фермента максимальна, называется температурным оптимумом. Температурный оптимум ферментов термофильных микроорганизмов находится в области более высоких температур.
Влияние рН на скорость ферментативной реакции
График зависимости ферментативной активности от рН представлен на рис. 33.
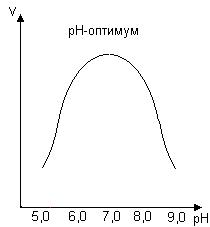
Рис. 33. Влияние рН на скорость ферментативной реакции
График зависимости от рН имеет колоколообразную форму. Значение рН, при котором активность фермента максимальна, называется рН-оптимумом фермента. Значения рН-оптимума для различных ферментов колеблются в широких пределах.
Характер зависимости ферментативной реакции от рН определяется тем, что этот показатель оказывает влияние на: a) ионизацию аминокислотных остатков, участвующих в катализе, b) ионизацию субстрата, c) конформацию фермента и его активного центра.
