
Вопросы к 1 кр
.docxВопросы к 1-й контрольной работе
Общая характеристика полимерных веществ, основные понятия и термины. Линейные, разветвленные и сетчатые полимеры (примеры). Полимеризационные и поликонденсационные методы получения полимеров (примеры). Методы синтеза полимеров: в газовой фазе, блочная полимеризация, полимеризация в растворе, эмульсионная и суспензионная полимеризация. Особенности этих методов.
Высокомолекулярные соединения (ВМС) – это химические соединения с молекулярной массой от нескольких тысяч до нескольких миллионов углеродные единиц.
Большая
часть ВМС – полимеры. Полимеры построены
путем многократного повторения атомных
групп (составных звеньев), соединенных
в макромолекулы химическими связями.
Наименьшее составное звено – повторяющееся
звено. Наибольшее составное звено –
мономер. Количество мономерных звеньев
– степень полимеризации. Название
линейного полимера образуется путем
прибавления приставки поли-. Полимер,
получаемый полимеризацией этилена =
полиэтилен.
 или
;
-
полипропилен.
или
;
-
полипропилен.
Полимер – это в-во, состоящее из молекул, характеризующихся многократным повторением одного или более типов составных звеньев, соединенных между собой в количестве, достаточном для проявления комплекса свойств, который осатется практически неизменным при добавлении или удалении 1 или нескольких составных звеньев. (ИЮПАК)
Полимерное состояние — это особая форма существования химических соединений, которая в основных физических и химических проявлениях качественно отличается от низкомолекулярных веществ.
Линейные полимеры (основная цепь состоит из повторяющихся звеньев, соединенных друг с другом в линейную конструкцию). Целлюлоза, натуральный каучук, некоторые белки и подавляющее большинство синтетических полимеров, используемые для производства волокон, термопластов, пленок, покрытий и т.д.
Разветвленные полимеры (основная цепь содержи произвольно расположенные боковые ответвления длиной от нескольких атомов до размеров, сопоставимых с длиной основной цепи. Предельный случай – звездообразные (совокупность цепей выходит из 1 центра), гребнеобразные (короткие ответвления в каждом звене). Амилопектин – полисахарид крахмала, полиэтилен низкой плотности. Гребнеобразные – эфиры акриловой и метакриловой кислот.
Сшитые или сетчатые полимеры (состоят из макромолекул, образующих пространственную сетку), лестничные полимеры (две параллельных цепи, которые соединены поперечными связями в каждом звене. Редкосшитые вулканизированные каучуки (основа шинной промышленности), реактопласты
Полимеризация – процесс получения высокомолекулярных соединений, при котором макромолекула образуется путем последовательного присоединения молекул 1 или нескольких низкомолекулярных веществ (мономеров) к растущему активному центру. Это цепная реакция, в которой развитие кинетической цепи сопровождается ростом материальной цепи макромолекулы.
Радикальная (активный центр – свободный радикал (радикал роста, макрорадикал));
Ионная – катионная и анионная (концевой атом растущей цепи несет полный или частичный положительный, или отрицательный заряд соответственно);
Координационно-ионная (противоион, входящий в состав активного центра, принимает участие в акте роста6 образуя с присоединяющей молекулой мономера координационный комплекс или циклическое переходное состояние)
Полимеризация в массе (блочная полимеризация) — это полимеризация мономера в конденсированной фазе при отсутствии растворителя.
«+» Возможность использования блоков полимера без последующей переработки и отсутствие стадии отделения от растворителя.
«-» Сложность отвода выделяющего тепла, особенно при высокой вязкости системы. Вопросы отвода тепла решают путем обрыва процесса на ранних стадия превращения или проведением полимеризационных процессов в несколько стадий.
Полимеризация в растворе - проводят либо в жидкости, смешивающейся с мономером и образующимся полимером («лаковый способ»), либо в среде, растворяющей только мономер. В последнем случае образующийся полимер выпадает из раствора и может быть отделен фильтрованием. Преимущество этих способов - легкость отвода выделяющегося тепла. Недостатки метода связаны с необходимостью дополнительных затрат на подготовку растворителя, отделение и регенерацию растворителя, промывку и сушку полученного полимера. Кроме того, полимеризацию в этом случае трудно довести до полного исчерпания мономера и получить продукт высокой молекулярной массы, так как концентрация мономера непрерывно убывает и на конечной стадии оказывается очень малой.
Полимеризацией в растворе получают по радикальному механизму получают поливинилацетат, полиакрилонитрил, политетрафторэтилен, пенополистирол и некоторые полиакрилаты.
Эмульсионная полимеризация – осуществляется в среде с высокоразвитой поверхностью раздела между несмешивающимися фазами, одна из которых содержит мономер. Инициаторы как ионы, так и радикалы
В эмульсионной полимеризации система включает мономер, инициатор и эмульгатор. Это основной метод получения полимеров на основе сопряженных диенов, гомо- и сополимеров стирола, винилацетата, (мет)акрилатов и т.д.
«+» легкость теплоотвода
«-» дополнительные затраты на очистку продукта от эмульгатора.
Полимеризация в суспензии (гранульная) проводят в воде, диспергируя мономер в виде небольших капель, стабилизированных водорастворимыми полимерами или твердыми гидрофильными порошками. Инициатор обычно растворим в мономере, поэтому полимеризацию в каждой капле можно рассматривать как микроблочную со всеми ее закономерностями.
Газофазная полимеризация – полимеризация мономеров, находящихся в газообразном состоянии. Не нашла широкого применения.
Практически с самого начала реакции образуется твердая фаза, и система становится гетерогенной, т.е. это один из видов гетерогенной полимеризации.
Общая характеристика полимерных веществ, основные понятия и термины. Классификация полимеров по химическому составу: природные, синтетические, модифицированные, гомоцепные, гетероцепные, (примеры). Классификация полимеров по физико-химическим свойствам: гибкоцепные и жесткоцепные полимеры.
Общую характеристику см. вопрос №1
По происхождению различают полимеры:
Природные, образующиеся в растительных и животных организмах – крахмал, целлюлоза, белки, нуклеиновые кислоты, натуральный каучук.
Искусственные, полученные химической модификацией природных – триацетат целлюлозы, нитроцеллюлоза.
Синтетические, полученные химически синтезом из мономеров илии химической модификацией синтетических полимеров, например, полиэтилен, полистирол, поливинилхлорид..
В зависимости от строения основной цепи, или типа атомов основной цепи, различают:
Гомоцепные полимеры. Основная цепь включает только 1 тип атомов или 1 химический элемент. Карбоцепные – основная цепь атом углерода. Классифицируют по природе бокового заместителя.Поливиниловый спирт, поливинилацетат, полиакролеин.
Гетероцепные полимеры. Основная цепь построена из 2 или более типов атомов или химических элементов. Классифицируют в зависимости от природы функциональной группы, повторяющейся в основной цепи. Полиэтилен, полипропилен, поливинилхлорид.
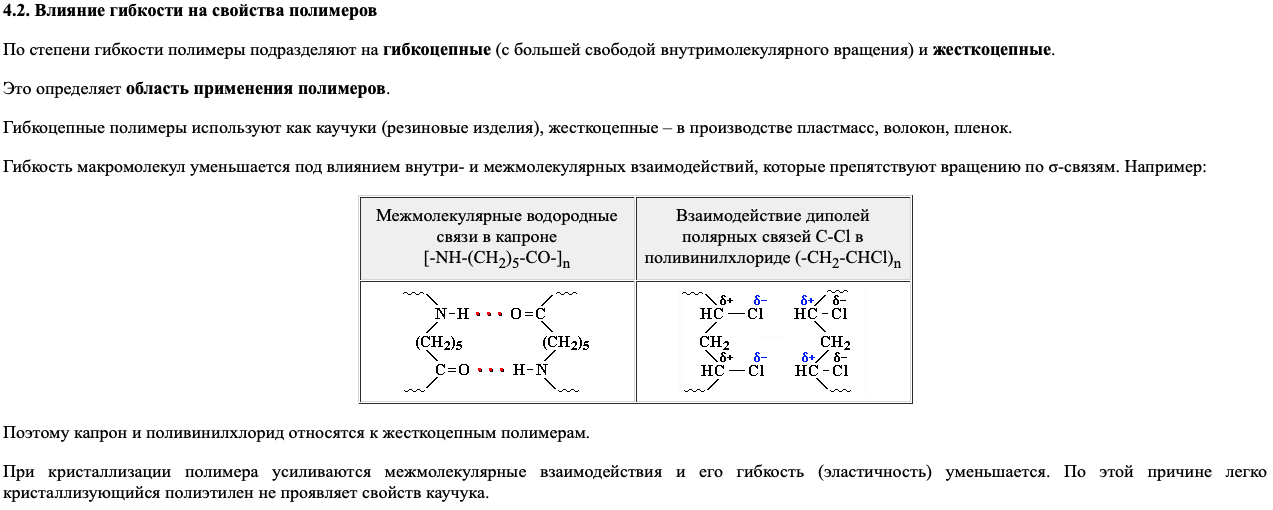
Особенности растворения полимеров. Две стадии растворения. Набухание межструктурное, внутриструктурное, ограниченное, неограниченное. Факторы, влияющие на набухание и растворение полимеров. Понятие степени набухания. Кинетика набухания.
Две стадии растворения: набухание (молекулы растворителя диффундируют в полимер) и собственно растворение (односторонняя диффузия молекул растворителя в объём полимера).
Набухание межструктурное, внутриструктурное, ограниченное, неограниченное. Понятие степени набухания. Факторы, влияющие на набухание и растворение полимеров. Кинетика набухания.
Если растворение полимера останавливается на стадии набухания, то говорят об ограниченном растворении, в ином случае растворение неограниченное и идет по всем стадиям. Если много надмолекулярного образования – набухание идет с трудом.
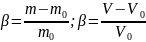
Где β – это степень набухания, m, V – масса и объём набухшего полимера, а m0 и V0 – массы и объём исходного полимера.
На картинке α это β в формуле, то есть степень набухания
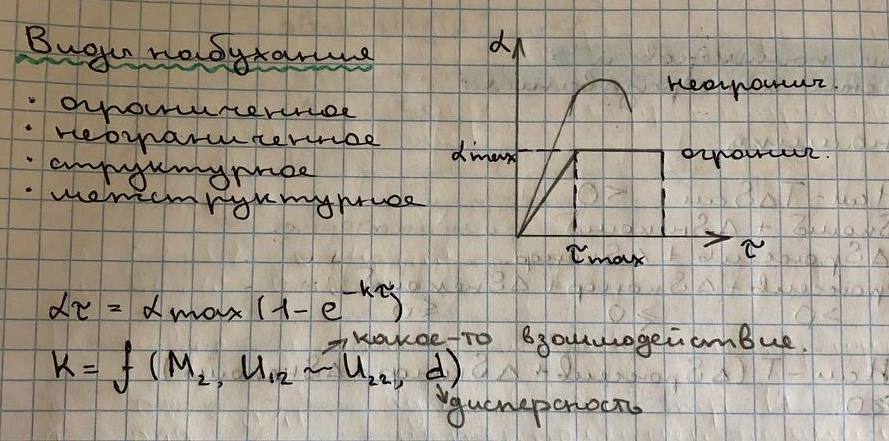
Изменение энтальпии оказывает сильное влияние на стадию набухания. Так же на это влияют дисперсность, внутренняя энергия взаимодействия растворителя и полимера, полимера и полимера, и растворителя и растворителя
Растворы полимеров. Термодинамика набухания и растворения полимеров. Энтальпия смешения. Комбинаториальная (рассеивающая и конформационная) и некомбинаториальная энтропия смешения. Возможные варианты соотношений ΔН и ΔS при растворении полимеров (примеры).

Давление набухания, осмотическое давление растворов полимеров. Вывод уравнения состояния растворов полимеров. Первый, второй и третий вириальные коэффициенты. Классификация растворителей по их термодинамическому сродству к полимеру. Экспериментальное определение молекулярной массы и величины А2.
Диффузия микромолекул способствует осмотическому давлению.
Осмотическое давление – дополнительное давление, которое надо приложить к ячейке с полимером для того, чтобы предотвратить диффузию молекул растворителя.
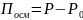
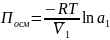 уравнение Вант-Гофа
уравнение Вант-Гофа
a1
– активность;
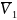 –
мольный объём растворителя;
–
мольный объём растворителя;
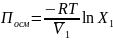
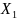 –
мольная концентрация
растворителя
–
мольная концентрация
растворителя
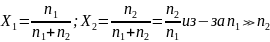
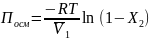
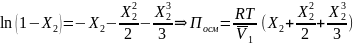
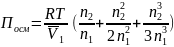

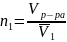
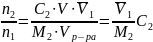
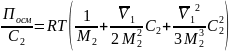
Вириальные коэффициенты:
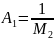 ;
;
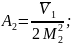 определяет
термодинамическое сродство растворителя
к полимеру
определяет
термодинамическое сродство растворителя
к полимеру
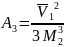 ;
определется энергией макромолекул при
больших концентрациях
;
определется энергией макромолекул при
больших концентрациях
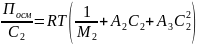 Уравнение состояния
растворов полимеров
Уравнение состояния
растворов полимеров
Классификация растворителей по их термодинамическому сродству к полимеру.
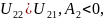 плохой растворитель
плохой растворитель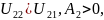 хороший растворитель
хороший растворитель квазиидеальный растворитель,
-растворитель
квазиидеальный растворитель,
-растворитель
Экспериментальное определение молекулярной массы и величины А2.
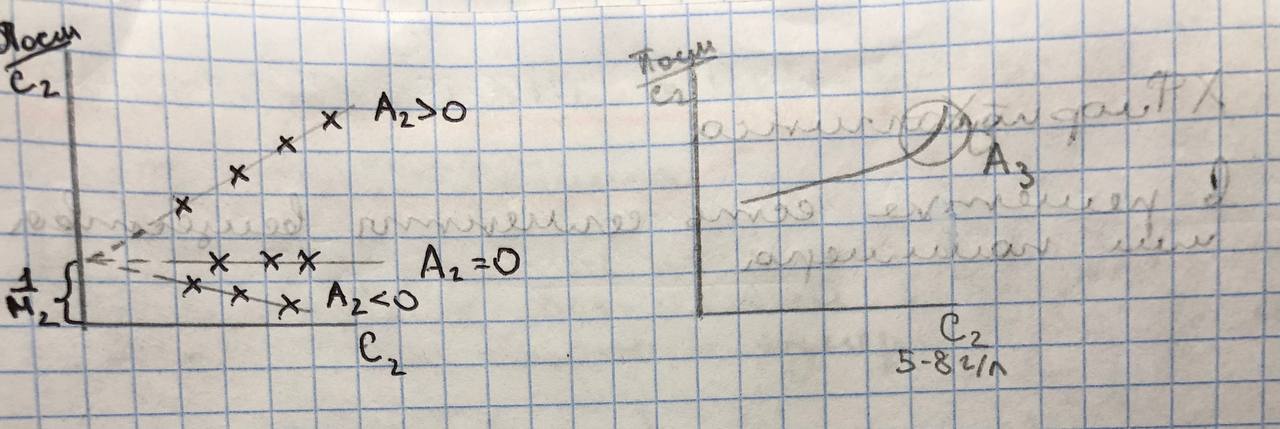
Термодинамическая теория растворов полимеров Флори-Хаггинса. Признаки идеальных растворов. Классификация растворов по отклонению от идеальности. Уравнение состояния растворов полимеров Ф-Х. Константа Хаггинса. Классификация растворителей по их термодинамическому сродству к полимеру. Связь константы Хаггинса с А2. Температура Флори, ее значение для определения молекулярных масс полимеров. экспериментальное определение. Конформации макромолекул в Θ – условиях. Методы определения константы Хаггинса
Идеальный
раствор – такой, при образованиии
которого не будет наблюдаться изменений
температуры, то есть при его образовании
не образуется и не потребляется энергия,
а
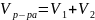
Признаки идеальных растворов.
Близость компонентов
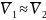
Молекула растворяемого вещества энергетически равноценно взаимодействуют с друг с другом и с растворителем
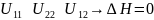
Энтальпия процесса равна нулю, процесс идёт за счет увеличения энтропии
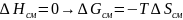
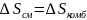
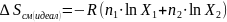
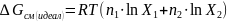
Классификация растворов по отклонению от идеальности.
Регулятрные растворы
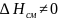 ,
,
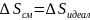
Атермические растворы
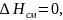
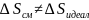
Изоактивные растворы
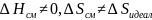 ,
,
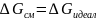
Уравнение состояния растворов полимеров Ф-Х. Константа Хаггинса.
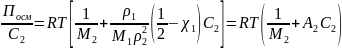
Связь константы Хаггинса с А2.
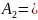
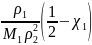
Классификация растворителей по их термодинамическому сродству к полимеру.
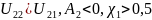 плохой растворитель
плохой растворитель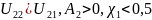 хороший растворитель
хороший растворитель квазиидеальный растворитель,
-растворитель
квазиидеальный растворитель,
-растворитель

Температура Флори, ее значение для определения молекулярных масс полимеров. экспериментальное определение. Конформации макромолекул в Θ – условиях. Методы определения константы Хаггинса
Фазовые равновесия в растворах полимеров. Правило фаз Гиббса для систем полимер-растворитель. Диаграммы состояния. Бинодаль, фазовое состояние полимерного раствора выше и ниже бинодали. Фазовые диаграммы состояния с верхней (ВКТС) или нижней (НКТС) критическими температурами смешения. Зависимости ВКТС и НКТС от молекулярной массы полимера. Для растворов каких полимеров характерны ВКТС и НКТС (примеры)? Зависимость растворимости полимеров от температуры в случаях ВКТС и НКТС, специфика приготовления растворов.
Фазовое поведение истинных растворов описывается правилом фаз Гиббса. Для конденсированных несжимаемых систем, когда можно пренебречь влиянием давления, правило фаз Гиббса записывается в виде
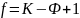
Где f-число степеней свободы (число независимых ТД переменных, температура, концентрация и т.д; К- число компонентов; Ф-число фаз
Графическое изображение = диаграмма состояния/фазовая диаграмма. Для 2х компонентных систем «аморфный полимер-низкомолекулярная жидкость» = кривая растворимости, кривая взаимного смешения в координатах температура состав.

Линия
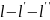 ,
разделяющая области составов, отвечающая
однофазной ии двухфазной системам –
бинодаль.
,
разделяющая области составов, отвечающая
однофазной ии двухфазной системам –
бинодаль.

Концентрация
отвечающая ВКТР = критическая концентрация
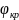 .
ВЫШЕ БИНОДАЛИ = ИСТИННЫЙ РАСТВОР,
НИЖЕ = НАСЫЩЕННЫЙ РАСТВОР ПОЛИМЕРА В
РАСТВОРИТЕЛЕ, НА БИНОДАЛИ = НАС. Р-Р Р-ЛЯ
В ПОЛИМЕРЕ.
.
ВЫШЕ БИНОДАЛИ = ИСТИННЫЙ РАСТВОР,
НИЖЕ = НАСЫЩЕННЫЙ РАСТВОР ПОЛИМЕРА В
РАСТВОРИТЕЛЕ, НА БИНОДАЛИ = НАС. Р-Р Р-ЛЯ
В ПОЛИМЕРЕ.
Чем выше молекулярная масса, тем выше ВКТС(ВКТР)
Типичные примеры
ВКТС полистирол-циклогексан,
полиизобутилен-бензол, ацетилцеллюлоза-бензол.


Метилцеллюлоза-вода, полиэтиленоксид-вода, нитроцеллюлоза-этиловый спирт.

Молекулярная масса и молекулярномассовое распределение полимеров. Среднечисловая, среднемассовая и средневязкостная молекулярные массы. Соотношение между ними для полидисперсных систем. Коэффициент полидисперсности. Дифференциальные кривые молекулярномассового распределения. Экспериментальные методы определения среднечисловой среднемассовой и средневязкостной молекулярных масс
Молекулярная
масса для полимеров также служит мерой
длины полимерной цепи – степень
полимеризации (число мономерных звеньев
в полимерной цепи).
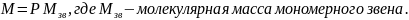 Для синтетических полимеров не выполняется
закон постоянства состава.
Для синтетических полимеров не выполняется
закон постоянства состава.

Наиболее полной характеристикой полидисперсности полимеров являютяс функции ММР. Дифференциальные и интегральные. Каждая из них может быть числовой или весовой.
Дифференциальной числовой (весовой) функцией ММР является зависимость числовой доли макромолекул данной фракции от их молекулярной массы. Экспериментальные дифф. функции ММР выглядят как непрерывные функции.
Интегральная числовая функция ММР определяет суммарную числовую долю всех макромолекул массой меньшей или равной М.
Интегральная весовая функция ММР – суммарную массовую долю данных макромолекул массой меньшей или равной М.

Для
полидисперсных полимеров молекулярная
масса, экспериментально определяемая
методом
вискозиметрии
– средневязкостная молекулярная масса
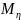
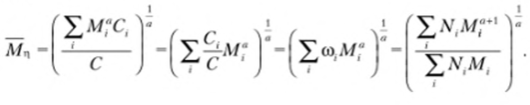
На практике кривые ММР экспериментально получают методами фракционирования, т.е. разделением полидисперсных образцов на фракции с различными молекулярными массами. Методы фракционирования разделяют на препаративные, при которых выделяют фракции и изучают их свойства, и аналитические, когда кривые распределения получают без выделения отдельных фракций. К первым относятся:
Фракционное осаждение;
Фракционное растворение;
К последним:
Ультрацентрифугирование;
Турбидиметрическое титрование;
Гель-проникающую хроматографию;
Молекулярная масса и молекулярномассовое распределение полимеров. Фракционирование полимеров. Термодинамические основы фракционирования полимеров. Критическое значение константы Хаггинса, при котором полимер перестает растворяться в растворителе. Методы фракционирования полимеров: дробное осаждение, дробное растворение, разделение на хроматографических колонках, турбидиметрическое титрование, гель-проникающая хроматография. Описание, достоинства и недостатки.
Чем
больше молекулярная масса, тем хуже
растворимость. При равновесии характер
распределения каждой фракции со степенью
полимеризации
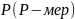 между концентрированной и разбавленной
фазами в общем виде описывается следующим
уравнением:
между концентрированной и разбавленной
фазами в общем виде описывается следующим
уравнением:
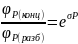 (1)
(1)
Где
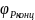 и
и
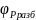 – объемные доли P-мера
в концентрированной и разбавленной
фазах соответственно;
– объемные доли P-мера
в концентрированной и разбавленной
фазах соответственно;
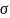 -безразмерный
параметр, не зависящий от P.
-безразмерный
параметр, не зависящий от P.
Уравнение
(1) является основным уравнением теории
фракционирования.
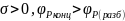 .
Чем > степень полимеризации, тем ,
больше
.
Чем > степень полимеризации, тем ,
больше
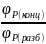 .
При фазовом разделении происходит
существенное обогащение концентрированной
фазы высокомолекулярными фракциями.
.
При фазовом разделении происходит
существенное обогащение концентрированной
фазы высокомолекулярными фракциями.
Экспериментально препаративное фракционирование проводят в режимах фракционного осаждения и фракционного растворения.
Метод фракционного осаждения состоит в последовательном осаждении из раствора полимера ряда фракций, молекулярные массы которых монотонно убывают. Вызвать осаждение фракций полимера можно различными способами:
Добавлением осадителя (смешивающейся с растворителем жидкости, в которой полимер нерастворим) к раствору полимера при постоянной температуре;
Испарением растворителя, если полимер был предварительно растворен в смеси «растворитель-осадитель» (растворитель должен быть более летучим, чем осадитель);
Изменением температуры раствора, которое приводит к ухудшению термодинамического качества растворителя и фазовому разделению.
Метод фракционного растворения состоит в последовательном экстрагировании полимера серией жидкостей, представляющих собой смеси «растворитель-осадитель» различного состава. Растворяющая способность этих смесей по отношению к данному полимеру последовательно возрастает по мере увеличения содержания растворителя. Преимуществом этого метода является то, что исходный полимер может быть твердым, в виде коацервата или пленки на инертном или активном носителе. Растворяемые при этом фракции характеризуются последовательно возрастающей молекулярной массой.
Метод турбидиметрического титрования предназначен для качественной оценки молекулярно-массового распределения (ММР) полимера без выделения отдельных фракций. Метод состоит в измерении мутности раствора полимера при добавлении осадителя. По мере добавления осадителя мутность растет до тех пор, пока не выделится весь полимер, после чего мутность остается постоянной. Количественный метод. Недостатки возможно старение, агрегация, изменение размера частиц вследствие набухаемости, коагуляция частиц, нельзя достичь равновесия, нужно постоянно поддерживать условия, в которых проводится эксперимент. Преимущества – быстрота и возможность работать с очень малыми количествами полимера ( до неск. Миллиграммов). Полезен при подборе систем «растворитель-осадитель».
Фракционирование по методу ГПХ. В колонку, заполненную частицами геля в растворителе, вносят раствор полидисперсного полимера и вымывают полимер растворителем. Растворитель: ТГФ, вода, толуол и т.д. Условия вымывания выбирают таким образом, чтобы успевало установится диффузионное равновесие между наружным и внутренним объемом частиц геля. Регистрацию осуществляют с помощью с помощью детекторов (проточный дифференциальный рефрактометр, который сочетают с спектрофотометром и вискозиметром).
Критическое значение константы хагинса больше 0,5 перестает растворяться.
Колоночная хроматография – способ препаративного разделения смесей жидких или твердых веществ, основанный на различном сродстве разделяемых веществ к неподвижной (сорбент) и подвижной (элюент) фазам. Как правило, чем лучше вещество сорбируется неподвижной фазой - тем медленнее вещество выходит с колонки.
