
диссертации / 92
.pdf31
геморрагического инсульта.
Таким образом, не существует однозначного мнения относительно влияния уровня АД в острейшей фазе инсульта на выраженность сопутствующего перифокального отека мозга, исход и смертность. С
другой стороны, в некоторых исследованиях было показано, чрезмерное снижение АД может сопровождаться ухудшением церебрального перфузионного давления и нарастанием повреждения мозга, что возможно при повышенном внутричерепном давлении. Так, в
клиническом исследовании SCAST изучали целесообразность снижения АД в остром периоде инсульта (как ишемического, так и геморрагического). Пациенты рандомизированы в группы кандесартана и плацебо. Оказалось, что в группе лечения кандесартаном уровень АД был статистически значимо ниже, чем в группе плацебо, при этом исходы не отличались в обеих группах. Таким образом, в этом клиническом исследовании показано не только отсутствие необходимости снижения АД с помощью препарата кандесартан у пациентов с острым инсультом и высоким уровнем АД, но и продемонстрирован отрицательный эффект от снижения АД.
По всей видимости, такие результаты можно объяснить тем, что в этом клиническом исследовании оценивались пациенты как с ишемическим, так и с геморрагическим инсультом, что на наш взгляд не совсем верно, так как известно, что чрезмерное снижение АД в остром периоде ишемического инсульта может привести к развитию повторного инсульта [26; 28; 36; 57; 78].
В доступной литературе мы не выявили четких рекомендаций относительно целевого уровня АД, достигаемого в лечении гипертонического криза, осложненного геморрагическим инсультом, а
-
32
также возможности снижения АД до более низких цифр. Остается открытым вопрос о скорости снижения АД. Также не совсем ясно, чем руководствоваться в выборе оптимального препарата гипотензивного препарата для данной категории пациентов. Это и определило необходимость данной работы.
Глава 2. Характеристика больных и методы исследования.
-
33
2.1. Характеристика больных
В соответствии с поставленной целью и задачами в исследование были включены 86 пациентов в возрасте 61 (52-72) лет, 42 мужчины и 44 женщины.
Критериями включения были пациенты старше 18 лет, госпитализированные в отделение нейрореанимации ГКБ №12 с гипертоническим кризом, осложненным геморрагическим инсультом.
Все пациенты были доставлены бригадой СМП в течение 1-2
часов от начала симптомов (учитывались данные талона скорой медицинской помощи).
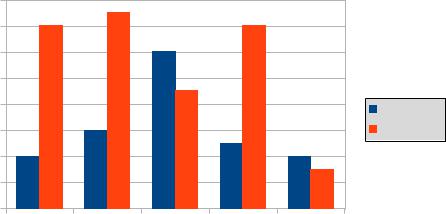
На схеме 1 представлены исходные характеристики пациентов в соответствии с возрастным и половым составом исследуемой группы.
16 |
|
|
|
|
14 |
|
|
|
|
12 |
|
|
|
|
10 |
|
|
|
|
8 |
|
|
|
Женщины |
n |
|
|
|
|
6 |
|
|
|
Мужчины |
4 |
|
|
|
|
2 |
|
|
|
|
0 |
|
|
|
|
34-49 |
50-59 |
60-69 |
70-79 |
80-89 |
|
|
Возраст, лет |
|
|
Схема 1. Возрастной и половой состав группы. |
||||
Как видно из схемы 1, распределение женщин в возрастных группах близкое к нормальному, в то время как у мужчин оно было более закономерным. И наибольшее количество женщин с гипертоническим кризом, осложненным геморрагическим инсультом
-
34
пришлось на возраст 60-69 лет.
Из исследования исключались пациенты с ишемическим инсультом, субарахноидальным кровоизлиянием, пациенты с артерио-венозной мальформацией, нарушениями ритма и проводимости, гемодинамически значимыми клапанными пороками,
декомпенсацией хронической сердечной недостаточности, сахарного диабета, онкологическими заболеваниями, анемией средней и тяжелой степенями. Кроме того, нами были исключены пациенты с печеночной и/или почечной недостаточностью.
2.2. Хирургическое лечение гематомы
В задачи хирургического лечения входило максимально полное удаление сгустков крови с минимальным повреждением окружающей массы паренхимы головного мозга.
Показаниями к хирургическому лечению являлись:
1)субкортикальная или путаменальная гематома объемом более 20 мл или диаметром более 3 см, сопровождающаяся неврологоческим дефицитом и приводящая к дислокации мозга
2)вентрикулярное кровоизлияние, приводящее к окклюзии желудочков мозга
3)при наличии геморрагического инсульта мозжечка – объем гематомы 14 мл и более, дислокация ствола мозга, окклюзионная гидроцефалия
Абсолютными противопоказаниями к хирургическому мешательству были нарушения бодрствования до комы, нестабильная гемодинамика.
Относительными противопоказаниями были тяжелая соматическая патология (коагулопатия, декомпенсация сахарного диабета, декоменсация хронической сердечной недостатосности,
дыхательная недостаточность); возраст больных старше 70-75 лет.
-
35
Среди исследуемой группы больных 13 пациентам было выполнено хирургическое вмешательство по поводу дренирования гематомы. Это был наиболее тяжелый контингент больных, которые напрявлялись на операцию с купированным гипертоническим кризом и со стабильным уровнем АД. В исследовании выживаемости эти пациенты считались цензурированными до момента нейрохирургической операции.
2.3. Лабораторные исследования.
Поскольку в нашем исследовании анемия средней и тяжелой степени, декомпенсация сахарного диабета, почечная, печеночная недостаточностью являлись критериями исключения, всем пациентам в качестве скринингового исследования были выполнены клинический и биохимический анализы крови (оценка уровня электролитов, мочевины, креатинина, глюкозы, печеночных трансаминаз).
2.4. Инструментальные методы обследования.
Всем пациентам с целью исключения острого коронарного синдрома, а также нарушений ритма и проводимости было выполнено электрокардиографическое исследование аппаратом <Shiller AT-2 plus>.
Кроме того, для исключения застойных явлений в легких пациентам выполнялась обзорная рентгенография органов грудной клетки аппаратом <Toshiba, Raffain>.
2.5. Эхокардиографическое исследование.
На старте исследования всем пациентам проводилось эхокардиографическое исследование. Тяжесть состояния пациентов
-
36
позволяла в основном оценить фракцию выброса левого желудочка
(ФВ ЛЖ), исключить гемодинамически значимые клапанные пороки,
тяжелые локальные дисфункции ЛЖ.
Эхокардиографическое исследование на аппарате Siemens Sequoia 512 выполнялось всем пациентам одним исследователем, в
М- и В- режимах, в стандартных эхокардиографических позициях.
Размеры полостей ЛЖ, толщина межжелудочковой перегородки и задней стенки ЛЖ, переднезадний размер ЛП измерялись по методу Тейхольца. Диаметр выносящего тракта ЛЖ определялся в В-режиме.
ФИ, КДО и КСО ЛЖ оценивались методом Симпсона. Исследовалось также отношение диаметра ЛП и конечного диастолического размера ЛЖ, отражающее объёмную нагрузку на левые отделы сердца.
Ударный и сердечный индексы определялись с помощью импульсного допплера (датчик 3,5 МГц) при установке контрольного объема в путях оттока ЛЖ на уровне выносящего тракта.
Кроме того, больным проводилось допплеровское эхокардиографическое исследование из верхушечной четырехкамерной позиции. При этом оценивались максимальная скорость кровотока в фазу раннего наполнения (Е), максимальная скорость кровотока в фазу позднего наполнения (А), и их соотношение (Е/А).
Выполнялось также тканевое допплеровское картирование, при котором оценивались скорости движения латеральной и медиальной частей фиброзного кольца митрального клапана (Еа лат. и Еа мед.
соответственно).
2.6. Мониторинг АД.
Всем пациентам, госпитализированным в отделение нейрореанимации с гипертоническим кризом, осложненным геморрагическим инсультом, проводился мониторинг неинвазивного
-
37
измерения АД с помощью прикроватного монитора <General Electric, Dash 3000>. Этот метод относится к непрямому измерению АД и представляет собой сфигмоманометр Рива-Роччи, состояший из манжетки и ртутного манометра, измеряющего АД в манжетке.
С момента поступления в отделение нейрореанимации и до момента купирования гипертонического криза шаг измерения АД составлял 5 минут. Затем шаг измерения АД был увеличен до 20
минут.Учитывая шаг измерения АД с помощью прикроватного монитора, мы выбрали две условные точки: 20-я и 220-я минуты от начала лечения.
2.7. Оценка тяжести неврологических проявлений.
После госпитализации пациента в отделение нейрореанимации врачами-неврологами были определены сила и объем мышечных движений в конечностях, которые выражалась в баллах от 0 до 5:
Шкала оценки силы мышц:
0 баллов — нет произвольных движений, паралич.
1 балл — едва заметные сокращения мышц, ощущение напряжения при попытке совершить произвольное движение;
2 балла — движение возможны в полном объеме только по плоскости (без преодоления силы тяжести), при удобном расположении с упором на скользкую поверхность;
3 балла — присутствует сокращение объёма движений в суставе,
движение в полном объеме под действием только силы тяжести,
больной может оторвать конечности от поверхности; 4 балла — больной может совершать движения в полном объеме
под действием силы тяжести, при наличии небольшого внешнего противодействия, легкое снижение силы мышц;
5 баллов — нормальная сила мышц, полный объём движений под
-
38
действием силы тяжести с максимальным внешним противодействием.
В дальнейшем после выписки больныго из стационара для оценки степени инвалидизации и функциональной независимости пациента, перенесшего инсульт, нами была использована
модицифицированная шкала Рэнкина (The Modified Rankin Scale).
Шкала позволила объективизировать динамику симптомов и
функциональных нарушений:
0 баллов – симптомы отсутствуют.
После перенесенного инсульта у пациента отсутствуют какие-
либо остаточные симптомы, не возникло никаких ограничений.
1 степень – отсутствие существенных нарушений жизнедеятельности, несмотря на наличие некоторых симптомов:
способен выполнять все повседневные обязанности.
Предполагает отсутствие признаков инвалидности. Больной в состоянии выполнить без посторонней помощи все действия по уходу за собой. Однако это не исключает наличие у больного мышечной слабости, расстройств чувствительности, нарушений речи или других признаков неврологического дефицита. Эти нарушения выражены в незначительной степени и не ведут к ограничению активности.
2 степень – легкое нарушение жизнедеятельности:
неспособен выполнять прежние обязанности, однако справляется с собственными делами без посторонней помощи.
Предполагает наличие легких признаков инвалидности, но
больной в состоянии обслуживать себя без посторонней помощи.
3 степень – умеренное нарушение жизнедеятельности;
потребность в некоторой помощи, но ходит самостоятельно.
Пациент нуждается в некоторой посторонней помощи при одевании,
гигиеническом уходе за собой, больной не в состоянии внятно читать
-
39
или свободно общаться с окружающими. Пациент может
пользоваться ортопедическими приспособлениями или тростью.
4 степень - выраженное нарушение жизнедеятельности;
неспособен ходить, справляться со своими физическими
потребностями без посторонней помощи.
Предполагается, что у пациента имеются выраженные признаки инвалидности. Больной не в состоянии ходить и ухаживать за собой без посторонней помощи, он нуждается в круглосуточном присмотре. При этом пациент в состоянии самостоятельно или при минимальной помощи со стороны выполнять какую-то часть мероприятий по уходу за собой.
5 степень – грубое нарушение жизнедеятельности; прикован к постели, недержание кала и мочи, потребность в постоянной помощи медицинского персонала.
6 степень – смерть пациента.
2.8. Компьютерная томография.
Компьютерная томография головного мозга проведена всем 86 больным сотрудниками рентгенологического отделения ГКБ №12 аппаратом <Toshiba, Aquilion Prime>.
Исследование производили сразу при поступлении пациента в приемное отделение. Сканирование проводили в спиральном режиме, толщина сканов составила 1 мм с последующей мультипренарной реконструкцией. Определяли площадь высокоплотной части гематомы, окружающей зоны пониженной плотности (отека), общую площадь патологического очага, выраженность и распространенность кровоизлияний, наличие и степень выраженности поперечной и аксиальной дислокации мозга.
-
40
Кроме того, при необходимости пациентам выполнялась КТ в динамике (для оценки изменений объема гематомы, при ухудшении неврологической симптоматики с целью подтверждения дислокационного синдрома, отека мозга, повторного кровоизлияния,
а также после хирургического вмешательства).
2.9. Статистическая обработка результатов.
Полученные данные обрабатывались с помощью пакета статистических программ STATISTICA for Windows 6.1 (StatSoft, Inc., 2004). В отсутствие нормального распределения использовались непараметрические методы определения статистической значимости различий: для двух независимых групп – критерий Манна-Уитни
(PMW), для двух зависимых – критерий Уилкоксона (PW). Различия считались достоверными при p < 0,05.
Для оценки значимости показателей вычислялась медиана значений конкретного показателя по всей выборке, после чего производилось деление больных на группы выше или ниже медианы.
Исследование выживаемости проводилось с помощью построения кривых Каплана-Мейера с оценкой статистической значимости с применением критерия Гехана-Вилкоксона.
Все приведенные данные, если это не оговорено иначе,
представлены в виде медианы и значений интерквартильного размаха.
2.10. Гипотензивная терапия.
Первоначально пациенты были рандомизированы методом конвертов на две группы: группа интенсивного снижения АД исследователем (n=28) и группа гипотензивной терапии, принятой в
-
