
протоколы всеее
.pdfПроизвели идентификацию выделенной чистой культуры с использованием следующих тестов:
-оксидазный и каталазный – положительно,
-окисление сахаров путем посева на чашки с 20% сывороточным агаром, содержащие один из углеводов (глюкоза, мальтоза, сахароза, лактоза, фруктоза) и индикатор;
-посев на бессывороточный МПА;
-посев на 20% сывороточный агар с 0,2% желчи.
Посевы поместили в термостат на сутки при +37°С.
4 этап
Учет дифференциальных тестов:
-окисление сахаров: глюкоза «+», мальтоза «+», сахароза «-», лактоза «-», фруктоза «-»;
-на бессывороточном МПА - рост отсутствует;
-на 20% сывороточномагаре с 0,2% желчи – рост отсутствует. Идентифицировали вид нейссерий с помощью таблицы.
Произвели определение серогруппы, выделенной культуры Neisseria meningitidis в реакции агглютинации на стекле с помощью агглютинирующих сывороток против менингококков серогрупп А, В, С. Для этого на предметное стекло, разделенное маркером на три части, нанесли физ. раствор (по капле на каждую часть). Далее стерильной петлей с поверхности агаровой среды отобрали культуру менингококков и тщательно суспендировали в каплях физиологического раствора на стекле. После этого, если не выявлено спонтанной агглютинации с физ. раствором, в три подготовленные части добавили антисыворотки А, В и С (по капле) и перемешали.
Учет реакции произвели через 1 - 2 мин. Наблюдали образование крупных хлопьев на фоне полного просветления агглютинационного поля в капле с антисывороткой А и гомогенное помутнение в каплях с антисыворотками В и С.
Заключение
На основании изученных морфологических, тинкториальных, культуральных, биохимических, антигенных свойств считаем, что из ликвора больного с подозрением на гнойный менингит выделена культура
Neisseria meningitidis серогруппы А.
Протокол № 18 Бактериологическое исследование отделяемого дыхательных путей
больного с подозрением на коклюш
1 этап исследования
У больного с подозрением на коклюш на 2-й неделе заболевания произвели забор материала двукратно ежедневно натощак. Для этого слизь с задней стенки глотки отобрали «заднеглоточными» тампонами (последовательно сухим, затем смоченным физиологическим раствором по прописи Е.А. Кузнецова).
Исседуемый материал доставили в лабораторию при температуре +3537°С в течение 2 часов.
Посев материала произвели на две чашки казеиново-угольного агара (КУА): с добавлением селективного фактора (цефалексин 40 мг/л среды) и без него. Материал тщательно втирали тампоном по периферии чашки Петри в виде 4 - 5 площадок, а затем - Z-образным штрихом в центре чашки. Далее стерильным шпателем растерли центральные части посева, не касаясь площадок.
Посевы поставили в термостат при +35°С на 2-5 суток с ежедневным просмотром.
2 этап исследования
Учет роста. Через 72 часа на КУА обнаружили рост небольшого количества выпуклых, влажных, гладких, блестящих с ровными краями, серого цвета с жемчужным оттенком колоний, мягкой (маслянистой) консистенции, легко снимающихся петлей. Произвели просмотр колоний при помощи бинокулярного стереоскопического микроскопа и обнаружили узкий луч света («хвост кометы»), отходящий от центра колонии.
Для накопления чистой культуры бордетелл подозрительные колонии пересеяли сектора пластинки КУА.
Посевы поставили в термостат при +35°С на 2-3 сут.
3 этап исследования
Учет роста. На секторах среды КУА - рост в виде сплошного сероватожемчужного налета. В мазках – Граммелкие овоидные палочки (коккобактерии), расположенные равномерно.
Для идентификации выделенной культуры по антигенным свойствам произвели постановку реакции агглютинации (РА) на стекле со специфическими неадсорбированными сыворотками в разведении 1/10:
-коклюшная «+»,
-паракоклюшная «+»,
адсорбированными монорецепторными сыворотками:
-факторная 1 «+»,
-факторная 14 «-»
Для определения сероварианта коклюшного микроба дополнительно поставили РА на стекле с монорецепторными сыворотками:
-- факторная 2 «-», - факторная 3 «+».
Для изучения биохимических свойств произвели посев выделенной чистой культуры на среду с тирозином (определение фермента тирозиназы), среду с мочевиной (определение фермента уреазы), среду Симмонса (определение способности утилизировать цитраты). Для определения подвижности сделали посев «уколом» в полужидкий агар. Для определения способности расти на простых средах – посев на скошенный МПА.
Посевы поставили в термостат при +35°С на 1-2 сут.
4 этап исследования
Произвели учет дифференциальных тестов:
-на МПА - роста нет,
-на среде с тирозином - изменения цвета среды не обнаружено (фермент тирозиназа отсутствует),
-на среде с мочевиной - изменения цвета среды не обнаружено (фермент уреаза отсутствует),
-на среде Симмонса - изменения цвета среды не обнаружено
(утилизация цитратов отсутствует).
Заключение:
На основании изучения морфологических, тинкториальных, культуральных, антигенных и биохимических свойств считаем, что от больного выделена культура Bordetella pertussis, серовариант 1.0.3.
Протокол № 19 Бактериологическое исследование отделяемого из зева и носа больного с
подозрением на дифтерию
1 этап исследования
У больного с подозрением на дифтерию ротоглотки отобрали отделяемое зева и носа отдельными стерильными ватными тампонами натощак, с использованием шпателя, не касаясь тампоном языка и внутренних поверхностей щек и зубов. Материал из ротоглотки отбирали на границе пораженных и здоровых тканей миндалин, слегка нажимая на них тампоном. Материал из носа отбирали тампоном, который вводили сначала в один, а потом в другой носовой ход, не касаясь крыльев носа снаружи.
Тампоны доставили в лабораторию в течение 3 часов.
Произвели посев материала с тампонов на два сектора (по 1/2 пластинки) кровяно-теллуритового агара (КТА), маркируя их: «зев», «нос». При посеве
на секторе сначала формировали площадку 2х1 см2, затем оставшуюся поверхность засевали частыми штрихами.
Посевы поместили в термостат при +37°С на 1 сутки, при отсутствии роста - оставили на 2-е сутки.
2 этап исследования
Учет роста. На КТА обнаружили рост R-форм колоний: темно-серых, мелких (1 -2 мм), шероховатых в виде «маргаритки».
Произвели постановку основного диагностического теста — определение токсигенности культуры (продукции дифтерийного токсина) в иммунопреципитационном тесте (РП в геле) Элека. Исследовали не менее 2-х колоний, половину каждой из них отсеяли на среду для определения токсигенности дифтерийных микробов (ОТДМ) и необожженной петлей - на среду Пизу для определения цистиназной активности.
Другую половину колонии пересевали на скошенный сывороточный агар для накопления чистой культуры.
Постановка РП в геле по Элеку
На поверхность чашки Петри с ОТДМ поместили диски с дифтерийным антитоксином. Вокруг каждого диска с антитоксином сформировали пять «бляшек»: две бляшки контрольного токсигенного штамма С.diphtheriae tох+ и три — испытуемые.
Чашки с посевами поместили в термостат при +37°С.
3 этап исследования
Учет теста Элека произвели через 18-24 часа, а также — через 48 часов: между диском с антитоксином и испытуемой культурой образовались линии преципитации, которые под углом сливались с линиями преципитации контрольного токсигенного штамма С.diphtheriae tох+ (рис.1).
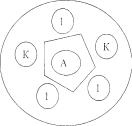
Рис. 1. Схема постановки реакции РП в геле по Элеку с помощью бумажных дисков
Условные обозначения:
А — бумажные диски с антитоксином; К - контрольный токсигенный штамм; 1 - испытуемый материал.
Проба Пизу положительна (в столбике среды вокруг «укола» образовалось облачко черно-коричневого цвета).
Предварительный ответ:
На основании наличия специфических линий преципитации и положительной пробы Пизу от больного выделена культура токсигенных коринебактерий дифтерии.
Для окончательной идентификации вида коринебактерий по биохимическим свойствам произвели посев чистой культуры на среды Гисса (с сахаразой, глюкоза, крахмалом) и добавлением сыворотки, а также в среду с мочевиной (для определения уреазной активности).
Посевы поместили в термостат при +37°С на сутки.
4 этап исследования
Учет дифференциальных тестов:
-сахарозой «-»,
-глюкоза «+»,
-крахмал «+»,
-уреаза «-».
С помощью идентификационных таблиц установили вид и биовар возбудителя.
Заключение:
На основании изучения токсигенных, морфологических, культуральных, биохимических, считаем, что от больного выделена культура C.diphtheriae
биовар gravis tox+.
Протокол № 20
Бактериологическое исследование крови больного с подозрением на брюшной тиф
1 этап исследования
В разгар лихорадки у больного из локтевой вены взяли 10 мл крови с соблюдением соответствующих правил асептики и сразу засеяли во флакон со 100мл среды Раппопорт. Флакон доставили в лабораторию и поставили в термостат при +37° Сс ежедневным просмотром до появления признаков роста бактерий, с максимальным сроком наблюдения до 10 суток.
Параллельно из крови приготовили мазок по типу «толстой капли», окрасили по Граму, при микроскопии обнаружили Грампалочки небольших размеров.
2 этап исследования
Через 24ч. обнаружили помутнение и покраснение среды Раппопорт, отсутствие пузырьков газа в поплавке. Произвели высев выросшей культуры на две среды: пластинку агара Эндо и в полиуглеводную среду Олькеницкого для первичной биохимической идентификации. Посевы поставили в термостат при +37° С на сутки-двое.
3 этап исследования
1. Учет роста.
На пластинке Эндо - колонии 2-3 мм в диаметре, прозрачные, lac- (бесцветные и бледно-розовые).
В среде Олькеницкого обнаружили изменение цвета среды в «столбике» с красно-оранжевого на желтый, без пузырьков газа; скошенная часть цвет не изменила; на границе «столбика» и скошенной части – кольцо черного цвета.
2.Для контроля чистоты выделенной культуры готовили мазки. Обнаружили Грампалочки.
3.Для изучения ферментативных свойств отсеяли чистую культуру в среды минимального дифференцирующего ряда с набором углеводов, многоатомных спиртов, аминокислот и др. в соответствии с идентификационной таблицей; на скошенный МПА - для последующего серотипирования.
4.Выполнили посевы чистой культуры для определения ее чувствительности к сальмонеллезному бактериофагу и антибактериальным препаратам по стандартным методикам.
4 этап исследования
1.Учет ферментативных свойств:
-глюкоза (газ) - «-»
-лактоза - «-»
-сахароза - «-»
-дульцит - «-»
-индол - «-»
-сероводород - «+»
-орнитин - «-»
-лизин - «+»
-цитрат Симмонса - «-»
-ацетат натрия - «-»
2.Провели серотипирование чистой культуры, выросшей на МПА, в реакции слайд-агглютинации последовательно с сальмонеллезными сыворотками:
-поливалентной ABCDE– «+»
-О 9, О12, Оvi - «+»; О2, О4, О6, О7 - «-»
-Нd - «+»
3.Учет определения чувствительности выделенной культуры к поливалентному сальмонеллезному бактериофагу: в месте нанесения капли бактериофага обнаружили зону лизиса на фоне «сплошного газона» исследуемой культуры.
4.Идентифицировали культуру по совокупности ферментативных и антигенных свойств, а также чувствительности к сальмонеллезному фагус помощью таблиц.
Заключение: на основании изучения морфологических, культуральных, ферментативных, антигенных свойств, чувствительности к сальмонеллезному бактериофагу считаем, что из крови больного выделена культура Salmonella enterica subsp. Enterica serovar Typhi.
Протокол № 21
Бактериологическое исследование фекалий больного с подозрением на дизентерию
1 этап исследования
1.2г испражнений отбирали с помощью ложки-шпателя, вмонтированного в крышку стерильного контейнера, сразу после дефекации из дезинфицированного и тщательно вымытого судна, на дно которого был помещен лист плотной чистой бумаги. Материал был доставлен в лабораторию в течение 2 ч.
2.Из нативных испражнений готовили суспензию в стерильной пробирке: 1г фекалий заливали пятью мл 0,9%-ого раствора хлорида, тщательно гомогенизировали, оставляли на 30 мин. для оседания крупных частиц.
2.По 2-3 капли надосадочной жидкости засевали на пластинки дифференциально-селективных сред средами Эндо и Плоскирева, висмутсульфитного агара;
1мл суспензии - в 5 мл селенитовой среды обогащения.
3.Посевы поставили в термостат при +37° Сна сутки-двое.
2 этап исследования
1.Учет роста:
-на среде Эндо и Плоскирева - характерные мелкие, прозрачные, бесцветные колонии;
-на висмут-сульфите - рост отсутствовал;
-в селенитовой среде – диффузное помутнение.
2.Из характерных колоний готовили мазки, обнаружили Грампалочки.
3.Отсевали колонии на среду Олькеницкого.
4.Посевы поставили в термостат при +37° Сна сутки.
3этап исследования
1.Учет роста: в среде Олькеницкого обнаружили изменение цвета среды в «столбике» с красно-оранжевого на желтый, без пузырьков газа; скошенная часть цвет не изменила; почернение отсутствует.
2.Для контроля чистоты выделенной культуры готовили мазки. Обнаружили Грампалочки.
3.Для изучения ферментативных свойств отсевали чистую культуру в среды минимального дифференцирующего ряда с набором углеводов, многоатомных спиртов, аминокислот и др. в соответствии с идентификационной таблицей; на скошенный МПА - для последующего серотипирования.
4.Выполнили посевы чистой культуры для определения ее чувствительности к дизентерийному бактериофагу и антибактериальным препаратам по стандартным методикам.
5. Посевы поставили в термостат при +37° Сна сутки.
4этап исследования
1.Учет ферментативных свойств:
-глюкоза (газ) - «-»
-лактоза - «+» замедленно
-маннит - «+»
-сахароза - «-»
-дульцит - «-»
-индол - «-»
-сероводород - «-»
-орнитин - «-»
-лизин - «-»
-цитрат Симмонса - «-»
-ацетат натрия - «-»
2.Провели серотипирование чистой культуры, выросшей на МПА, в реакции слайд-агглютинации последовательно с шигеллезными сыворотками:
-поливалентной ФЗН (Флекснера-Зонне-Нью-Кастл)– «+»
-S.flexneri 1-5 - «-»
-S.flexneri 6 - «-»
-S.sonnei (1-2 фазы) - «+»
3.Учет определения чувствительности выделенной культуры к поливалентному дизентерийному бактериофагу: в месте нанесения капли бактериофага обнаружена зона лизиса на фоне «сплошного газона» исследуемой культуры.
4.Идентифицировали культуру по совокупности ферментативных и антигенных свойств, а также чувствительности к дизентерийному фагу с помощью таблиц.
Заключение: на основании изучения морфологических, культуральных, ферментативных, антигенных свойств, чувствительности к дизентерийному бактериофагу считаем, что из фекалий больного выделена культура Shigella sonnei.
Протокол № 22
Бактериологическое исследование фекалий больного с подозрением на эшерихиоз
1 этап исследования
1.2г испражнений отобрали с помощью ложки-шпателя, вмонтированного в крышку стерильного контейнера, сразу после дефекации из дезинфицированного и тщательно вымытого судна, на дно которого был помещен лист плотной чистой бумаги. Материал был доставлен в лабораторию в течение 2 ч.
2.Из нативных испражнений приготовили суспензию в стерильной пробирке: 1г фекалий залили пятью мл 0,9%-ого раствора хлорида, тщательно гомогенизировали, оставили на 30 мин. для оседания крупных частиц.
2.По 2-3 капли надосадочной жидкости засеяли на пластинки дифференциально-селективных сред средами Эндо и Плоскирева, висмутсульфитного агара;
1мл суспензии - в 5 мл селенитовой среды обогащения.
3.Посевы поставили в термостат при +37° Сна сутки-двое.
2 этап исследования
Учет роста:
-на среде Эндо и Плоскирева характерные lac+ колонии темно-красного цвета с металлическим блеском и lacбесцветные колонии;
-на висмут-сульфите–коричневые колонии, при снятии которых петлей под ними не оставалось отпечатка на среде;
-в селенитовой среде – диффузное помутнение.
2.Из характерных колоний готовили мазки, обнаружили Грампалочки.
3.Агглютинировали на стекле культуры из 10 подозрительных колоний поливалентной ОКА-эшерихиозной сывороткой; наблюдали положительный результат с культурой из lacколоний.
4.Отсеяли колонии, давшие положительный результат с ОКА-сывороткой, на среду Олькеницкого и параллельно — на скошенный агар для последующего серотипирования.
5.Посевы поставили в термостат при +37° Сна сутки.
3 этап исследования
1.Учет роста: в среде Олькеницкого обнаружили изменение цвета среды в «столбике» с красно-оранжевого на желтый, с пузырьками газа; скошенная часть цвет не изменила; почернение отсутствует.
2.Для контроля чистоты выделенной культуры приготовили мазки. Обнаружили Грампалочки.
3.Для изучения ферментативных свойств отсеяли чистую культуру в среды минимального дифференцирующего ряда с набором углеводов,
