- •Введение
- •Общая часть
- •1.1. Общая характеристика технологического процесса.
- •1.2 Обзор приборов и средств автоматизации.
- •1.3. Обзор существующих систем автоматического управления тп
- •2. Технологическая часть
- •2.1.Технико-экономическое обоснование выбранной базовой схемы тп.
- •2.2. Подробное описание принципов работы объекта управления.
- •3. Конструкторская часть.
- •3.1.Пути модернизации выбранной базовой схемы.
- •3.2 Составление и описание и расчет функционльной схемы управления разрабатываемого дроссельной диафрагмы.
- •Литература и нормативно-техническая документация
3. Конструкторская часть.
3.1.Пути модернизации выбранной базовой схемы.
Виды пара
Известно, что любое вещество в зависимости от внешних условий (давления и температуры) может находиться в газообразном, жидком и твердом агрегатных состояниях, или фазах, а также одновременно находиться в двух или трех состояниях.
Переход вещества из одного агрегатного состояния в другое называется фазовым переходом, или фазовым превращением. Вещество в разных агрегатных состояниях имеет различные свойства, в частности плотность. Это различие объясняется характером межмолекулярного взаимодействия.
Переход вещества из твердого состояния в жидкое называется плавлением, из жидкого в газообразное — испарением, из твердого в газообразное — сублимацией. Обратные процессы соответственно называются затвердеванием,или кристаллизацией,конденсацией и десублима-цией.
Процесс получения пара из жидкости может осуществляться испарением и кипением. Испарением называется парообразование, происходящее только со свободной поверхности жидкости и при любой температуре.
Кипением называется бурное парообразование по всей массе жидкости, которое происходит при сообщении жидкости через стенку сосуда определенного количества теплоты. При этом образовавшиеся у стенок сосуда и внутри жидкости пузырьки пара, увеличиваясь в объеме, поднимаются на поверхность жидкости.
Процесс парообразования начинается при достижении жидкостью температуры кипения, которая называется температурой насыщения tн и на протяжении всего процесса остается неизменной. Температура кипения, или температура насыщения, tн зависит от природы вещества и давления, причем с повышениемдавления tн увеличивается.Давление,соответствующее tн называ-ется давлением насыщения рн.
Насыщенным паром называют пар, который образовался в процессе кипения и находится в динамическом равновесии с жидкостью. Насыщенный пар по своему состоянию бывает сухим насыщенным и влажным насыщен-ным.
Сухой насыщенный пар представляет собой пар, не содержащий капель жидкости и имеющий температуру насыщения (t=tн) при данном давлении.
Влажный насыщенный пар – это равновесная смесь, состоящая из капель жидкости, находящейся при температуре кипения, и сухого насыщенного пара.
Отношение массы сухого насыщенного пара mс.п. к массе влажного насыщенного пара mв.п. называется степенью сухости х влажного пара, то есть
Очевидно, что для жидкости х=0, для сухого насыщенного пара х=1.
Если к сухому насыщенному пару продолжать подводить теплоту, то его температура увеличится. Пар, температура которого при данном давлении больше, чем температура насыщения (t>tн), называется перегретым. Другими словами говоря перегретый пар – это пар, находящийся при температуре, превышающей температуру кипения жидкости при давлении, равном давлению перегретого пара. Величина превышения температурой пара температуры кипения жидкости называется степенью перегрева пара.
Водяной пар является реальным рабочим телом и может находиться в трёх состояниях: влажного насыщения, сухого насыщения и в перегретом состоянии. Для технических нужд водяной пар получают в паровых котлах (парогенераторах), где специально поддерживается постоянное давление.
Советскими учеными М. П. Вукаловичем и И. И. Новиковым в 1939 г. было получено уравнение для реальных газов с учетом ассоциации и диссоциации их молекул. В общем виде это уравнение записывается в следующей форме:
(2) |
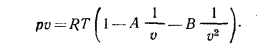
Коэффициенты А и В определяют из равенств:
(2’) |
|
|
|
(2”) |

Приведенное уравнение можно применять к любому реальному газу, и в частности к перегретому водяному пару. Но в связи с тем, что практически это сложное уравнение использовать трудно, с его помощью были вычислены основные физические величины перегретого водяного пара при различных р и Т, составлены таблицы и построена диаграмма в is-координатах, на основании которых и проводятся расчеты процессов изменения состояния водяного пара.
Параметры пара.
Жидкость.
Удельный объем воды при 0![]() и различных давлениях одинаков и равен
0,001 м3/кг
(v0’).
При температурах насыщения и различных
давлениях удельный объем воды (v’)
изменяется в узком диапазоне – от 0,001
(tн
= 0
)
и pн
= 0,61 кПа) до 0,003147 м3/кг
(tн
= tк=
374.116
и pн
= pк=
и различных давлениях одинаков и равен
0,001 м3/кг
(v0’).
При температурах насыщения и различных
давлениях удельный объем воды (v’)
изменяется в узком диапазоне – от 0,001
(tн
= 0
)
и pн
= 0,61 кПа) до 0,003147 м3/кг
(tн
= tк=
374.116
и pн
= pк=
|
В соответствии с первым
законом термодинамики q
= ![]() U
+ А имеем
U
+ А имеем
q' = U' – U’0+р(v' - v) (а)
т.к. при давлениях ниже p
= 4 МПа внешняя работа А незначительна,
ей можно пренебречь, поэтому q'![]() U'
(б)
U'
(б)
При определении энтальпии имеем i' = U' + pv',
i' = q' + U’0 - р(v' – v0) + pv' = q' + U’0 +pv’0 =q' + pv’0
Теплоемкость воды: ![]() (3)
(3)
Считая, что Ср = 4,19 кДж/(кr*К)
const, энтропия ![]() (4)
(4)
Сухой насыщенный пар. Состояние cyxoгo насыщенного пара, который получается в результате подогрева воды до tн, а затем полного ее испарения, определяется одним параметром р или tн (см. Рис. 1). Поэтому все остальные параметры cyxoгo пара (v", s", i" и т:' д.) находят по таблицам насыщенных паров в зависимости от давления или температуры.
Уравнение первого закона термодинамики для процесса парообразования имеет вид:
r = U" - U' + р(v" - v').
Обозначая U"
- U' = ![]() и р(v"
- v') =
и р(v"
- v') =![]() ,
получим: r
=
,
получим: r
= ![]() (где
(где ![]() внутренняя и внешняя теплота
парообразования.)
внутренняя и внешняя теплота
парообразования.)
Внутреннюю энергию cyxoгo
пара определяют по формуле: U"
=![]()
Энтальпию сухого пара определяют:
i'’= U"+ pv’’,
Энтропию:
s" = s'
+![]() (5)
(5)
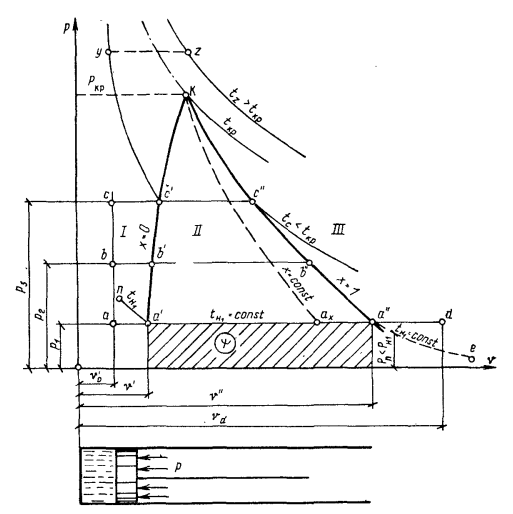
Рис.1 Диаграмма парообразования.
Удельный объем сухого насыщенного пара v" определяется исходя из уравнения:
(6) |
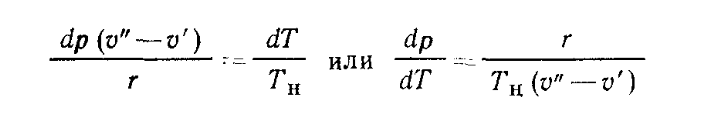
Влажный насыщенный пар. Состояние влажного пара в отличие от cyxoгo характеризуется двумя параметрами: pн (или Tн) и степенью сухости х. Все параметры влажного пара снабжаются индексом х: например vx , U х, ix и т. д. Удельный объем влажноuо пара vx как объем смеси, состоящей из (1- х) кг кипящей воды и х кг cyxoгo пара, находят из равенства vx =(1-х) v' + хv"
откуда, ![]()
![]() (7)
(7)
Для вычисления Uх
используют соотношение: Uх
=![]() (8)
(8)
Энтальпия: ![]() (9)
(9)
Энтропия: ![]() =
s'
+
=
s'
+![]() (10)
(10)
Перегретый пар. Свойства перегретого пара резко отличаются от свойств насыщенного пара и приближаются к свойствам газов и тем больше, чем больше eгo перегрев.
Количество теплоты, необходимой для перевода 1 кг cyxoгo насыщенного пара при постоянном давлении в перегретый с температурой t, называют теплотой перегрева qпер, и определяют по выражению:
(11) |
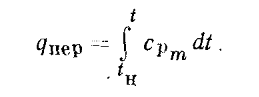
Внутреннюю энергию перегретого пара U находят из равенства:
(12) |
Энтальпию перегретого пара i определяют по известному соотношению
i = U + pv или
(13) |
Энтропию во время процесса
перегрева (см. Рис.1) от![]() до Т вычисляют:
до Т вычисляют:
(14). [3]
|