
- •Практические занятия по физике
- •Часть 1
- •Учебное пособие
- •Краткие теоретические сведения и основные формулы
- •Величина полного ускорения
- •Поступательное движение
- •В случае равномерного вращательного движения угловая скорость
- •Алгоритм решения задач
- •Вращательное движение
- •Примеры решения задач
- •Решение
- •Решение
- •Уравнение движения при равноускоренном движении имеет вид
- •Решение
- •Решение
- •Задачи для самостоятельного решения
- •Краткие теоретические сведения и основные формулы
- •Выражение (2.5) можно записать в виде
- •Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Подставив это выражение в уравнение (2), найдём
- •Решение
- •Подставляя численные значения, получаем
- •Решение
- •Решение
- •Задачи для самостоятельного решения
- •Занятие 3
- •Законы сохранения импульса и момента
- •Импульса. Энергия. Работа. Мощность
- •Контрольные вопросы для подготовки к занятию
- •Краткие теоретические сведения и основные формулы
- •Потенциальная энергия упруго деформированного тела
- •Полная механическая энергия:
- •Для переменного момента силы:
- •Примеры решения задач
- •Решение
- •Решение
- •Перепишем векторное уравнение (1) в скалярном виде
- •Кинетическая энергия начального положения тела
- •Решение
- •Подставив числовые значения, получим
- •Решение
- •Решение
- •Кинетическая энергия диска, вращающегося вокруг своей оси
- •Решение
- •Решение По закону сохранения энергии
- •Задачи для самостоятельного решения
- •Занятие 4
- •Краткие теоретические сведения и основные формулы
- •Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Тогда – плотность газа равна произведению массы одной молекулы на концентрацию молекул. Получим
- •Отсюда получаем изменение давления при утечке газа
- •Задачи для самостоятельного решения
- •Занятие 5
- •Явления переноса. Распределение молекул
- •По энергиям.
- •Контрольные вопросы для подготовки к занятию
- •Краткие теоретические сведения и основные формулы
- •Примеры решения задач
- •Решение
- •Решение Барометрическая формула
- •Задачи для самостоятельного решения
- •Занятие 6 первое и второе начала термодинамики Контрольные вопросы для подготовки к занятию
- •Краткие теоретические сведения и основные формулы Первое начало (закон) термодинамики выражает закон сохранения энергии:
- •На основании первого начала термодинамики
- •Адиабатный процесс
- •Работа, совершаемая газом при адиабатном процессе:
- •Теплоемкость одного моля и удельная теплоемкость при постоянном давлении:
- •Методика решения задач
- •I часть Примеры решения задач
- •Решение
- •Задачи для самостоятельного решения
- •II часть Примеры решения задач
- •Решение
- •Тогда работа
- •Вычислим
- •Решение
- •Решение
- •Задачи для самостоятельного решения
- •Занятие 7 закон кулона. Теорема остроградского – гаусса Контрольные вопросы для подготовки к занятию
- •Краткие теоретические сведения и основные формулы
На основании первого начала термодинамики
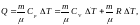
откуда вытекает уравнение Р. Майера для идеального газа:
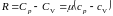 .
(6.12)
.
(6.12)
Изотермический процесс
(Т = const) рV= const; (т = соnst, μ = const);
T = 0, U = 0, Q = A, (6.13)
т.е. теплота, сообщенная газу, полностью идет на совершение работы против внешних сил:
 .
(6.14)
.
(6.14)
Адиабатный процесс
Адиабатным называется процесс, при котором отсутствует теплообмен (Q = 0) между термодинамической системой и окружающей средой.
Из первого начала термодинамики для адиабатного процесса следует
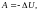 (6.15)
(6.15)
т.е. работа газа против внешних сил совершается за счет убыли его внутренней энергии.
Соотношение между двумя параметрами состояния идеального газа при адиабатном процессе:
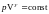 ;
(6.16)
;
(6.16)
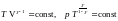
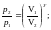
 (6.16а)
(6.16а)
где
=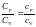 - показатель адиабаты или коэффициент
Пуассона.
- показатель адиабаты или коэффициент
Пуассона.
Работа, совершаемая газом при адиабатном процессе:
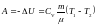 (6.17)
(6.17)
или,
учитывая, что
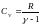
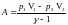 ;
(6.17а)
;
(6.17а)
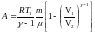 .
(6.17б)
.
(6.17б)
Теплоемкость одного моля и удельная теплоемкость при постоянном объеме определяются соответственно по формулам
 ;
(6.18)
;
(6.18)
 .
(6.19)
.
(6.19)
Теплоемкость одного моля и удельная теплоемкость при постоянном давлении:
 ;
(6.20)
;
(6.20)
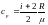 .
(6.21)
.
(6.21)
Отношение теплоемкости газа при постоянном давлении к теплоемкости при постоянном объеме п показатель адиабаты:
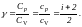 (6.22)
(6.22)
В формулах (6.18 - 6.22) i – число степеней свободы.
Методика решения задач
1. Определить вид процесса, происходящего в газе. Для этого найти, какая величина – р, V или Т - остается постоянной.
2. Записать первое начало термодинамики в интегральной форме.
3. Применить первое
начало к данному процессу. Для этого:
а) определить, совершается ли в данном
процессе работа. Элементарная работа
А = р dV.
Если происходит изменение объема,
значит, работа совершается. Записать
формулу полной работы, взяв интеграл
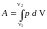 с учетом процесса; б) найти изменение
внутренней энергии
с учетом процесса; б) найти изменение
внутренней энергии
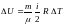 или
или
 ;
в) определить количество теплоты,
сообщенное газу,
;
в) определить количество теплоты,
сообщенное газу,
 или
или
 .
.
4. Решить задачу
численно, найдя нужные параметры,
используя при этом уравнения изопроцессов
или уравнение Менделеева – Клапейрона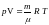 .
.
I часть Примеры решения задач
Задача 1. 10 г кислорода находятся под давлением 3 . 105 Па при температуре 100С. После нагревания при постоянном давлении газ занял объем 10 л. Найти: 1) количество тепла, полученное газом; 2) изменение внутренней энергии газа; 3) совершенную газом работу.

Решение
1. р = const; процесс изобарный.
2. Q = U+ A, где Q – количество тепла, сообщенное газу; U – изменение внутренней энергии газа; А – совершенная газом работа.
3. а) Элементарная работа

Дано:
т = 10 г = 10 –2 кг
=
32 .
10-3
р = 3 . 105 Па = const
t = 100 С; Т = 283 К
V2 = 10 л = 10-2 м3
А- ?U - ? Q - ?
где р – давление газа; dV – бесконечно малое изменение его объема. Из условия задачи видно, что dV> 0, т.е. газ расширяется, тогда работа А > 0, т.е. работа совершается газом против внешних сил. Полная работа расширения
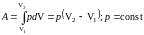 .
.
б) Изменение внутренней энергии равно

где Т – изменение температуры; i – число степеней свободы молекулы кислорода (i = 5, так как кислород – двухатомный газ).
в) Количество теплоты, полученное газом при нагревании, может быть найдено как сумма А и U, или с помощью молярной теплоемкости Ср:
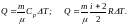
4. Решим задачу численно, сделав некоторые преобразования формул и вычислив недостающие параметры газа.

Используем два уравнения Менделеева – Клапейрона для состояния 1 и 2:
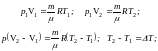

(Справедливо только для изобарного процесса).

Найдем
Т:
Т
= Т2
– Т1;
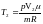 – из уравнения Менделеева – Клапейрона
для второго состояния.
– из уравнения Менделеева – Клапейрона
для второго состояния.
Т
= Т2
– Т1
=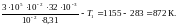
Тогда работа
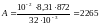 Дж.
Дж.
Изменение внутренней энергии
 Дж.
Дж.
Количество теплоты
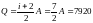 Дж.
Дж.
 .
.
Ответ: А = 2265 Дж; U = 5660 Дж; Q = 7920 Дж.
Задача 2. В закрытом сосуде объемом V = 10 л находится воздух при давлении 105 Па. Какое количество теплоты нужно сообщить газу, чтобы повысить его давление в 5 раз?
Дано: Решение
V = 10 –2 м3 1) Из условия задачи следует, что процесс изохорный,
р1 = 10 5 Па так как сосуд закрытый. Следовательно, V = const.
р2 = 5р1 2) Q = U + A – первое начало термодинамики.
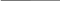
i = 5 3) Применим I начало к изохорному процессу:
Q
- ? а)
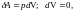 следовательно, А
= 0;
следовательно, А
= 0;
б)
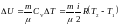 ;
;
в)
 .
.
4) Вычислим разность температур, пользуясь уравнениями состояния для 1 и 2 состояний:
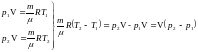 .
.
Тогда

Ответ: Q = 104 Дж.
Задача 3. Некоторая масса азота при давлении р1 = 1 атм имела объем V1 = 5 л, а при давлении р2 = 3 атм – объем V2 = 2 л. Переход от первого состояния ко второму сделан в два этапа – сначала по изохоре, затем по изобаре. Определить изменение внутренней энергии, количество теплоты и произведенную работу.

Дано: Решение Решение

= 28 . 10-3
i = 5
p1 = 1 атм = 105Па
р2 = 3 атм = 3 .105Па
V1 = 5 л = 5 .10-3м3
V2 = 2 л = 2 .10-3м3

U - ? A - ? Q - ?
1) V = const – I процесс; р = сonst – II процесс.
I процесс – изохорное нагревание; II процесс – изобарное сжатие.
2) Первое начало термодинамики

3)
а)
 ;
;
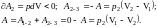
Работа в изобарном сжатии на участке 2-3 отрицательна, так как объем газа уменьшается, газ сжимается под действием внешних сил:
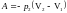 .
.
б)

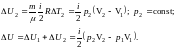
Изменение внутренней энергии зависит только от начального и конечного состояния системы и не зависит от пути перехода.
в) Q = U + A.
Вычисления:

– работу совершают внешние силы.
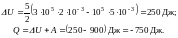
Работа совершается над газом, тепло отводится от газа, газ нагревается (U> 0).
Ответ: А = -900 Дж; U = 250 Дж; Q = -750 Дж.
Задача 4. 10,5 г азота изотермически расширяются при температуре –23 0С от р1 = 2,5 атм до р2 = 1 атм. Найти работу, совершенную при расширении, изменение внутренней энергии и количество тепла, переданное газу.

Дано: Решение Решение

По условию задачи T = const, процесс изотермический
Q = U + A.
a) A = pdV; dV> 0; A> 0;
б)
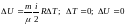 ;
;
в) Q = A все переданное газу тепло идет на работу газа против внешних сил.
т = 10,5 г = 10,5 . 10-3 кг
= 28 . 10-3
t1 = -230C; T1 = 250 К
р1 = 2,5 атм = 2,5 . 105 Па
р2 = 1 атм = 1 . 105 Па

А- ?U - ? Q - ?
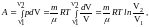
так
как процесс изотермический, то
 т.е.
т.е.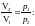

Ответ: А = 713,8 Дж.
Задача 5. 7 г углекислого газа СО2 было нагрето на Т = 10 К в условиях свободного расширения. Найти работу расширения газа и изменение его внутренней энергии.

Дано: Решение

1) Свободное расширение газа означает, что его давление не изменяется, т.е. p = const, процесс изобарный.
2) Q = U + A;
a)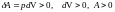 ;
;
i = 6
m = 7 . 10-3кг
= 44 . 10-3
Т = 10 К
А- ? U - ?
 ;
;
T2 – T1 = T;
б)
 .
.
Вычисления:
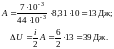
Ответ: А = 13 Дж; U = 39 Дж.
