
- •Органическая химия для школьников
- •Оглавление
- •Предисловие
- •Глава 1. Введение в органическую химию
- •§ 1. Теория химического строения органических соединений А. М. Бутлерова
- •§ 2. Классификация органических соединений
- •§ 3. Строение атомов
- •§ 4. Типы и характеристики химической связи
- •§ 5. Первоначальные представления о типах и механизмах органических реакций
- •Глава 2. Алканы
- •§ 6. Изомерия и номенклатура алканов
- •§ 7. Гомологи. Гомологический ряд алканов
- •§ 8. Строение молекул алканов. Физические свойства алканов
- •§ 9. Химические свойства алканов
- •§ 10. Получение и применение алканов
- •§ 11. Алкены: гомологический ряд, номенклатура, изомерия. Строение молекул алкенов
- •§ 12. Физические и химические свойства алкенов
- •§ 13. Получение и применение алкенов
- •§ 14. Циклоалканы: изомерия, номенклатура, физические свойства и получение
- •§ 15. Строение и химические свойства циклоалканов
- •§ 16. Алкины: изомерия и номенклатура. Строение молекулы ацетилена
- •§ 17. Физические и химические свойства алкинов
- •§ 18. Получение и применение алкинов
- •§ 20. Строение и свойства дивинила
- •§ 21. Каучук. Резина
- •§ 23. Электронное и пространственное строение бензола. Изомерия и номенклатура аренов
- •§ 26. Конденсированные ароматические углеводороды
- •§ 27. Природные источники углеводородов. Нефть
- •Глава 5. Галогенопроизводные углеводородов. Спирты. Фенолы
- •§ 28. Галогенопроизводные углеводородов
- •§ 29. Спирты: классификация, изомерия, номенклатура и методы получения
- •§ 30. Физические и химические свойства спиртов. Водородная связь
- •§ 31. Многоатомные спирты
- •§ 32. Фенолы: классификация, особенности строения, физические свойства. Получение и применение фенола
- •§ 33. Химические свойства фенола
- •§ 34. Простые эфиры
- •Глава 6. Карбонильные соединения. Альдегиды и кетоны
- •§ 35. Альдегиды и кетоны: классификация, номенклатура, изомерия и физические свойства
- •§ 36. Получение альдегидов и кетонов. Строение карбонильной группы
- •§ 37. Химические свойства альдегидов и кетонов
- •Глава 7. Карбоновые кислоты
- •§ 40. Строение карбоновых кислот, их физические и химические свойства
- •§ 41. Важнейшие представители карбоновых кислот
- •§ 42. Гидроксикислоты и кетокислоты. Оптическая изомерия
- •§ 43. Сложные эфиры
- •§ 44. Жиры: строение, свойства, применение и роль в природе
- •Глава 8. Углеводы
- •§ 45. Классификация углеводов. Глюкоза
- •§ 46. Химические свойства глюкозы и ее получение
- •§ 47. Дисахариды
- •§ 48. Полисахариды
- •Глава 9. Амины
- •§ 50. Электронное и пространственное строение аминов. Химические свойства аминов
- •Глава 10. Аминокислоты. Белки
- •§ 51. Классификация, изомерия, номенклатура аминокислот
- •§ 53. Белки
- •Глава 11. Гетероциклические соединения. Нуклеиновые кислоты
- •§ 54. Общая характеристика гетероциклических соединений
- •§ 55. Нуклеиновые кислоты
- •Глава 12. Обобщающие разделы курса органической химии
- •§ 56. Теория химического строения органических соединений как основа курса органической химии
- •§ 57. Полимеры
- •Литература

§ 57. Полимеры
мическом строении веществ // Ученые записки Казанского университета (отд. физ.-мат. и мед. наук). 1862. Вып. 1, отд. 1. С. 1–11].
Синтез и анализ — взаимодополняющие методы установления строения органического соединения. При этом возможности структурного анализа (обнаружение функциональных групп, сопряженных систем, неравноценных водородных атомов и т. д.) заметно возросли с внедрением спектральных методов.
ВОПРОСЫ И УПРАЖНЕНИЯ
1.Химические свойства функциональных групп зависят от того, с каким фрагментом молекулы эти группы соединены: с алкильной, арильной или ацильной группами. Проиллюстрируйте это утверждение на примере следующих функциональных групп: –ОН, –Cl, –NH2.
2.«От химического строения зависят реакции; следовательно, зная эту зависимость и выражая формулой строение, мы выражаем все те превращения, которым вещество может подвергнуться». Это слова А. М. Бутлерова. Подтвердите на конкретных примерах справедливость такого утверждения.
3.На примере галоген- и аминосодержащих органических соединений обсудите проблему взаимного влияния атомов в молекулах.
4.Приведите примеры характерных химических реакций углеводородов, молекулы которых содержат атомы углерода только в sp2-гибридном состоянии.
5.Выберите среди перечисленных соединений те, которые могут выступать в каче-
стве кислот: NH3, C2H2, CCl4, CH4, AlCl3, CH3OH, С6Н5ОН, пиррол. Подтвердите свой выбор соответствующими уравнениями химических реакций.
6.Выберите среди перечисленных соединений те, которые могут выступать в ка-
честве оснований: СН3NH2, C2H2, CCl4, CH4, AlCl3, С2Н5–О–С2Н5, CH3OH, СН3СОNH2, NH2CH2COOН. Подтвердите свой выбор соответствующими уравнениями химических реакций.
§ 57. ПОЛИМЕРЫ
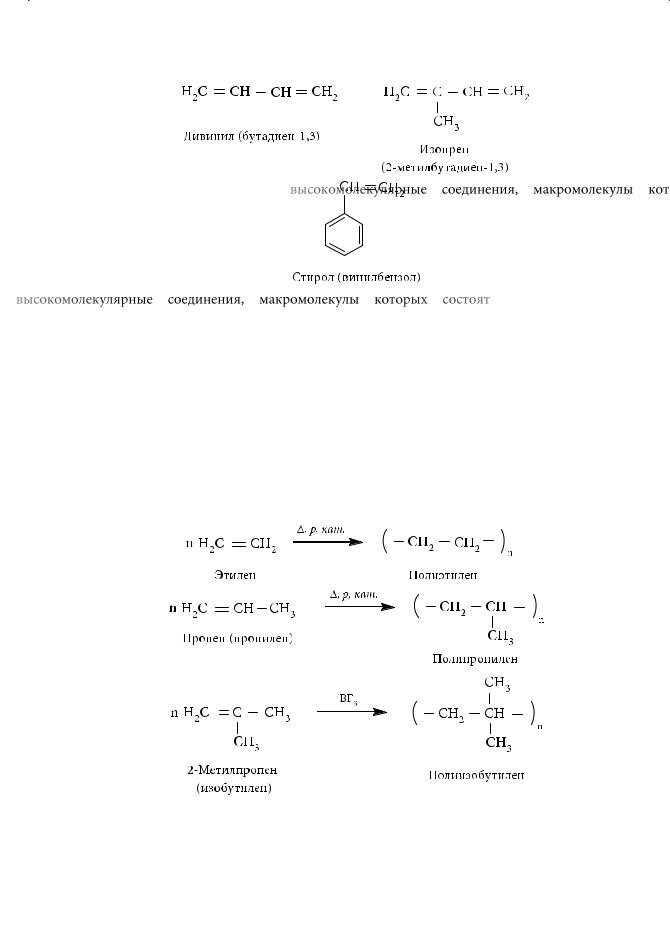
При крекинге нефти образуются алкены (этилен, пропилен, изобутилен и т. д.), при ароматизации и последующем дегидрировании можно получить стирол (винилбензол). Эти непредельные углеводороды далее используются при синтезе спиртов, галогенопроизводных углеводородов, лекарственных препаратов, пластмасс. Из бутан-бутеновой фракции (продукта крекинга нефти) при последующем ступенчатом дегидрировании выделяют бутадиен-1,3, а из изо- пентан-изопентеновой — 2-метилбутадиен-1,3 (изопрен). Эти сопряженные диеновые углеводороды, алкены, стирол — важнейшее сырье для получения синтетических полимерных материалов:
375
Глава 12. Обобщающие разделы курса органической химии
Полимеры — высокомолекулярные соединения, макромолекулы которых состоят из повторяющихся структурных звеньев. Полимеры образуются из мономеров в реакциях полимеризации или поликонденсации. Для того чтобы из конкретного мономера можно было получить полимер (высокомолекулярное соединение), в его молекулах должны присутствовать кратные связи или функциональные группы.
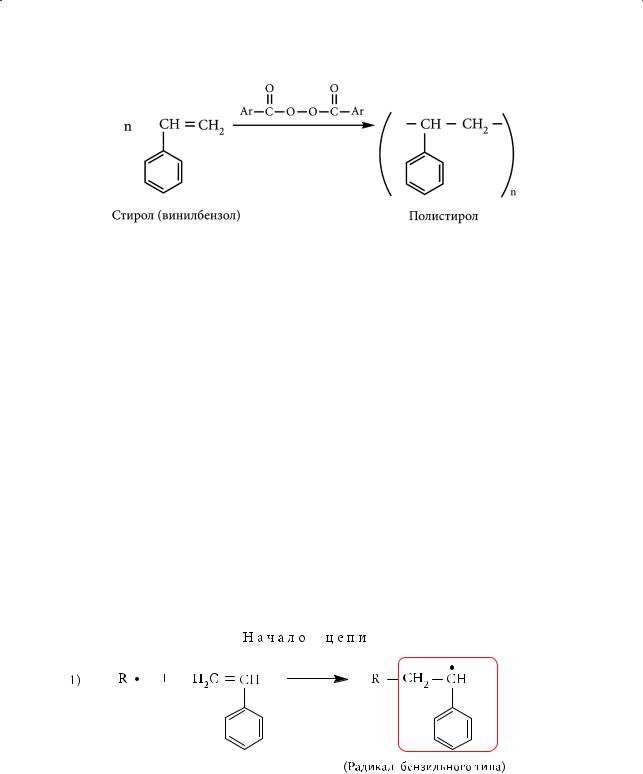
В результате реакций поликонденсации наряду с полимером образуется низкомолекулярный продукт (например, вода, аммиак), а в результате реакций полимеризации — единственный продукт, высокомолекулярное органическое соединение. Так, например, из этилена получают полиэтилен, из пропилена — полипропилен, из изобутилена — полиизобутилен, из стирола — полистирол:
376
§ 57. Полимеры
Использование полимеров в существенной степени определяется их свойствами. Свойства же полимеров зависят от их химического строения (природы мономеров), степени полимеризации, расположения структурных звеньев в пространстве. На физико-химические характеристики полимеров влияют и условия проведения процесса полимеризации.
Различают четыре типа реакций полимеризации: радикальную, катионную, анионную и координационную.
В основе такой классификации лежит природа того инициатора, который активирует молекулу мономера. При радикальной полимеризации в качестве инициаторов обычно выступают органические перекиси, например перекись бензоила, которая, легко образуя свободные радикалы, инициирует процесс полимеризации:
С6Н5СО–О–О–СОС6Н5 → 2 С6Н5СО.
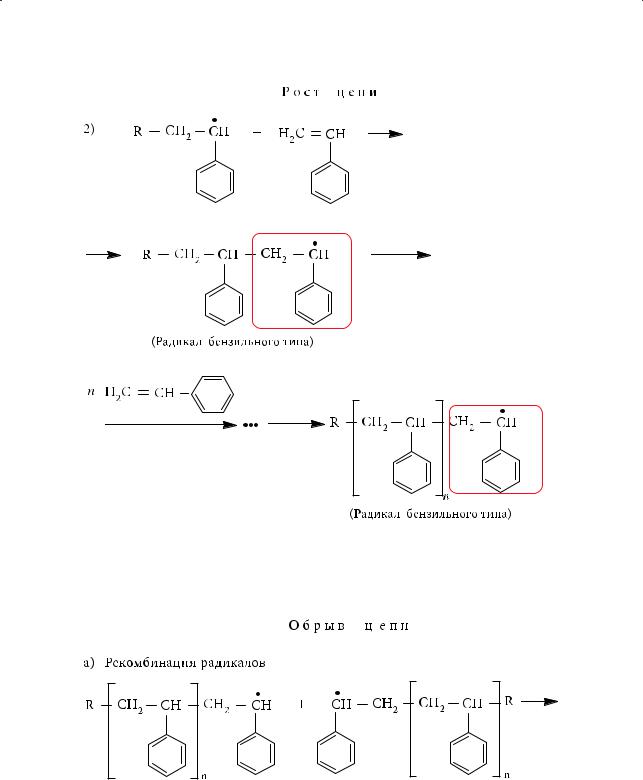
Образующиеся радикалы взаимодействуют с молекулами непредельных углеводородов и генерируют новые радикалы, что может быть схематически проиллюстрировано на примере полимеризации стирола:
377
Глава 12. Обобщающие разделы курса органической химии
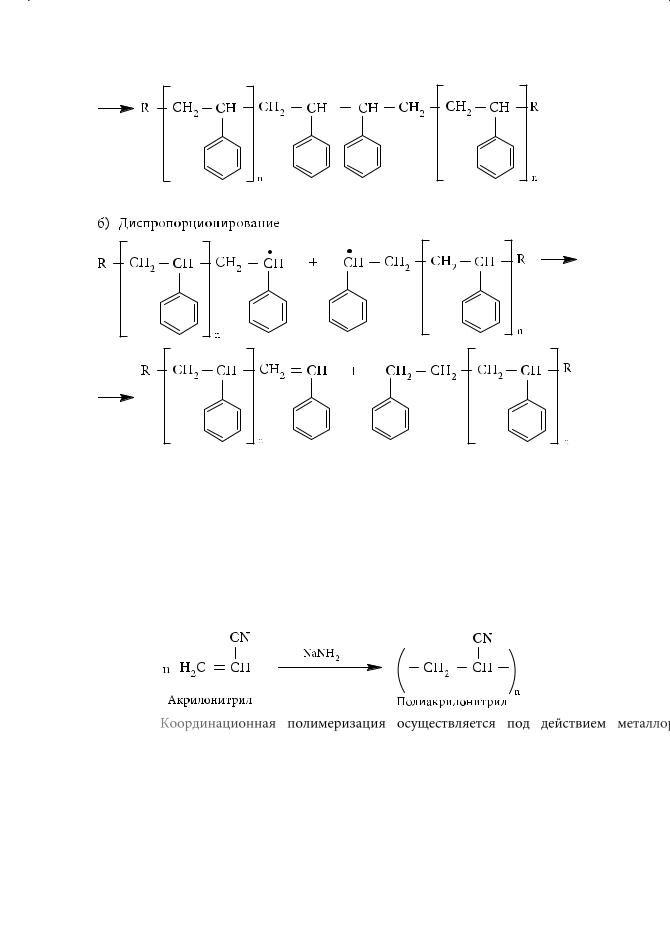
Реакция завершается, когда в реакционной системе не остается свободных радикалов за счет процессов их рекомбинации или действия ингибиторов:
378
57. Полимеры
Радикальная полимеризация этилена проходит в жестких условиях — при температуре 100 °С и высоком давлении (примерно 2000 атм). Получаемый полиэтилен имеет разветвленную структуру.
В анионной полимеризации роль инициаторов выполняют нуклеофильные частицы: амид-ион NH2–, алкоксид-ион RO–, литийорганические соединения. Так, акрилонитрил СН2=СН–CN, получаемый из ацетилена и циановодорода, полимеризуется по анионному типу с образованием акрилонитрила. Инициатором полимеризации является амид натрия:
Координационная полимеризация осуществляется под действием металлорганических катализаторов, например на основе хлорида титана(IV) и триэтилалюминия (катализатор Циглера — Натта; Нобелевская премия 1963 года). Катализатор выполняет роль матрицы, на которой растет полимерная цепь.
379

Глава 12. Обобщающие разделы курса органической химии
ВОПРОСЫ И УПРАЖНЕНИЯ
1.Напишите уравнения реакций полимеризации, лежащих в основе синтеза полистирольных пластмасс и бутадиенстирольного каучука.
2.В каких условиях получают полиэтилен низкого и высокого давления? Как различаются по свойствам образующиеся полимерные продукты?
3.Напишите уравнения реакций полимеризации, в ходе которых можно получить следующие полимеры: а) поливинилхлорид из хлорэтилена; б) тефлон из тетрафторэтилена.
4.Полипропилен занимает промежуточное положение между пластмассами и волокнами: он идет на изготовление волокон для ковров и при этом может быть
использован как пластик, аналогично полиэтилену. Предложите метод синтеза полипропилена с использованием в качестве исходного сырья ацетилена и любых неорганических соединений. Укажите условия соответствующих реакций.
5.Известно, что шерсть и шелк по своему строению похожи на белок: это полимеры, получающиеся в реакции поликонденсации и содержащие амидные (пептидные) связи –CONH. Запишите уравнение реакции поликонденсации, в результате которой образуются полиамидные волокна найлона, используя 1,6-диаминогексан и адипиновую кислоту НООССН2СН2СН2СН2СООН.
6.Какие реакции лежат в основе получения ацетатного волокна и синтеза капрона?
380
