
- •Органическая химия для школьников
- •Оглавление
- •Предисловие
- •Глава 1. Введение в органическую химию
- •§ 1. Теория химического строения органических соединений А. М. Бутлерова
- •§ 2. Классификация органических соединений
- •§ 3. Строение атомов
- •§ 4. Типы и характеристики химической связи
- •§ 5. Первоначальные представления о типах и механизмах органических реакций
- •Глава 2. Алканы
- •§ 6. Изомерия и номенклатура алканов
- •§ 7. Гомологи. Гомологический ряд алканов
- •§ 8. Строение молекул алканов. Физические свойства алканов
- •§ 9. Химические свойства алканов
- •§ 10. Получение и применение алканов
- •§ 11. Алкены: гомологический ряд, номенклатура, изомерия. Строение молекул алкенов
- •§ 12. Физические и химические свойства алкенов
- •§ 13. Получение и применение алкенов
- •§ 14. Циклоалканы: изомерия, номенклатура, физические свойства и получение
- •§ 15. Строение и химические свойства циклоалканов
- •§ 16. Алкины: изомерия и номенклатура. Строение молекулы ацетилена
- •§ 17. Физические и химические свойства алкинов
- •§ 18. Получение и применение алкинов
- •§ 20. Строение и свойства дивинила
- •§ 21. Каучук. Резина
- •§ 23. Электронное и пространственное строение бензола. Изомерия и номенклатура аренов
- •§ 26. Конденсированные ароматические углеводороды
- •§ 27. Природные источники углеводородов. Нефть
- •Глава 5. Галогенопроизводные углеводородов. Спирты. Фенолы
- •§ 28. Галогенопроизводные углеводородов
- •§ 29. Спирты: классификация, изомерия, номенклатура и методы получения
- •§ 30. Физические и химические свойства спиртов. Водородная связь
- •§ 31. Многоатомные спирты
- •§ 32. Фенолы: классификация, особенности строения, физические свойства. Получение и применение фенола
- •§ 33. Химические свойства фенола
- •§ 34. Простые эфиры
- •Глава 6. Карбонильные соединения. Альдегиды и кетоны
- •§ 35. Альдегиды и кетоны: классификация, номенклатура, изомерия и физические свойства
- •§ 36. Получение альдегидов и кетонов. Строение карбонильной группы
- •§ 37. Химические свойства альдегидов и кетонов
- •Глава 7. Карбоновые кислоты
- •§ 40. Строение карбоновых кислот, их физические и химические свойства
- •§ 41. Важнейшие представители карбоновых кислот
- •§ 42. Гидроксикислоты и кетокислоты. Оптическая изомерия
- •§ 43. Сложные эфиры
- •§ 44. Жиры: строение, свойства, применение и роль в природе
- •Глава 8. Углеводы
- •§ 45. Классификация углеводов. Глюкоза
- •§ 46. Химические свойства глюкозы и ее получение
- •§ 47. Дисахариды
- •§ 48. Полисахариды
- •Глава 9. Амины
- •§ 50. Электронное и пространственное строение аминов. Химические свойства аминов
- •Глава 10. Аминокислоты. Белки
- •§ 51. Классификация, изомерия, номенклатура аминокислот
- •§ 53. Белки
- •Глава 11. Гетероциклические соединения. Нуклеиновые кислоты
- •§ 54. Общая характеристика гетероциклических соединений
- •§ 55. Нуклеиновые кислоты
- •Глава 12. Обобщающие разделы курса органической химии
- •§ 56. Теория химического строения органических соединений как основа курса органической химии
- •§ 57. Полимеры
- •Литература

Глава 4. Ароматические углеводороды
3.Галогенирование хлорбензола и фенола идет в орто- и пара-положения. При этом если гидроксильная группа облегчает реакцию электрофильного замещения
в бензольном кольце, то атом галогена, наоборот, затрудняет ее. Почему?
4.Напишите уравнения реакций, при помощи которых из известняка, используемого в качестве исходного сырья, и любых неорганических реагентов можно получить о-бромбензойную кислоту. Дайте названия реакциям и веществам, образовавшимся в результате превращений. Укажите условия реакций.
5.Напишите уравнения реакций, при помощи которых можно из карбида алюминия получить 2,4,6-тринитротолуол. Дайте названия реакциям и веществам, которые образовывались в результате превращений, укажите условия реакций.
6.Предложите метод синтеза п-бромбензойной кислоты с использованием в качестве исходного соединения н-гептана и любых неорганических реагентов.
7.Нитрование толуола проводят с использованием нитрующей смеси и при нагревании до 30 °С. Нитрование мезитилена (1,3,5-триметилбензол) с хорошим выходом
осуществляют мягким нитрующим реагентом ацетилнитратом (CH3COONO2) при температуре –10 °С. Напишите уравнения обсуждаемых реакций и дайте объяснение различия реакционной способности толуола и мезитилена в реакции электрофильного замещения.
§26. КОНДЕНСИРОВАННЫЕ АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
Многоядерные ароматические соединения
К ароматическим углеводородам относятся также соединения, содержащие несколько бензольных колец:
150
§ 26. Конденсированные ароматические углеводороды
Если в молекулах таких соединений есть общая грань (углерод-углеродная связь), они называются конденсированными ароматическими углеводородами.
Начиная с тетрацена, эти углеводороды имеют окраску, меняющуюся с добавлением следующего бензольного кольца (тетрацен — желто-оранжевые кристаллы; пентацен — сине-фиолетовые кристаллы и т. д.). Они характеризуются наличием подвижной системы π-электронов. Тетрацен и пентацен могут быть использованы в качестве органических полупроводников.
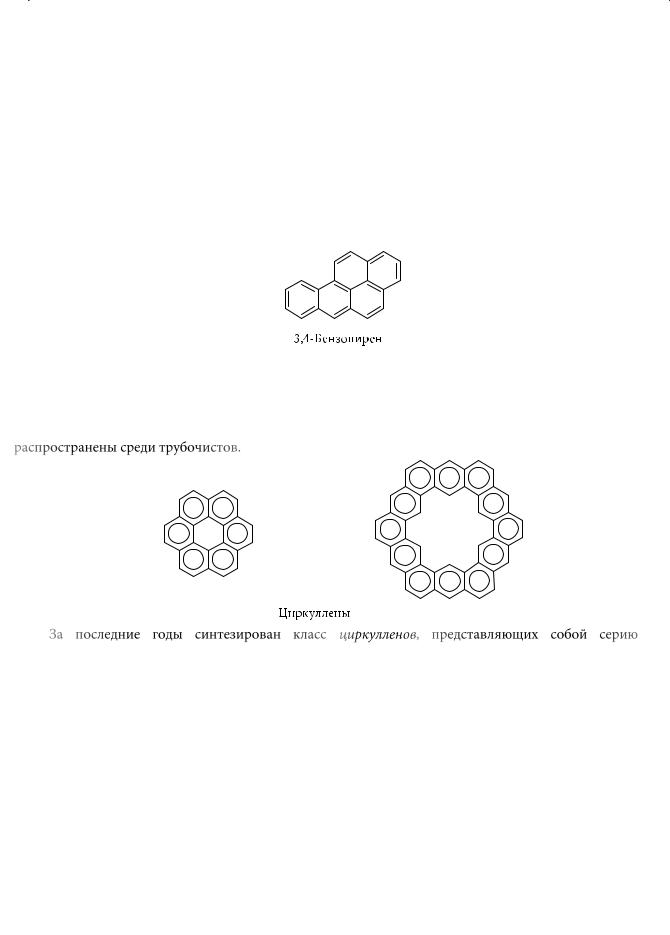
В сланцевой смоле, в каменном угле обнаружен 3,4-бензопирен, являющийся сильным канцерогеном:
Содержание этого крайне опасного химического соединения в указанных природных объектах (например, в саже) достигает 1,5 %. Вот почему заболевания раком кожи были так распространены среди трубочистов.
За последние годы синтезирован класс циркулленов, представляющих собой серию конденсированных бензольных колец, расположенных «ромашкой»:
Важную роль среди конденсированных ароматических соединений играют нафталин и антрацен.
Нафталин
Нафталин — бесцветное кристаллическое вещество, которое плавится при температуре 80 °С и кипит при 218 °С. Он практически не растворяется в воде, но при этом хорошо растворим в большинстве органических растворителей. Основной промышленный метод получения нафталина — выделение его
151
Глава 4. Ароматические углеводороды
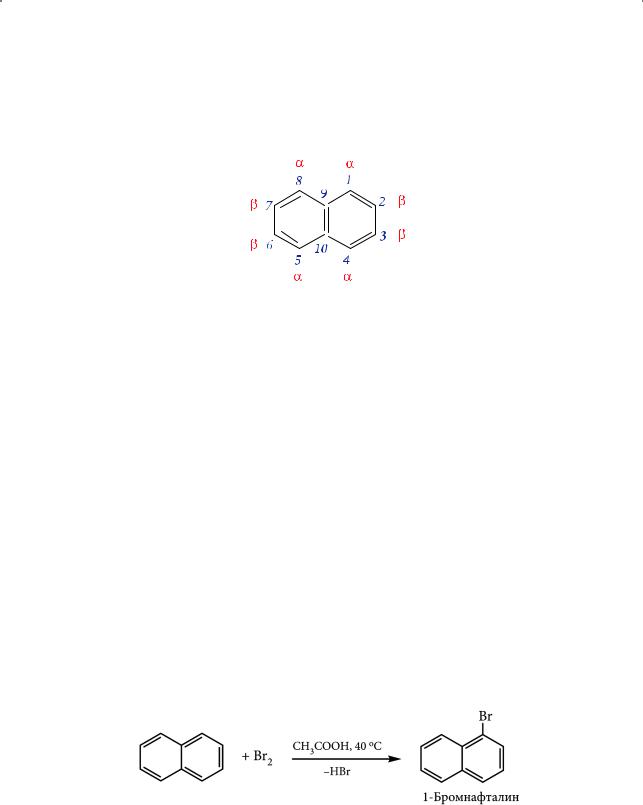
из каменноугольной смолы. Молекула нафталина содержит два бензольных ядра, которые имеют между собой два общих углеродных атома, называемых узловыми (9, 10); при узловых углеродных атомах нафталина отсутствуют водородные атомы:
Атомы углерода 1, 4, 5, 8 обозначают буквой α, а углеродные атомы 2, 3, 6, 7 — буквой β. Длины связей между атомами углерода в нафталине уже несколько различаются. Молекулы нафталина и антрацена имеют меньшую стабильность по сравнению с бензолом. Энергии сопряжения бензола, нафталина и антрацена составляют 151, 255, 351 кДж/моль соответственно. Сопоставив эти значения, видим, что энергия сопряжения конденсированных аренов меньше суммы таких энергий двух (нафталина) или трех (антрацен) бензольных колец. Именно по этой причине для нафталина и других конденсированных ароматических углеводородов реакции электрофильного замещения идут в более мягких условиях. При этом в большинстве случаев замещение в молекуле нафталина осуществляется в α-положение.
Химические свойства
1.Реакции электрофильного замещения
Подобно бензолу, для нафталина как для ароматического углеводорода главными реакциями являются реакции электрофильного замещения: галогенирование, нитрование, алкилирование и ацилирование по Фриделю —Крафтсу, сульфирование. При этом более реакционноспособным оказывается α-положение.
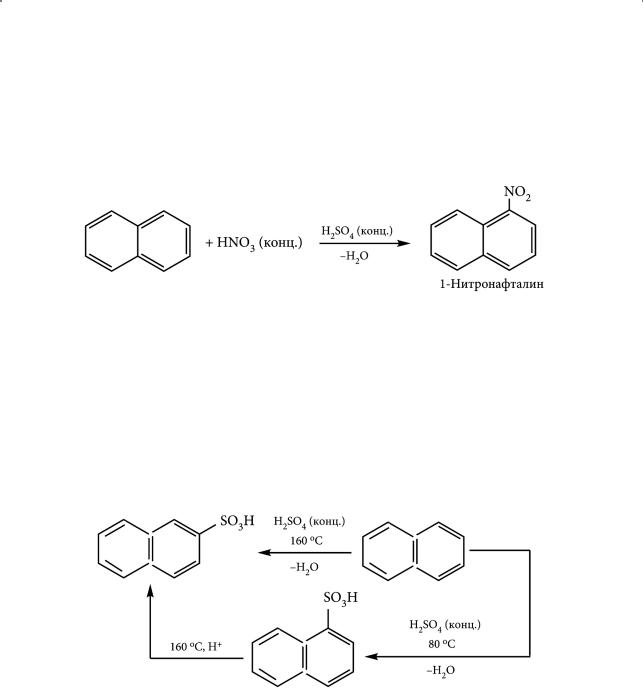
Бромирование нафталина осуществляют бромом в уксусной кислоте при температуре 40 °С. Образуются два монозамещенных продукта — 1-бром- и 2-бромнафталины в соотношении 99 : 1 соответственно:
152
§ 26. Конденсированные ароматические углеводороды
Нитрование, так же как и бромирование, идет в более мягких условиях, чем для бензола: нафталин нитруется либо азотной кислотой в уксусном ангидриде при незначительном нагревании, либо смесью концентрированных азотной и серной кислот (нитрующая смесь) при комнатной температуре. Образуется α-нитронафталин:
Интересной является реакция сульфирования нафталина. Характер образующегося продукта зависит от температуры реакции. Сульфирование концентрированной серной кислотой при 80 °С идет с образованием α-изоме- ра — нафталин-1-сульфоновой кислоты. Повышение температуры реакции до 160–180 °С приводит к соответствующему β-изомеру — нафталин-2-сульфо- новой кислоте. При этом, если нагреть нафталин-1-сульфоновую кислоту до этих же температур, она полностью изомеризуется в β-изомер. Следовательно, последний является более стабильным (термодинамически контролируемый продукт), а нафталин-1-сульфоновая кислота образуется с большей скоростью (кинетически контролируемый продукт):
Таким образом, в отличие от бензола уже введение первого заместителя в молекулу нафталина, в принципе, может привести к получению двух различных монозамещенных производных.
Каковы же правила ориентации в реакциях электрофильного замещения нафталина при введении следующего заместителя?
153
Глава 4. Ароматические углеводороды
Если в одном из колец находится активирующий, донорный заместитель (например, алкил, –ОН, –NH2), то cледующая электрофильная частица будет атаковать это же (активированное) ароматическое кольцо.
Напротив, если с одним из бензольных колец нафталина связан акцепторный, дезактивирующий заместитель (например, –NO2, –COOH, –SO3H), электрофильный агент атакует незамещенное кольцо (т. е. недезактивированное). Замещение также происходит в α-положение.
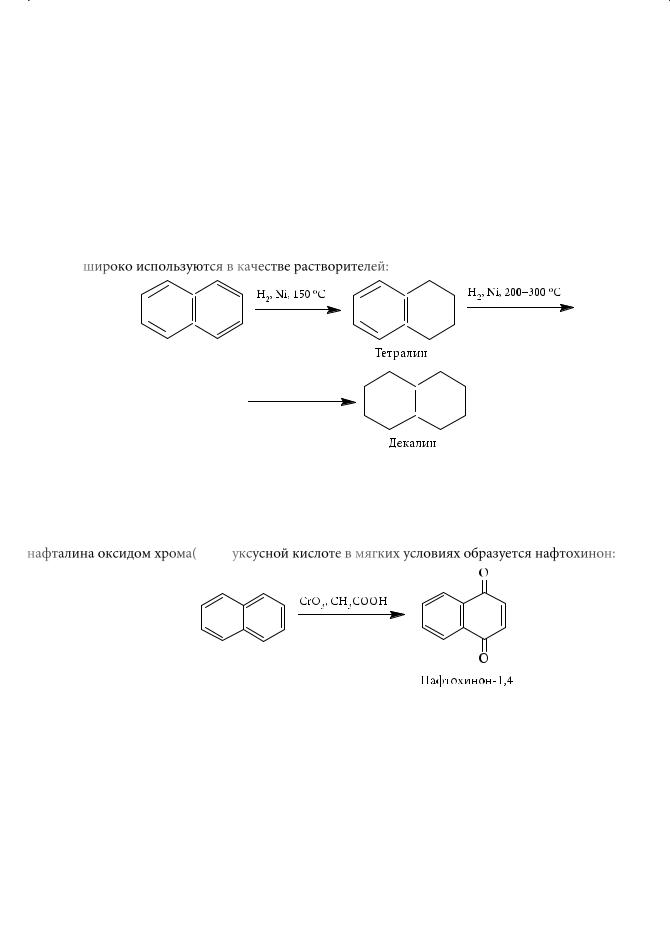
Восстановление нафталина в присутствии катализатора дает тетралин и декалин, которые широко используются в качестве растворителей:
Окисление нафталина происходит значительно легче, чем в случае бензола. При окислении нафталина оксидом хрома(VI) в уксусной кислоте в мягких условиях образуется нафтохинон:
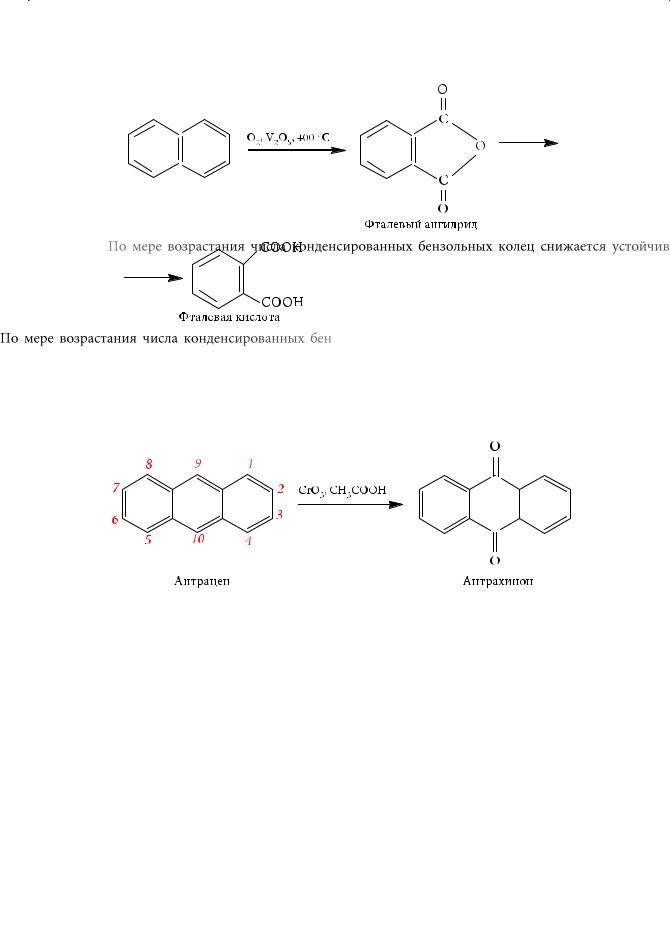
Окисление нафталина в жестких условиях (при высоких температурах, в присутствии катализатора V2O5) приводит к образованию фталевого ангидрида, в результате гидролиза которого получается двухосновная ароматическая фталевая кислота:
154
§ 26. Конденсированные ароматические углеводороды
По мере возрастания числа конденсированных бензольных колец снижается устойчивость этих углеводородов и уменьшается их ароматичность. Ближайший конденсированный линейный аналог нафталина, антрацен, легко окисляется с образованием антрахинона:
Соединения нафталина и антрацена нашли применение в производстве красителей.
ВОПРОСЫ И ЗАДАНИЯ
1.Почему реакции электрофильного замещения, окисления и присоединения в конденсированных аренах осуществляются в более мягких условиях, чем для бензола?
2.Напишите уравнения реакций, с помощью которых можно осуществить следующую цепочку превращений: оксид кальция → карбид кальция → ацетилен → бензол → изопропилбензол → бензойная кислота. Укажите условия проведения соответствующих реакций.
155
