
Методы выделения очистки и идентификации органических веществ
..pdfМинистерство образования и науки Российской Федерации
Федеральное государственное бюджетное образовательное учреждение высшего образования Пермский национальный исследовательский политехнический университет
С.Е. Уханов
МЕТОДЫ ВЫДЕЛЕНИЯ, ОЧИСТКИ И ИДЕНТИФИКАЦИИ ОРГАНИЧЕСКИХ ВЕЩЕСТВ
Утверждено Редакционно-издательским советом университета
в качестве учебно-методического пособия
Издательство Пермского национального исследовательского
политехнического университета
2016
1
УДК 547:54.05+66.048](075.8) У89
Рецензент канд. хим. наук, доцент Е.С. Денисламова
(Пермский национальный исследовательский политехнический университет)
Уханов, С.Е.
У89 Методы выделения, очистки и идентификации органических веществ : учеб.-метод. пособие / С.Е. Уханов. – Пермь: Изд-во Перм. нац. исслед. политехн. ун-та, 2016. – 48 c.
Даны общие теоретические сведения о методах выделения очистки и идентификации органических веществ, а также для закрепления материала предложены две лабораторные работы по органической химии по теме «Методы выделения, очистки и идентификации органических веществ».
Предназначено для студентов, обучающихся по направлению 240100.62 «Химическая технология» по профилю подготовки бакалавров 08. «Химическая технология природных энергоносителей и углеродных материалов».
УДК 547:54.05+66.048](075.8)
ISBN 978-5-398-01594-2 |
ПНИПУ, 2016 |
2
1.ВЫДЕЛЕНИЕ И ОЧИСТКА ОРГАНИЧЕСКИХ ВЕЩЕСТВ
Вреакциях между органическими веществами почти никогда не образуются чистые индивидуальные соединения, наряду с нужным веществом обычно всегда присутствует некоторое количество неизменного исходного продукта. Кроме того, получаются также побочные и промежуточные продукты, окрашенные примеси, смолистые загрязнения и т.д. Вследствие этого одной из важнейших задач препаративной органической химии является выделение вещества из смеси и получение его в химически чистом, пригодном для анализа и дальнейшего использования виде. Соответственно и операции, связанные с этой задачей, проводят обычно в две стадии: выделяют полученный продукт из реакционной смеси и затем проводят его очистку.
1.1. Выделение и препаративное разделение органических веществ
Под выделением вещества понимают его извлечение из реакционной смеси в индивидуальном состоянии в виде, пригодном для дальнейшей очистки и идентификации. Такая операция целесообразна тогда, когда необходимо получить лишь целевой продукт синтеза, а остальные компоненты реакционной смеси (побочные продукты, непрореагировавшие исходные вещества, катализаторы и т.д.) не представляют интереса и не подлежат выделению. Тем не менее в лабораторной практике нередки случаи, когда из сложной смеси необходимо выделить и идентифицировать все составляющие ее компоненты (например, при изучении механизмов химических реакций, исследовании природных и биологических объектов, с целью утилизации побочных веществ и т.д.). Такую операцию называют разделением органических веществ. Разделение применяют и тогда, когда реакционная смесь очень сложна по составу и непосредственное выделение целевого продукта не представляется возможным.
3
В этом случае реакционную смесь сначала разделяют на относительно простые части (фракции, классы соединений, гомологические ряды) и из основной части выделяют целевой продукт.
Разделение органических веществ проводят двумя различными методами, основанными на химических и физических свойствах соединений. При помощи первого метода обычно удается достичь быстрого и полного разделения, и его следует использовать, когда это только возможно. Второй метод применяется главным образом для разделения химически однородных веществ, например, различных членоводного гомологического ряда.
1.1.1. Разделение, основанное на различии химических свойств
При разделении этим методом одно из подлежащих выделению веществ в форме соли, производного или продукта присоединения переводят в водный раствор или в нерастворимую в органических растворителях форму, а затем выделяют путем перегонки с водяным паром, экстракции и т.д. Например, не растворимые в воде органические кислоты при обработке щелочью превращаются в водорастворимые калиевые или натриевые соли и переходят в водный слой, в то время как примеси (углеводороды, их нитро- и галогенопроизводные, спирты, альдегиды, кетоны и т.д.) остаются в органическом слое. После разделения слоев водный слой подкисляют соляной или другой минеральной кислотой, при этом органическая кислота выделяется в свободном виде и может быть экстрагирована, например, эфиром.
Данный метод имеет два ограничения. Во-первых, необходимо знать строение и химические свойства выделяемого соединения. Во-вторых, это соединение должно отличаться по химическим свойствам от других компонентов смеси, состав и свойства которых также должны быть известны. Так, в рассмотренном примере выделение в чистом виде карбоновой кислоты будет возможно, если в реакционной смеси не было других кислот. В противном случае все карбоксильные соединения дадут при обработке щелочью водорастворимые соли и перей-
4
дут в водный слой. Мы достигнем разделения класса карбоновых кислот от других классов органических соединений, но для выделения интересующей нас кислоты потребуются дополнительные операции, например перегонка.
1.1.2. Разделение, основанное на различии физических свойств
Агрегатное состояние. Отделение газов от твердых веществ и жидкостей не представляет труда, поскольку происходит самопроизвольно. Разделение твердых и жидких веществ осуществляют путем декантации, фильтрования, отсасывания, центрифугирования и т.д.
Температура кипения. По температуре кипения разделяют жидкие, а иногда и твердые вещества. В основе метода лежат различные виды перегонки, т. е. испарение вещества при температуре его кипения с последующей конденсацией паров и отбором соответствующих фракций дистиллята.
Растворимость. Различная растворимость используется для разделения как твердых, так и жидких веществ путем экстракции, причем одна из составных частей смеси должна быть трудно растворима в растворителе и таким путем может быть выделена, или же подлежащие разделению вещества по-разному распределяются между двумя не смешивающимися между собой растворителями. Твердые вещества разделяют путем дробной кристаллизации, причем растворяют все составные части реакционной смеси и выкристаллизовывают наиболее трудно растворимую из них.
Адсорбционная способность. Методы разделения по ад-
сорбционной способности относятся к хроматографическим методам. Несмотря на разнообразие аппаратурного оформления и техники исполнения, все они основаны на различной способности разных веществ удерживаться на поверхности того или иного адсорбента. Хроматография широко применяется для разделения жидких, твердых и газообразных веществ. Правильным подбором адсорбента и параметров хроматографического про-
5
цесса можно добиться качественного разделения даже очень близких по строению и свойствам соединений.
В заключение отметим, что в лабораторной практике зачастую не делают различий между разделением и выделением органических веществ. Действительно, если реакционная смесь достаточно проста, то операции разделения и выделения совпадают как по методам исполнения, так и по достигаемому результату. В простейшем случае, когда в смеси находятся только два вещества, выделение любого из них автоматически означает и разделение данной смеси.
1.2. Очистка сырых продуктов
Продукт после выделения в виде индивидуального химического соединения необходимо подвергнуть очистке и привести
впригодное для анализа состояние. В зависимости от агрегатного состояния полученного вещества применяют различные способы очистки.
Жидкие вещества. Очистка их производится главным образом путем перегонки, причем нестойкие соединения перегоняют
ввакууме. В ряде случаев для этой цели применяют хроматографию.
Твердые вещества. Их очистка производится обычно путем перекристаллизации или, если возможно, возгонки (сублимации). В некоторых случаях применяют также и хроматографию.
Ниже будут рассмотрены различные способы выделения и очистки жидких и твердых органических веществ, поскольку работа с газообразными продуктами встречается в лабораторной практике сравнительно редко, и, кроме того, выделение и очистка газов представляют значительно более простую проблему.
Применяемые в лаборатории способы можно разделить на те, при которых работа ведется без растворителя (возгонка и перегонка), и на способы, при которых применяется растворитель (экстракция, перекристаллизация, хроматография, диализ). Уже отсюда становится ясной та роль, которую играют растворители при работе с органическими веществами.
6
2. ПЕРЕГОНКА |
|
Под перегонкой подразумеваются переведение |
вещества |
в парообразное состояние путем нагревания его до |
кипения |
иобратное превращение при охлаждении в жидкое состояние: (твердый) → жидкий → газообразный → жидкий → (твердый), причем при этой операции очень большое значение имеют отведение и конденсация паров и сбор дистиллята.
При перегонке нужно различать два случая; в одном из них интересен бывает дистиллят (перегонка, в более точном смысле этого слова), в другом нужен остаток после перегонки (отгонка растворителя или упаривание).
Перегонку в точном смысле этого слова применяют или с целью очистки какого-либо отдельного вещества, или же для разделения путем дробной перегонки смеси веществ. Ниже будут рассмотрены сначала перегонка при атмосферном давлении
ив вакууме, затем упаривание и, наконец, особый вид перегонки – перегонка с паром.
2.1. Перегонка при атмосферном давлении
Для сборки различных химических установок и приборов
игерметического закрывания посуды применяют резиновые пробки и различные шлифы.
Шлиф – это разъёмное соединение, использующееся в стеклянной лабораторной посуде. Шлиф состоит из притёртых друг к другу конических керна и муфты. В настоящее время довольно широко распространена химическая стеклянная посуда, в том числе и приборы для перегонки с так называемыми нормальными шлифами строго определенных размеров. Это позволяет обходиться совсем без резиновых или корковых пробок и быстро собирать сложные аппараты из взаимозаменяемых частей, поскольку шлифы одного и того же размера взаимно заменяют друг друга
иобеспечивают герметичность прибора.
7

Сосуды для перегонки. При перегонке большинства веществ применяют обычно колбы Вюрца – круглодонные термостойкие колбы, к горлышку которых припаяна в наклонном положении трубка, соединяющая колбу с холодильником. Термометр вставляют в отверстие колбы с помощью резиновой пробки.
Насадки для перегонки (насадки Вюрца) используются совместно с колбами на шлифах, у которых боковой отвод отсутствует. Они представляют собой широкие трубки с боковым отростком, конец которого имеет шлиф для соединения с холодильником. В верхний шлиф насадки вставляют термометр, нижний шлиф служит для соединения со шлифованным горлом колбы.
Дефлегматоры служат для разделения смеси веществ путем дробной перегонки. Принцип действия дефлегматоров основан на удлинении пути, который проходят пары из колбы до холодильника, причем на пути паровой фазы по дефлегматору устроены конденсационные системы. Благодаря им вышекипящие (а потому и легче конденсирующиеся) компоненты жидкости конденсируются уже в дефлегматоре и стекают обратно в колбу, а нижекипящие составные части смеси выходят из дефлегматора в парообразном состоянии и конденсируются уже олодильнике. Имеется большое число различных конструкций дефлегматоров. Самый простой из них представляет собой удлиненную насадку для перегонки, которая имеет ряд шарообразных утолщений (так называемый дефлегматор Вюрца, или шариковый дефлегматор). Образцы посуды для перегонкипоказаны нарис. 1.
1 2 3
Рис. 1. Посуда, применяемая при перегонке: 1 – колба Вюрца; 2 – насадка Вюрца; 3 – шариковый дефлегматор
8
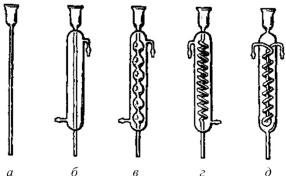
Холодильники (рис. 2) служат для охлаждения перегоняющихся паров и конденсации их в жидкость. Для перегонки применяют прямые нисходящие холодильники (холодильники Либиха) с водяным или воздушным охлаждением.
Рис. 2. Холодильники: а – воздушный; б – Либиха; в – шариковый; г – змеевиковый; д – Димрота
При перегонке веществ, кипящих приблизительно до 130 °С, применяют либиховские или змеевиковые холодильники, через рубашку которых пропускают холодную воду. При перегонке очень летучих соединений (например, ацетальдегида, ТКИП = 21 °С) либиховский холодильник рекомендуется соединять со змеевиковым холодильником и, кроме того, охлаждать приемник льдом или снегом. При перегонке веществ с температурой кипения выше 130 °С охлаждения водой не применяют, в этом случае используются воздушныехолодильники.
Приемники. В качестве приемников для дистиллята применяют колбы или пробирки. При перегонке твердых веществ приемники непосредственно подставляют к отводу колбы для перегонки, так как в этом случае не применяют никаких особых мер для охлаждения дистиллята. При дробной перегонке твердых веществ удобнее всего собирать отдельные фракции в фарфоровые чашки, из которых перегнанное вещество извлекают путем расплавления.
9
2.1.1. Подготовка жидкости к перегонке
Перед перегонкой обычно необходимо осушить вещество, т.е. полностью удалить из жидкости воду, так как в ее присутствии при перегонке происходят неприятные толчки (особенно при перегонке в вакууме). Следует также исключить возможность гидролиза некоторых веществ при их нагревании с водой в ходе перегонки. Сушку ведут при помощи осушающих веществ, которые обычно прибавляют к разбавленной растворителем жидкости. При выборе подходящего средства для сушки необходимо руководствоваться его химической индифферентностью по отношению к осушаемому веществу. Осушитель не следует брать в избытке, лучше оставить смесь стоять на более продолжительное время. К наиболее важным осушающим средствам можно отнести:
Хлористый кальций (сплавленный или гранулированный) – наиболее доступное и широко распространенное средство. Хлористый кальций обладает достаточно высокой осушающей способностью, но его нельзя применять для высушивания спиртов
иаминов, с которыми он образует продукты присоединения. Продукты присоединения с ним способны давать также некоторые кетоны и сложные эфиры (например, ацетон, диэтиловый эфир янтарной кислоты).
Безводные соли серной кислоты (сульфаты натрия, магния
имеди) в химическом отношении почти вполне индифферентны, а потому очень удобны для сушки нестойких соединений: альдегидов, кетонов, спиртов, эфиров и т.д. Действуют они, однако, довольно медленно, поэтому процесс сушки занимает обычно несколько дней.
Едкие щелочи (КОН и NaОН) применяют для сушки органических оснований типа алифатических аминов, пиридина и их производных.
Углекислый калий (поташ) используют для высушивания спиртов, кетонов и легко окисляющихся органических оснований, которые не рекомендуется сушить едким кали.
10
