
Органические соединения. Часть 2. Кислородсодержащие и высокомолекуля
.pdf
2KOH |
|
H O |
HCN |
|
2H2O |
5. СH2Br–CH2 Br спирт. р-р |
A |
2 |
Б KCN |
В |
Г |
H+, Hg+2 |
|||||
6. |
|
|
|
|
|
7. |
|
|
|
|
|
8.
9.
10.
11.
31

12.
13.
14.
15.
16. С3H6O2  С3H5O2Cl
С3H5O2Cl  С3H6O3
С3H6O3  С3H4O2
С3H4O2  С3H6O3
С3H6O3
17. С6H5CH(CH3)2 KMnO4 +H2 SO4 А HNO3 |
Б Fe + HCl |
В NaOH (изб.) Г |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
H 2SO4 |
|
|
|
|
|
|
|
|
|
|
|
|
Br 2 |
|
|
|
NaOH |
|
|
|
H |
O |
|
|
H |
2 |
|
|||||
18. СH3CH=CH2 |
|
А |
|
р-р |
Б |
+ |
2 |
|
+2 |
В |
|
Г |
|||||||||
|
|
CCl4 |
|
|
спирт. |
|
H |
, Hg |
|
Ni, t° |
|
||||||||||
KMnO +H |
|
SO |
|
|
|
HNO |
|
|
C 2H5OH |
|
Fe + HCl |
|
|||||||||
19.С6 H5 CH3 |
4 |
|
2 |
|
4 |
А |
|
H |
SO3 Б |
|
|
H+ |
|
В |
|
|
Г |
||||
|
|
|
|
|
|
|
|
|
2 |
4 |
|
|
|
|
|
|
|
|
|
|
|
20. Пропанол-2 |
HClt° (г) |
|
А AlClC6H6 |
Б KMnO4 + H2 SO4 |
В пропанолH+ -2 Г |
||||||||||||||||
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
21. СH3 COOH |
|
Cl2 |
|
|
А |
2NH3 |
|
Б |
|
H2SO 4 |
|
В |
C2H5OH |
Г |
|||||||
|
P(кр) |
|
|
|
|
|
|
|
|
|
|
|
H+ |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
32

|
С3 H4 |
H2O |
А |
H2 |
Б |
|
HCl(г) |
В |
C6 H5 CH3 |
Г |
|
22. |
|
|
|
||||||||
H+, Hg +2 |
Ni; t° |
|
H+ |
AlCl3 |
|||||||
|
|
|
|
|
|
|
|||||
|
|
|
KMnO4 + H2SO4 |
А |
Cl2 |
2NH3 |
В |
C2H5OH |
|||
23. СH3–CH=CH–CH3 |
|
|
Б |
|
+ |
Г |
|||||
|
|
|
|
|
|
|
P(кр) |
|
|
H |
|
24.СH3CHO  С2H6O
С2H6O 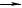 С4 H6
С4 H6  С4H6B2
С4H6B2  С4 H8O2
С4 H8O2
25.С7H6Cl2  С7H6O
С7H6O  С7H9NO2
С7H9NO2  С7H6O2
С7H6O2  С7H5NO4
С7H5NO4
26. СH3–CHCl–CH3
1
27.СH 3 COONa
4
1
28.СH3COONa
4
KOH |
A |
|
Б |
Cl2 |
В |
KOH |
Г |
H O |
|
H2 SO4, t° |
|
ССl4 |
|
спирт. р-р |
|
2 |
|
|
|
|
|
|
|
C 2 H5 OH
3
2
5  СH 3 COOH
СH 3 COOH
6
СH 3 COOC2H5
CH3 COOH |
3 |
|
|
|
|
2 |
5 |
(СH3 COO)2Ca |
|
||
|
|
|
|
6 |
|
СH3COOCH3 |
|
|
33

|
|
C n H2nO2 |
|
3 |
|
1 |
|
|
|
|
С2n H4n O2 |
2 |
5 |
Сn H2n–1KO2 |
29. |
|
|||
|
|
|||
|
4 |
|
|
6 |
|
|
|
|
|
|
|
Сn H2n+2 O |
|
|
|
|
C2n H4n–2O3 |
|
|
|
1 |
|
|
3 |
|
|
2 |
5 |
С2n H4n O2 |
30. |
Сn H2n O2 |
|
||
|
|
|||
|
4 |
|
|
6 |
|
|
|
|
|
Сn H2n–1OCl
Пример 1. Осуществите следующие превращения:
Назовите полученные соединения.
Ответ:
1) С2H6 + Cl2 h ν CH3–CH2Cl + HCl
|
хлорэтан |
2) СH3 –CH2 Cl + Mg |
CH3 –CH2 –MgCl |
|
эфир |
|
хлоридэтилмагний |
34

|
|
|
|
O |
|
|
|
|
3) CH3 –CH2 |
–MgCl + H С + HCl |
|
|
|
||||
|
|
|
|
H |
|
|
|
|
CH3–CH2–CH2–OH + MgCl2 |
|
|
|
|||||
|
|
пропанол-1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
4) CH3–CH2–CH2–OH + CuO t° |
CH3–CH2 С |
+ Cu + H2O |
||||||
|
|
|
|
|
пропаналь |
|
H |
|
|
|
|
O |
|
|
|
|
|
5) CH3–CH2 |
С |
+ 2[Ag(NH3 )2 ]OH |
|
|
||||
|
|
|
H |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
CH 3–СH2 |
С |
|
+ 2Ag + 3NH3 + H2O |
|||||
|
|
|
ONH4 |
|
|
|
|
|
|
|
|
пропаноат аммония |
|
|
|
|
|
|
|
|
O |
|
|
|
|
O |
6) CH3–CH2 |
С |
+ HCl |
CH3 –CH2 |
С |
+ NH4 Cl |
|||
|
|
|
ONH4 |
|
|
|
|
OH |
|
|
|
|
|
пропановая кислота |
|||
|
|
O |
|
|
Cl |
|
O |
|
7) CH –СН |
2 |
С |
+ Cl2 |
P(кр) |
CH |
–CH |
С |
+ HCl |
3 |
|
OH |
3 |
|
|
OH |
||
|
|
|
|
|
|
|
||
2-хлорпропановая кислота
35

Cl |
O |
|
O |
8) CН3CH С |
+NH 3 + H2 O CH |
3–CH С |
+ NH4 Cl |
|
OH |
OH |
ONH4 |
|
|
|
2-гидроксипропаноат аммония
Пример 2. Напишите уравнения реакций, соответствующих следующей схеме:
Ответ
В этой задаче два необычных момента. Во-первых, отсутствуют стрелки в схеме, и направления реакций можно выбирать самостоятельно. Во-вторых, в схеме даны не конкретные вещества, а гомологические ряды; это усложняет задачу, поскольку для ее решения нужно хорошо представлять взаимосвязь разных классов органических соединений.
Попробуем расшифровать гомологические ряды. CnH2n–6 и CnH2n–8 – это, вероятнее всего, ароматический углеводород и его производное с двойной связью в боковой цепи. Вещества состава Cn–1H2n-10O2 содержат два атома кислорода, которые могут входить в состав карбоксильной группы COOH. Если из Cn–1H2n–10O2 вычесть COOH, то получится Сn–2H2n–11, что соответствует ароматическому радикалу (CmH2m–7 при m = n – 2). Таким образом, Cn–1H2n–10O2 – ароматическая кислота, что подтверждается также образованием калиевого производного Cn–1H2n–11KO2. Для опреде-
36

ления конкретного значения n надо заметить, что при переходе от
СnH2n–6 к Сn–1H2n–10O2 число атомов углерода уменьшается на единицу. Это означает, что один атом углерода из боковой цепи окис-
ляется до CO2. Это возможно только в том случае, если n = 8,
а СnH2n–6 – этилбензол (C6H5CH2CH3). Тогда СnH2n–8 – стирол
(C6H5CH=CH2); Сn–1H2n–10O2 – бензойная кислота (С6H5COOH); Cn–1H2n–11KO2 – бензоат калия (C6H5COOK).
1)
2)
3)
37

4)
5)
6)
Задание № 3
1.Как из карбида кальция и воды получить винилацетат, применив реакцию Кучерова? Напишите уравнение реакции. Составьте схему полимеризации винилацетата.
2.Какие полимеры называются термопластичными? Приведите примеры.
3.Что такое полимеры? Какими способами получают полимеры? Составьте схему поликонденсации анилина с формальдегидом.
4.Полимером какого непредельного углеводорода является натуральный каучук? Напишите структурную формулу этого углеводорода. Как называют процесс превращения каучука в резину?
38
5.Составьте схему поликонденсации фенола и формальдегида
сполучением линейного полимера (новолака). Охарактеризуйте физические и химические свойства новолака.
6.Составьте схему полимеризации метилметакрилата. Приведите механизм радикальной полимеризации в присутствии перекиси бензоата.
7.Составьте схему поликонденсации фенола и формальдегида
сполучением полимера резольного типа. Охарактеризуйте физические и химические свойства резита и резола.
8.Напишите схему сополимеризации бутадиена со стиролом. Разберите его механизм.
9.Составьте схему полимеризации пропена. Разберите механизм радикальной полимеризации в присутствии перекиси водорода.
10.Какие вещества можно использовать в качестве мономеров в цепной полимеризации? Составьте схему полимеризации этена.
11.Какие свойства и области применения имеют фенолформальдегидные, мочевиноформальдегидные и глифталевые смолы? Составьте схему поликонденсации глицерина и фталевой кислоты.
12.Составьте схему полимеризации бутадиена в присутствии металлического натрия. Разберите механизм анионной полимеризации.
13.Какова схема полимеризации синтетического изопренового каучука?
14. Приведите примеры натуральных, модифицированных и синтетических высокомолекулярных соединений. Охарактеризуйте физические и химические свойства соединений.
15. В чем состоит процесс поликонденсации? Что общего и какие отличия у процессов полимеризации и поликонденсации? Приведите примеры.
16.Составьте схему поликонденсации крезола с мочевиной. Какие вещества можно использовать в качестве мономеров в реакции поликонденсации?
17.Составьте схему полимеризации изобутена по катионному механизму в присутствии тетрахлорида титана.
39
18.Составьте схему полимеризации стирола. Разберите механизм катионной полимеризации в присутствии BF3.
19.Составьте схему полимеризации тетрафторэтилена. Какие вещества можно использовать в качестве мономеров в реакции полимеризации?
20.В чем состоит процесс сополимеризации? Составьте уравнение реакции сополимеризации этилена и стирола.
21.Какие полимеры называют стереорегулярными? Дайте оценку их свойств. Приведите примеры.
22.В чем заключается сущность процесса вулканизации каучука? Изобразите структуру вулканизированного изопренового каучука.
23.В чем состоит процесс поликонденсации? Составьте схему поликонденсации фталевой кислоты и этиленгликоля.
24.Какие вещества называются полимерами? Составьте уравнение реакции получения лавсана. Охарактеризуйте физические
ихимические свойства соединения.
25.Как происходит инициирование реакции полимеризации с помощью перекисных соединений? Приведите примеры.
26.Какие полимеры называют элементорганическими, кремнийорганическими соединениями? Приведите примеры и укажите важнейшие свойства кремнийорганических полимеров.
27.Какие полимеры относят к природным, искусственным
исинтетическим? Приведите примеры и охарактеризуйте физические и химические свойства этих соединений.
28.Какие пластмассы называют термореактивными? Каковы методы переработки термореактивных пластмасс в изделия?
29.Приведите примеры полимеров, получаемых методом поликонденсации и полимеризации.
30.Какие вещества называются высокомолекулярными? Что такое макромолекула? Составьте уравнение реакции получения поликарбонатов.
40
