
Полезные материалы за все 6 курсов / Учебники, методички, pdf / Диспансерное_наблюдение_детей_с_аллергическими_и_иммунными_заболеваниями
.pdf
Диспансерное наблюдение детей с аллергическими и иммунными заболеваниями
Актуальность проблемы - увеличение бремени аллергии
>По данным Всемирной аллергологической организации, до 50% населения планеты страдают проявлениями аллергии.
>На сегодняшний день аллергия представляет собой огромную проблему для здравоохранения, приобретая масштабы пандемии и затрагивая более 150 млн человек в одной только Европе, что в значительной степени влияет не только на бюджет здравоохранения, но и на макроэкономику государств.
>В настоящее время в мире около 0,5 млрд людей страдают аллергическим ринитом и приблизительно 380 млн — бронхиальной астмой, среди них 14% дети.
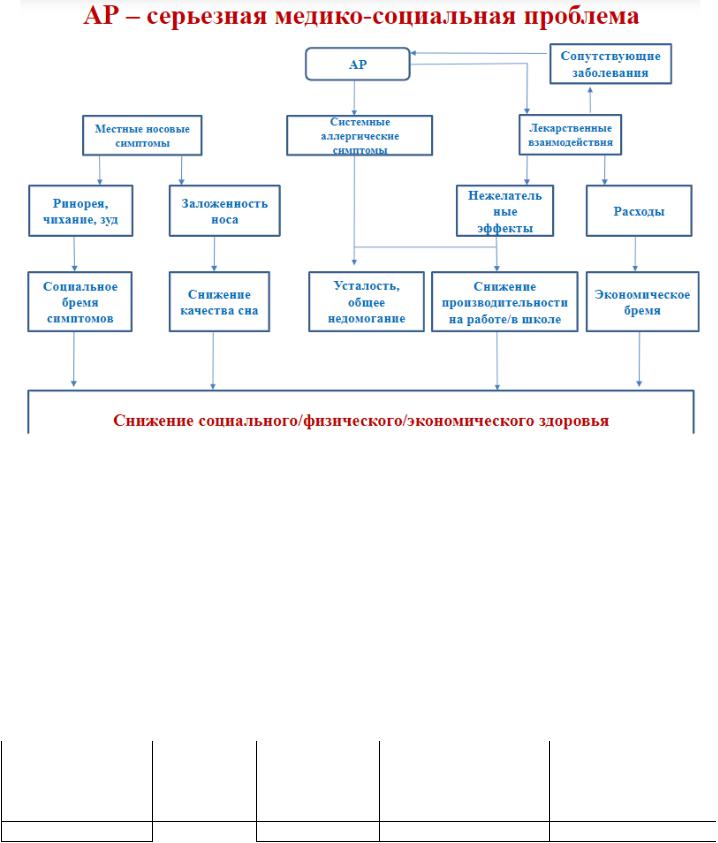
>Аллергические болезни, широко распространенные среди детей и подростков, отрицательно влияют на их физическое и психологическое состояние, социальную жизнь, школьную успеваемость, снижают качество жизни как самих пациентов, так и членов их семей.
Актуальность проблемы - увеличение бремени аллергии
>Сегодня АЛЛЕРГИЧЕСКИЕ ЗАБОЛЕВАНИЯ - НАИБОЛЕЕ РАСПРОСТРАНЕННЫЕ ХРОНИЧЕСКИЕ ЗАБОЛЕВАНИЯ в европейских странах, которыми страдают более 150 млн. человек.
>По прогнозам Европейской академии аллергии и клинической иммунологии (European Academy of Allergy and Clinical Immunology, EAACI), к 2025-2030 г. ожидается, что более половины населения Европы будут страдать оттого или иного вида аллергии
Результаты европейских исследований показывают что
•15% - кожными формами аллергии,
•20% - бронхиальной астмой (70 млн. европейцев), -------------
•до 30% популяции страдают аллергическим ринитом^1 100 млн. европейцев
>Пик заболеваемости приходится на самые продуктивные годы жизни, так
>АР болеют 45% населения Европы в возрасте 20-40 лет, дебют которого регистрируется с периода детства
В 2020 году вышли Практические рекомендации для педиатров, в которых освещены вопросы этиопатогенеза, диагностики, лечения и профилактики аллергических болезней у детей.
Под ред. Намазовой-Барановой В развитии любой аллергической реакции условно выделяются три стадии:
I. Иммунологическая стадия начинается с момента первого контакта организма с аллергеном н заключается в образовании и накоплении антител или сенсибилизированных лимфоцитов. При повторном попадании в организм происходит соединение аллергена с антителами или сенсибилизированными лимфоцитами, что и обусловливает следующую стадию аллергической реакции.
II. Патохимическая стадия заключается в образовании и выделении биологически активных веществ — медиаторов аллергии — в ответ на действие аллергена.
III. Патофизиологическая стадия — стадия клинических проявлений — заключается в повреждающем действии медиаторов аллергии, образовавшихся на предыдущей стадии и обладающих высокой биологической активностью, на ткани организма с развитием клинических симптомов аллергических болезней (зуд, гиперемия, отек, кожные высыпания, удушье и др.).
Патогенетические механизмы, лежащие в основе развития аллергических болезней
Тип гипер- |
Иммунологические |
Патохимические |
Клинические |
Период |
чувстви- |
реакции |
изменения |
проявления |
развития |
тельности |
|
|
|
|
1 |
Анафилактический |
Дегрануляция |
Крапивница, отек, |
1-6 ч после |
|
lgE-зависимый |
тучных клеток и |
бронхоспазм, |
воздействия |
|
|
базофилов |
анафилактический шок |
аллергена |
|
|
|
и другие аллергические |
|
|
|
|
болезни |
|
II |
Цитотоксический IgGl. |
Комплементзавис |
Лекарственная аллергия |
5-15 дней от |
|
3/lgM и комплемент |
имый цитолиз |
(агранулоцитоз) |
начала приема |

|
|
|
|
лекарствен, |
|
|
|
|
препарата |
III |
Иммунокомплексный |
Отложение |
Сывороточная болезнь |
На 1-21-й день |
|
IgG/IgM и комплемент |
иммунных |
|
от начала |
|
или FcR |
комплексов |
|
приема |
|
|
|
|
лекарствен, |
|
|
|
|
препарата |
IVa |
Гиперчувствительность |
Моноцитарное |
Контактный дерматит, |
На 1-21-й день |
|
замедленного типа (Т- |
воспаление |
лекарственная аллергия, |
после |
|
зависимая активация) |
|
экзема, буллезная |
воздействия |
|
Th1-моноциты- |
|
экзантема |
аллергена |
|
макрофаги- |
|
|
|
|
ИФНу/ФНОα |
|
|
|
IVb |
Гиперчувствительность |
Эозинофильное |
Макулопапулезная |
От 1 до |
|
замедленного типа Th2 |
воспаление |
экзантема |
нескольких |
|
- IL4, IL5, IL13, |
|
|
дней после |
|
эотаксин |
|
|
воздействия |
|
|
|
|
аллергена |
IVc |
Цитотоксические |
Гибель |
Макулопапулезная |
На 1-2-е сут |
|
лимфоцитарные |
кератиноцитов, |
экзантема. |
воздействия |
|
(перфорины, |
вызванная |
Пустулярная экзантема. |
аллергена. |
|
гранзимы) |
цитотоксичными |
Синдром Стивенса- |
На 4-28-е сут |
|
|
Т лимфоцитами |
Джонсона/Токсический |
после |
|
|
или Th |
эпидермальный |
воздействия |
|
|
|
некролиз |
аллергена |
IVd |
Т-лимфоцитарные |
Нейтрофильное |
Острый |
Типично на 1-2- |
|
|
воспаление |
генерализованный |
е сут после |
|
|
|
экзантематозный |
воздействия |
|
|
|
пустулез |
аллергена (но |
|
|
|
|
может быть |
|
|
|
|
позже) |
Виды аллергических реакций Немедленного типа (гуморального) ГНТ Замедленного типа (клеточного) ГЗТ
I.Анафилактические и атопические
II. Цитотоксические
III. Иммунокомплексная патология
IV. Клеточноопосредованная аллергия
V. Рецепторно - опосредованная аллергия
Типы аллергических реакций
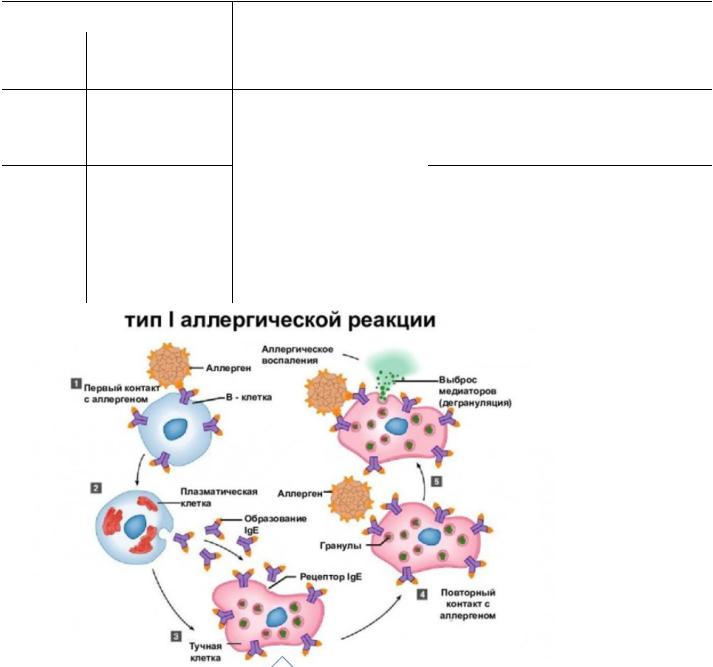
Аллергические реакции |
Примеры |
Механизм |
|
1 типа |
Немедленного |
Анафилаксия, Крапивница, Реакция антигена с IgЕ на тучных |
|
|
типа |
Отек Квинке |
клетках, выброс медиаторов воспаления |
|
|
|
и тучных клеток |
II тина |
Цитотоксические |
Аутоиммунная |
Реакция IgG или IgM с антигеном на |
|
|
гемолитическая |
поверхности клетки, активация |
|
|
анемия |
комплемента |
|
|
Интерстициальный нефрит |
|
III гм на |
Иммунокомплексны Сывороточная болезнь |
Образование иммунных комплексов, |
|
|
е |
Васкулит |
активация коплемента и миграции ней- |
|
|
Гемолитическая |
трофилов |
|
|
анемия |
|
IV типа |
Замедленного |
Аллергический контактный Реакция Т-лимфоцитов с антигеном на |
|
|
типа |
дерматит |
поверхности клетки |
|
|
Фотодерматит |
|
Роль тучных клеток и медиаторов воспаления (гистамина) в развитие аллергических реакций немедленного типа (IgE-опосредованных)
Патогенез аллергических заболеваний

Роль кишечного микробиома в патогенезе аллергических заболеваний Результаты исследований свидетельствуют о том. что нарушения микробиоценоза желудочно-
кишечного тракта (ЖКТ) оказывают негативное влияние на иммунную систему с увеличением риска развития аллергических и иммунопатологических состояний.
Установлено, что нарушение состава кишечного микробиоценоза уже при первоначальной микробной колонизации кишечника может привести к формированию аллергических реакций в детском возрасте, и иметь весьма отдаленные последствия.
Согласно результатам последних исследований, состав кишечного микробиоценоза в значительной мере генетически предопределен: микроорганизмы распознаются рецепторами, расположенными в муциновом слое слизистой оболочки кишечника. Кроме того, доказан факт колонизации кишечника микроорганизмами околоплодных вод уже во время беременности.
Негативное влияние на становление микробиоценоза оказывают такие факторы, как осложненное течение беременности, недоношенность, оперативное родоразрешение. позднее прикладывание к груди или раннее начало искусственного вскармливания, применение антибактериальных препаратов в периоде новорожденности и раннем возрасте.
У детей с пищевой аллергией кишечная микробиота изменена преморбидно. еще до развития симптомов аллергической болезни. С началом болезни воспалительные процессы и иммунные нарушения на уровне слизистой оболочки ЖКТ могут приводить к еще более значительным отклонениям в составе микробиоценоза. В свою очередь, нарушение биоценоза кишечника может способетвовать более тяжелому течению аллергического процесса.
Аллергены (АлГ) — это вещества, в основном белки или гликопротеины, которые при первом поступлении в организм, предрасположенный к развитию аллергии, вызывают сенсибилизацию. Низкомолекулярные соединения (гаптены) являются неполными антигенами и не способны самостоятельно запускать аллергическую реакцию.
Виды аллергенов
>Пыльца растений. Аллергические заболевания, обусловленные сенсибилизацией к аллергенам ветроопыляемых растений.
>Аллергены клещей домашней пыли (видов Dennatophagoides pteronyssinus и Dennatophagoides farinae).
>Эпидермальные аллергены (кошки, собаки, лошади и т. д.).
>Грибковые аллергены (плесневых грибов).
>Другие аллергены домашней пыли (библиотечной пыли, тараканов).
>Профессиональные аллергены.
>Пищевые аллергены.
Диагностика аллергических заболеваний
>Сбор анамнеза, физикальное обследование, включающее:
■визуальное исследование верхних дыхательных путей.
■визуальный осмотр и аускультацию с целью определения клинико-динамических особенностей заболевания, выявления признаков сопутствующей аллергопатологии (БА. АД) и создания ориентиров в определении тяжести состояния.
> Эллиминационная диета - важный способ выявления причинно-значимого аллергена. > Лабораторная диагностика:
■исследование ОАК с целью выявления возможного повышения уровня эозинофилов или выявления маркеров бактериального воспаления для диф. диагностики
■цитологическое исследование смывов с ВДП путей с целью выявления эозинофилии носового секрета при первичной диагностике АР. а в дальнейшем - при дифференциальной диагностике с другим хроническим ринитом и контроля эффективности терапии
> Накожные исследования реакции на аллергены (кожное тестирование с небактериальными аллергенами) с целью подтверждения аллергической природы ринита, выявления причиннозначимых аллергенов пациентам при отсутствии противопоказаний к тестированию и определения целесообразности проведения АСИТ.
> Исследование уровня АТ к антигенам растительного, животного и химического происхождения (определение уровня аллерген-специфических IgE антител) для выявления причиннозначимых аллергенов для определения целесообразности проведения аллергенспецифической иммунотерапии (АСИТ). При проведении аллергологической диагностики уровни lgE всегда должны интерпретироваться в свете результатов анамнестических и клинических данных.
> Молекулярно-генетическое исследование, подтверждающих с достоверной точностью аллергический генез заболевания и определяющих прогноз эффективности АСИТ.
Благодаря современным подходам можно не только установить правильный диагноз, но и выявить действительно ключевые причиннозначимые аллергены.
Компонент разделенная аллергодиагностика — основа для назначения специфической иммунотерапии и прогнозирования ее эффективности, при этом полученные результаты способны дать прогноз развития перекрестной реактивности, толерантности, с высокой долей достоверности.
Принципы лечения аллергических болезней Целью лечения пациентов с аллергическими болезнями является достижение контроля над
симптомами всех проявлений аллергии, сохранение трудоспособности и качества их жизни. Основные принципы лечения аллергических заболеваний заключаются в предупреждении
воздействия АлГ на восприимчивые ткани и необходимости создания устойчивости к такому воздействию.
Установлено, что достижение эффекта от лечения часто связано с уменьшением контакта, устранением причинного аллергена, проведением элиминационных мероприятий, техники использования ингаляторов, назальных спреев. Знание правил ступенчатой базисной терапии, а также навыки по профилактике тяжелых аллергических реакций и первой помощи при их развитии необходимы всем пациентам, страдающим аллергическими болезнями. Рекомендации по ограничению экспозиции к АлГ соответствуют высокому уровню доказательности. Особенно важно соблюдать элиминационный режим при серьезных ограничениях в проведении фармакотерапии. Добиться полного исключения контакта с АлГ невозможно, но существенное ограничение облегчает течение болезни.
На первом этапе диагностического поиска назначают неспецифическую гипоаллергенную диету. Лечебная элиминационная диета с полным исключением не только причинно-значимых продуктов,
но и продуктов с перекрестной реактивностью.
Существует понятие элиминационного режима. Он используется для пациентов с персистирующей астмой, аллергическим ринитом или атопическим дерматитом, когда неточно выявлены причиннозначимые аллергены.
Рекомендуется осуществлять мероприятия, направленные на уменьшение действия клещей домашней пыли, аллергенов тараканов, шерсти и продуктов жизнедеятельности домашних животных (безаллергенных животных не бывает). Обязательны следующие рекомендации:
•регулярно стирать постельное белье (1-2 раза в неделю) при температуре > 56°С для уничтожения клещей (стирка холодной водой уменьшает содержание клещевых АлГ на 90%, а стирка горячей водой уничтожает клещей);
•стирать подушки и одеяла горячей водой > 56°С и использовать для чехлов непроницаемые для клещей ткани:
•хорошая вентиляция жилища уменьшает влажность: снижение влажности в доме до 40% и ниже важно для контроля за количеством клещей и грибков.
Дополнительные сведения о профилактике читайте в Практических рекомендациях для педиатров «Аллергология и иммунология» под общей редакцией Л.С. НамазовойБарановой. 2020 г.
Одним из наиболее эффективных методов толерантности в организме сенсибилизированных пациентов является метод ACIIT. Аллергенспецифическая иммунотерапия является единственным этиопатогенетическим методом лечения аллергических болезней (аллергического ринита, конъюнктивита, бронхиальной астмы). Данный метод лечения оказывает профилактическое действие на их прогрессирование и формирование осложнений.
В последние годы, лечение тяжелой БА обогатилась новыми лекарственными препаратами. В 2003 г. создан инновационный препарат омализумаб, который представляет собой анти-IgE
антитела, препятствующий взаимодействию молекулы IgE с Fc-рецептором эффекторных клеток. Данный метод терапии эффективно применяется при тяжелых и среднетяжелых формах бронхиальной астмы, сопровождающихся высоким уровнем IgE. а также хронической идиопатической крапивницы.
Препарат связывается с IgE антителами и происходит снижение уровня свободно циркулирующих IgE антител и дальнейшего развития аллергических реакций. Удается не только снизить тяжетсь аллергического заболевания, но и сократить объем базисной противовоспалительной глюкокортикостероидной терапии.
Блокатор интерлейкинов 4 и 13 Дупилумаб — рекомбинантное человеческое моноклональное антитело (IgG4), блокирующее передачу сигналов интерлейкинов (IL) 4 и 13 путем специфического связывания их рецепторных комплексов. Препарат блокирует передачу сигналов IL4 через рецепторы I типа и общую передачу сигналов IL4 и IL13 через рецепторы II типа. Данные цитокины являются ключевыми в реализации воспаления 2-го типа при этом активируются множественные типы клеток — тучные, лимфоциты, эозинофилы. нейтрофилы, макрофаги и индуцируется выработка медиаторов — IgE. гистамина, эйкозаноидов. лейкотриенов. блокируются пути передачи сигналов IL4 и IL13 благодаря дупилумабу снижается концентрация маркеров Т2-воспаления (в том числе IgE).
Дупилумаб рекомендован в качестве дополнительной поддерживающей терапии бронхиальной астмы среднетяжелого и тяжелого течения у пациентов старше 12 лет. Он показан пациентам с эозинофильным фенотипом и, особенно, при сочетании тяжелой бронхиальной астмы и среднетяжелого/тяжелого атопического дерматита.
Ингибитор интерлейкина 5 Меполизумаб — препарат рекомбинантных гуманизированных моноклональных антител,
избирательно связывающих интерлейкин 5 (IL 5) человека.
Ингибирует биоактивность IL 5. препятствуя его связыванию с альфа-цепью рецепторного комплекса IL 5, экспрессируемого на клеточной поверхности эозпнофнлов. приводя к снижению продукции и выживаемости эозинофилов крови и дыхательных путей у пациентов с тяжелой бронхиальной астмой Т2эндотипа (как аллергического, так и неатопнческого генеза).
Для меполизумаба определены пациенты с тяжелой астмой, у которых стабильно в крови эозинофнлов более 150 кл./мкл на момент начала терапии или с числом эозинофнлов в крови более 300 кл./мкл в течение предшествующих 12 месяцев.
Эффективен в лечении детей в возрасте 6 лет и старше: на фоне лечения снизилось число обострений на 61-68%. Меполизумаб характеризовался благоприятным профилем безопасности и стабильной иммуногенностью при применении в дозе 40 мг у детей в возрасте 6-12 лет и 100 мг у детей старше 12 лет подкожно каждые 4 недели.
Профилактика аллергических заболевания Международной ассоциацией аллергологов и клинических иммунологов и Всемирной организацией
здравоохранения (ВОЗ) предложена многоуровневая комплексная программа профилактики аллергических болезней, включающая ее первичную, вторичную и третичную профилактику. Главной задачей первичной профилактики у детей из группы высокого риска являются
предотвращение сенсибилизации, с одной стороны, и необходимость формирования иммунологической толерантности — с другой.
Современная стратегия профилактики аллергии у детей на искусственном вскармливании не предусматривает полного исключения аллергена (белков коровьего молока — как наиболее значимого аллергена для детей первых месяцев жизни) из рациона ребенка.
Целью первичной профилактики с современных позиций является активное формирование у ребенка толерантности к белкам коровьего молока. Несмотря на то. что тонкие механизмы этого процесса до конца не расшифрованы, в современной научной литературе описаны некоторые факторы, влияющие на эффективность развития толерантности к белкам коровьего молока:
1 Возраст ребенка — чем младше ребенок, тем больше шансов на успешное формирование толерантности
2 Сбалансированный состав кишечной микробиоты влияет на иммунный гомеостаз в кишечнике, являясь важнейшим фактором становления толерантности.
3 Главным критерием профилактической эффективности смеси является наличие доказательств в снижении риска развития аллергической патологии, продемонстрированных в ходе клинических исследований.
В 2016 году вышли в свет обновленные требования Евросоюза к составу детских молочных смесей. В документе впервые сформулированы требования к белковому компоненту смесей на основе гидролизованных белков, которые вступят в силу с 2021 г. Обязательным будет являться двухступенчатый гидролиз с использованием трипсина и температурной обработки при 80-100°С. а также состав: на 63% — из изолята сывороточных белков, свободных от казеин-гликомакропептпда, и 37% — концентрата молочной сыворотки.
Показано, что назначение Lactobacillus GG матерям в период беременности и лактации снижает у детей частоту атопического дерматита, однако не снижает IgE сенсибилизацию. Эффективность пробиотиков в профилактике аллергии доказана только для детей, рожденных путем кесарева сечения. Грудное вскармливание необходимо сохранять как минимум до 4-6 месяцев. Введение продуктов прикорма с точки зрения толерантности в возрасте 4-6 месяцев способствует снижению риска развитии атопии в последующие годы. Раньше существовала практика отсроченного введения прикорма у детей группы риска. Введение после 6 месяцев не оказывает улучшение на развитие аллергии. Молоко и другие продукты с продукты с высокой аллергенностью следует вводить в рацион после 6 месяцев жизни. Ключевым правилом является введение прикорма межкомпонентных продуктов, а также соблюдение принципа постепенного расширения рациона (не более 1 продукта в неделю).
Вторичная профилактика направлена на предотвращение манифестации более тяжелой формы аллергических болезней.
Основная цель третичной профилактики — предупреждение тяжелого рецидивирующего течения аллергических болезней. Уменьшение частоты и продолжительности обострении.
Основные профилактические мероприятия включают:
•контроль за состоянием окружающей среды;
•аллергенспецифическую иммунотерапию;
•профилактику инфекционных заболеваний как триггеров аллергической патологии. Важное значение имеет метод специфической вакцинопрофилактики.
Бронхиальная астма Бронхиальная астма (БА) - это гетерогенное заболевание, которое характеризуется хроническим
воспалением дыхательных путей и диагностируется по респираторным симптомам свистящего дыхания, одышки, стеснения в груди или кашля, вариабельных по длительности и интенсивности, в сочетании с обратимой обструкцией дыхательных путей.
Кодирование по МКБ-10 Астма (J45):
J45.0 - Астма с преобладанием аллергического компонента J45.1 - Неаллергическая астма J45.8 - Смешанная астма J45.9 - Астма неуточненная

КЛАССИФИКАЦИЯ БРОНХИАЛЬНОЙ АСТМЫ
По этиологии |
Иммунологическая Не иммунологическая |
|
По степени |
- |
Интермиттирующая |
тяжести |
- |
Легкая персистирующая |
|
- |
Средней тяжести персистирующая |
|
- |
Тяжелая персистирующая |
Клинико |
Атопическая |
|
патогенетический |
Инфекционная |
|
вариант |
Аспириновая |
|
|
Бронхоконстрикция физического напряжения Пищевая |
|
|
Стероидозависимая |
|
По уровню |
Контролируемая |
|
контроля |
Частично контролируемая (более 2 приступов в неделю, есть ночные, ПСВ |
|
|
ниже нормы, ограничение активности) |
|
|
Не контролируемая (3 и более признака) |
|
Фаза |
Обострение, ремиссия |
|
Классификация бронхиальной астмы по степени тяжести 28 слайд
Тяжелая персистирующая астма
•Постоянные симптомы
•Частые обострения
•Частые ночные симптомы
•Физическая активность ограничена проявлениями бронхиальной астмы
•ПСВ меньше 60% от должного
•Колебания ПСВ более 30%
Средней тяжести персистирующая астма
•Ежедневные симптомы: обострения нарушают активность и сон
•Ночные симптомы астмы возникают более 1 раза в неделю
•Ежедневный прием бета2-агонистов короткого действия
•ПСВ 60-80% от должного
•Колебания ПСВ 20-30%
Легкая персистирующая астма
•Симптомы 1 раз в неделю или чаще, но не реже 1 раза в месяц
•Обострения могут нарушать активность и сон
•Ночные симптомы астмы возникают чаще 2 раз в месяц
•ПСВ более 80% от должного
•Колебания ПСВ 20-30% Интермитирующая астма
•Симптомы реже 1 раза в неделю
•Короткие обострения заболевания (от нескольких часов до нескольких дней) Ночные симптомы 2 раза в месяц или реже
•Отсутствие симптомов и нормальная функция легких между обострениями
•ПСВ более 80% от должного
•Колебания ПСВ менее 20%
Контроль является наиболее предпочтительным и общепринятым динамическим критерием, характеризующим состояние пациента с бронхиальной астмой.
Достижение контроля - основная цель лечения астмы.
Степень контроля над имеющимися симптомами - оценка текущих клинических проявлений, включает:
•выраженность дневных и ночных симптомов:
•потребность в короткодействующих В2-агонистах (КДБА);
•ограничение физической активности.
Стратегия фармакотерапии при астме представлена 5-тн ступенчатой терапией. При лёгком течении используется терапия 1-2 ступени, при среднетяжелой 3 ступени, при тяжелой 4-5 ступени.
Медикаментозную терапию бронхиальной астмы см. в Клинических рекомендациях 2019 г. Диспансерное наблюдение детей с БА
>Наблюдение детей с БА осуществляется аллергологом-иммунологом и педиатром.
>По показаниям проводятся консультации пульмонолога, оториноларинголога, гастроэнтеролога, фтизиатра, невролога.
>В амбулаторно-поликлинических условиях кратность консультаций аллергологаиммунолога. в зависимости от тяжести течения астмы у пациента и уровня контроля над болезнью, может составить 1 раз в 1-6 месяцев, педиатром - 1 раз в 3-6 месяцев.
Обследование детей с подозрением на БА может проводиться как в дневном, так и в круглосуточном стационаре, а также амбулаторно (в зависимости от выраженности симптомов заболевания). Сроки госпитализации в целях обследования и назначения (а также коррекции) базисной терапии могут составить от 5 до 14 дней (в зависимости от состояния пациента). Детям с обострением БА лечебные мероприятия могут проводиться амбулаторно, бригадой «скорой помощи», в отделениях неотложной помощи, в дневном / круглосуточном стационаре.
Диспансерное наблюдение является одним из важных компонентов успешного лечения больного БА. который проводит участковый педиатр и врач специалист аллерголог и или пульмонолог.
В задачи участкового педиатра входят: раннее выявление детей с БА, наблюдение детей с риском развития БА проводится в декретированные сроки: на первом году - ежемесячно первые 6 месяцев, затем в 9 и 12 месяцев, далее ежегодно. Нередко начальные проявления БА протекают под маской респираторной инфекции, «часто болеющие дети» требуют углубленного обследования и направления к специалистам. Контроль за БА осуществляется в соответствии с индивидуальным планом наблюдения: пациентов с лёгкой БА 1 раз в 12 месяцев, среднетяжелой и тяжелой БА - не реже 1 раза в 6 месяцев (с исследованием ФВД).
Амбулаторное лечение БА проводится по показаниям или по рекомендации специалиста. Оценка эффективности начальной противовоспалительной базисной терапии у детей со среднетяжелой и тяжелей БА проводится через 1 месяц, далее при эффективности терапии - через 3-6 месяцев, при неэффективности необходима госпитализация в специализированный стационар.
Обязательный компонент диспансерного наблюдения - выявление и санация очагов хронической инфекции, отбор детей с БА для этапного лечения в местных санаториях и организация восстановительного комплексного лечения, оформление медицинских заключений для детей-инвалидов
стяжелой БА, советы по профориентации больного ребенка.
План диспансеризации детей с БА согласовывается с аллергологом и/или пульмонологом. При наличии сопутствующего АР, АтД - с оториноларингологом, дерматологом.
Аллергический ринит - заболевание, характеризующееся lgE-опосредованным воспалением слизистой оболочки носа, развивающиеся под действием аллергенов, и наличием ежедневно проявляющихся в течение часа и более хотя бы 2 симптомов:
♦заложенность (обструкция) носа,
♦выделения из носа (ринорея),
♦чихание,
♦зуд в полости носа.
>АР часто сочетается с другими аллергическими заболеваниями, такими как аллергический конъюнктивит, атопический дерматит, бронхиальная астма (БА).
>АР рассматривается как фактор риска развития БА, неконтролируемый АР среднетяжелого течения приводит к снижению контроля над симптомами БА.
>АР является одним из звеньев реализации АТОПИЧЕСКОГО МАРША.
АР по механизму развития относится к аллергическим реакциям немедленного типа
Особенности формирования АР в детском возрасте
>Дети, у которых оба родителя имеют атопические заболевания, чаще развивают симптомы АР до пубертатного возраста, увеличивая риски развитие БА в 3-5 раз;
>Если болен только один родитель, то аллергическое заболевание у ребенка может развиться
позже;
>Показана высокая частота встречаемости АР у детей и подростков среди жителей больших городов, а также среди первенцев в семье;
>Круглогодичной АР может развиваться в очень раннем возрасте, тогда как сезонной АР обычно не развивается до 2-х летнего возраста, так как два сезона палинации необходимы для сенсибилизации;
>АР предиктор таких заболеваний, как БА, депрессия, нарушая качество жизни пациента.
>АР и ОРВИ потенцируют друг друга, формируя «порочный круг».
Респираторные вирусы, взаимодействуя с аллергенами, способствуют развитию и/или обострению аллергических заболеваний
Дети с аллергическими заболеваниями имеют сниженную противоинфекционную резистентность Группы риска развития тяжелого осложненного течения ОРВИ
Распространенность в различных регионах РФ |
|
|
||
В анамнезе |
Бронхиальна |
Атопический |
Аллергический ринит |
Часто болеющие дети |
|
я астма |
дерматит |
|
|
Доля детского |
5-10% |
6,2 - 15,5% |
18 - З8%3 |
20 - 65%4 |
населения |
|
|
|
|
Абсолютное кол-во |
2,5 млн |
4,65 млн |
до 11,5 млн |
До 19 млн |
Согласно Ориентировочным расчетным данным National Center for Immunization and Respiratory Diseases около 70% детской популяции в России (что составляет = 21 млн. детей) в зоне риска развития тяжелого / осложненного течения ОРВИ*
Диагностика аллергического ринита (АР)
>Сбор анамнеза, физикальное обследование, включающее:
■визуальное исследование верхних дыхательных путей,
■визуальный осмотр и аускультацию с целью определения клинико-динамических особенностей заболевания, выявления признаков сопутствующей аллергопатологии (БА, АД) и создания ориентиров в определении тяжести состояния.
> Лабораторная диагностика:
