
Полезные материалы за все 6 курсов / Учебники, методички, pdf / Биохимия учебное пособие
.pdf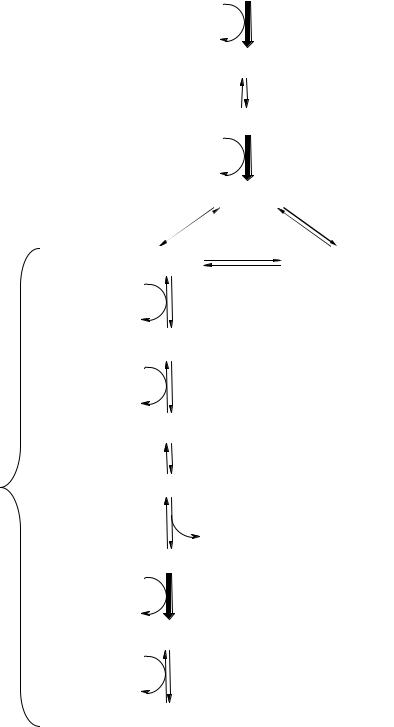
|
|
|
Глюкоза |
|
1 |
АТФ |
Гексокиназа, Mg2+ |
|
|
||
|
|
АДФ |
|
|
|
Глюкозо-6-фосфат |
|
|
2 |
|
Фосфоглюкоизомераза |
|
|
Фруктозо-6-фосфат |
|
|
|
АТФ |
|
|
3 |
АДФ |
Фосфофруктокиназа, Mg2+ |
|
|
|
|
|
|
Фруктозо-1,6-бисфосфат |
|
|
|
|
4 |
|
5 |
|
Альдолаза |
|
|
Изомераза |
|
|
3-Фосфоглицеральдегид |
||
|
ИзомДиоксиацетонфосфат |
||
|
ФН + НАД + |
|
Диоксиацет |
|
6 |
3-ФГА-дегидрогеназа |
|
|
НАДН2 |
|
|
|
1,3-Дифосфоглицерат |
||
|
АТФ |
|
|
|
7 |
Фосфоглицераткиназа |
|
|
АДФ |
|
|
|
3-Фосфоглицерат |
|
|
|
8 |
Фосфоглицератмутаза |
|
2 |
2-Фосфоглицерат |
|
|
|
9 |
Енолаза |
|
|
|
Н2О |
|
|
Фосфоенопируват |
|
|
|
АТФ |
|
|
|
10 |
Пируваткиназа, Мg2+ |
|
|
АДФ |
|
|
|
Пируват |
|
|
|
НАДН2 |
|
|
|
11 |
Лактатдегидрогеназа |
|
|
НАД+ |
|
|
Лактат (молочная кислота)
Рис.14.Схема реакцийгликолиза
50

Образовавшийсяфруктозо-6-фосфатнатретьейстадиифосфорилируетсядофрук- тозо-1,6-дифосфата. Подобно гексокиназной, эта реакция необратима и является наиболеемедленной реакцией гликолиза:
CH OPO H |
|
|
АТФ |
2+ АДФ |
CH OPO H |
||||||||||||
|
|
2 |
3 |
2 |
|
АТФ |
Mg АДФ |
|
|
2 |
3 |
2 |
|
||||
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
O |
|
|
CH2OH |
Mg2+ |
|
|
|
|
O |
|
|
CH2OPO3H2 |
||
|
|
H |
HO |
|
|
|
|
|
|
H |
HO |
|
|||||
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
|
|
H |
|
|
|
OH |
||||||
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
H |
|||
|
|
OH |
|
|
|
|
|
|
OH |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Ферментфосфофруктокиназа, катализирующий этустадию, являетсяважным ключевым ферментом гликолиза. Фосфофруктокиназа относится к числуаллостерическихферментов. Она ингибируетсяАТФи стимулируетсяАМФ.При увеличении отношенияАТФ/АМФактивностьфосфофруктокиназыугнетаетсяи гликолиз замедляется. Напротив, при снижении этого коэффициента интенсивность гликолиза повышается. Так, в неработающей мышце концентрация АТФ относительно высокая, соответственно активность фосфофруктокиназы низкая. Во время работы мышцы происходит интенсивное потребление АТФ и активность фосфофруктокиназы повышается, что приводит к усилению процесса гликолиза.
Четвертая стадия заключается в расщеплении фруктозо-1,6-дифосфата ровно пополам на две фосфотриозы. Эту обратимую реакцию катализирует альдола- зафруктозобисфосфата.Продуктыреакции3-фосфоглицеральдегид(ФГА)идигид- роксиацетонфосфат (ДГАФ) изомерны друг другу:
1
CH2OPO3H2
2
C O ДГАФ
O ДГАФ
OPO3H2 |
3 |
|
OH |
|
|||
CH |
|||
|
2 |
|
|
6
CH2 1
O CH2OPO3H2
5 H |
HO |
2 |
|
|
|
|
|
|
|
|
|
||
H |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
4 |
|
3 |
|
4 |
|
|
|
|
|
|
|||
OH |
H |
H |
|
|
C |
|
|
|
O |
|
|||
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
5 |
|
|
|
|
|
ФГА |
|
|
|
|
|
H |
|
C |
|
OH |
|||||
|
|
|
|
|
|
||||||||
Фруктозо-1,6-бисфосфат |
6 |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
CH2OPO3H2 |
|
||||||
51
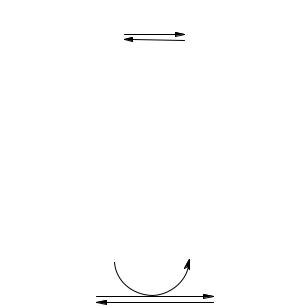
Пятую стадию обеспечивает фермент триозофосфатизомераза, ускоряющий превращениедигидроксиацетонфосфата в3-фосфоглицеральдегид. Вравновесном состояниидоляфосфоглицеральдегиданеболее5%.Однаковдальнейшихреакциях используется именно этот изомер. Поэтому фактически триозофосфатизомераза обеспечивает достаточно быстрое восполнение 3-фосфоглицеральдегида по мере егоубыли (т. е. катализирует реакцию, посуществу, в одном направлении). На этом завершается первый этап гликолиза.
Шестая стадия – окисление альдегидной группы 3-фосфоглицеральдегида под действием 3-фосфоглицеральдегид-дегидрогеназы. Обычно окислениеальдегидной группы происходит путем присоединения молекулы воды с последующим отнятием 2 атомов водорода, вследствие чего альдегидная группа превращается вкарбоксильную.Однакоприокислении3-фосфоглицеральдегидаспецификаНАД+- зависимойдегидрогеназыобеспечиваетиспользованиеневоды,афосфорнойкислоты. В результате образующаяся карбоксильная группа сразу же оказывается связанной с фосфатным остатком. Возникшая смешанная ангидридная связь является макроэргической:
|
|
O |
|
|
|
|
|
|
O |
|
|
|
|
||||||||||
|
|
|
C |
|
|
|
|
|
H |
+ H3PO4 + НАД + |
|
|
|
|
|
C |
|
|
|
|
|
O ~PO3H2 |
+ НАДН2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H |
|
C |
|
|
OH |
6 |
H |
|
C |
|
OH |
||||||||||||
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OPO3H2 |
|
|
|
CH2OPO3H2 |
|
||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
ФГА |
|
|
|
|
1,3-Бисфосфоглицерат |
|
||||||||||||||
Седьмая стадия представляет собой реакцию субстратного фосфорилирования. За счет энергии, выделяющейся при гидролизе макроэргической связи в 1,3- дифосфоглицератепроисходитпереносотщепляемогофосфатногоостаткана АДФ и образование молекулы АТФ. Эта реакция обратима. Фермент, катализирующий эту реакцию, называется фосфоглицераткиназа (по обратной реакции).
|
|
O |
|
|
АДФ |
АТФ |
||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
C |
|
|
|
|
|
O ~ PO3H2 |
|
|
|
COOH |
||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
C |
|
OH |
||||||||||||
H |
|
C |
|
OH |
|
|
||||||||||
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
7 |
|
|
|
|
|
|
|
|
|
|
CH2OPO3H2 |
|
|
|
CH2OPO3H2 |
|||||||
1,3-Бисфосфоглицерат |
3-Фосфоглицерат |
|||||||||||||||
52

Далее под действием фермента фосфоглицератмутазы 3-фосфоглицерат изомеризуется в 2-фосфоглицерат:
|
|
COOH |
|
|
|
|
|
COOH |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
C |
|
OH |
8 |
|
H |
|
C |
|
OPO3H2 |
|||
|
|
|
|
|
||||||||||
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
CH2OPO3H2 |
|
|
|
|
|
CH2OH |
||||||
3-Фосфоглицерат |
|
|
|
2-Фосфоглицерат |
||||||||||
Девятая стадия – дегидратация 2-фосфоглицерата. Эту обратимую реакцию катализирует фермент енолаза:
|
|
|
COOH |
|
|
|
H2O |
|
|
|
|
|
COOH |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O ~ PO3H2 |
H |
|
C |
|
O |
|
|
PO3H2 |
|
|
+ H2O |
|
|
|
C |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
9 |
|
|
|
|
|
|
|
|
|||||
|
|
CH2 |
OH |
|
|
CH2 |
||||||||||||||||
2-Фосфоглицерат |
|
|
|
|
|
Фосфоенолпируват |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(ФЕП) |
|
Результатом является образование сложного эфира фосфорной кислоты и енольной формыпирувата, называемогофосфоенолпируватом. Фосфоенолпируват содержитмакроэргическуюсвязь.Энергия,выделяющаясяпригидролизеэтойсвязи, используется на следующей стадии для синтеза АТФ.
Десятая стадия является реакций субстратного фосфорилирования. Катализирует ее пируваткиназа:
|
|
|
|
|
АДФ |
АТФ |
|||||
|
|
COOH |
|
COOH |
|||||||
|
|
|
|
|
O ~ PO3H2 |
|
|
|
|
|
|
|
C |
|
|
|
|
C |
|
O |
|||
|
|
|
|
10 |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
CH |
|||||||
|
|
|
|
|
|
|
3 |
|
|||
Фосфоенолпируват |
|
Пировиноградная |
|||||||||
|
|
|
(ФЕП) |
|
кислота (ПВК) |
||||||
Перенос фосфатного остатка с молекулы фосфоенолпирувата на АДФ (с образованием АТФ) приводит, однако, к освобождению неенолпирувата, а егоболее стабильногокето-изомера –пирувата. Этоделаетпируваткиназнуюреакциюнеобратимой, энергетически подкрепляя ее.
53
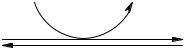
Приаэробныхусловияхпируватпроникаетвмитохондрии,гдеполностьюокисляется до СО2 и Н2О. Если содержание кислорода недостаточно, как это может иметь место в активно сокращающейся мышце, пируват превращается в лактат:
|
O |
|
|
|
|
НАДН |
2 |
НАД + |
|
|
O |
|
|
|
|
||||||
|
|
|
|
|
|
|
_ |
НАДН |
2 |
НАД+ |
|
|
|
|
|
|
|
|
_ |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
O |
|
|
|
|
|
|
|
C |
|
|
|
|
O |
||
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
O |
Лактатдегидрогеназа |
HO |
|
C |
|
|
H |
|||||||||||
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
CH3 |
|
|
|
|
|
|
|
|
CH |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
||||||
Пируват |
|
|
|
|
|
Лактат |
|
||||||||||||||
Подводя итог рассмотрению химизма процесса гликолиза, остановимся еще раз на его основных особенностях.
1.В гликолизенезависимо оттого, протекаетон поанаэробномуили аэробному пути, можно выделить два основных этапа.
Реакции 1–5 составляют первый этап гликолиза, суть которого– превращение стабильной молекулы глюкозы в две молекулы более реакционноспособного фосфоглицеральдегида. На этом этапе гликолиза расходуются две молекулы АТФ.
Второй этап гликолизавключаетреакции,приводящиекпревращениюфосфоглицеральдегида в пируват или лактат (соответственно реакции 6–10 или 6–11). Эти реакции связаны с синтезом АТФ;
2.Большинствогликолитическихреакций обратимо, за исключениемтрех(ре-
акции 1, 3и10);
3.Все промежуточные соединения находятся в фосфорилированной форме. Источникомфосфатной группыв реакцияхфосфорилированияявляютсяАТФ(реакции 1, 3) или Н3РО4 (реакция 6);
4.Регенерация НАД+, необходимого для окисления новых молекул фосфоглицеральдегида,происходитприаэробномгликолизепосредствомдыхательной цепи. При этом водород транспортируется из цитозоля в митохондрии с помощью челночного механизма.
При анаэробном гликолизе НАД+ регенерируется в реакции восстановления пирувата в лактат, сопряженного с окислением НАДН2.
5.Образование АТФ при гликолизе может идти двумя путями: либо субстрат-
ным фосфорилированием, когда для образования АТФ из АДФ и Н3РО4 используется энергия макроэргической связи субстрата (реакции 7, 9), либопутем окисли-
тельногофосфорилирования за счет энергии переноса электронов и протонов в дыхательной цепи.
3.3.2. Расчет выхода АТФ при анаэробном окислении глюкозы
Клетки, недостаточно снабжаемые кислородом, могут частично или полностью существовать за счет энергии гликолиза. В анаэробных условиях гликолиз
54
является единственным способом получения энергии для синтеза АТФ из АДФ и неорганического фосфата. На рис. 15 показаны участки гликолиза, на которых расходуется и образуется АТФ.
Глюкоза
|
2 АТФ |
|
Гексокиназа |
|
Фосфофруктокиназа |
|
2 АДФ |
|
Фосфоглицеральдегид |
|
НАД+ |
|
ГАФ-дегидрогеназа |
|
НАДН2 |
2 |
1,3-Дифосфоглицерат |
|
2 АДФ
Фосфоглицераткиназа
Пируваткиназа
2 АТФ
Пируват 
 Лактат
Лактат
Лактатдегидрогеназа
Рис. 15. Участки гликолиза, связанныесзатратой иобразованием АТФ ванаэробных условиях
2 молекулы АТФ потребляются на активацию одной молекулы глюкозы (реакции 1 и 3).
Врезультатепревращений каждогоиздвухС3-фрагментов вреакцияхсубстратного фосфорилирования (реакции 7 и 10) образуются 2 молекулы АТФ.
НАДН2, который образуется в ходе окисления фосфоглицеральдегида на пятой стадии, окисляется в лактатдегидрогеназной реакции с образованием молочной кислоты и в получении АТФ не участвует.
Такимобразом,выигрышэнергииванаэробныхусловияхсоставляет2мольАТФ на моль глюкозы:
реакция1 |
–1 АТФ |
–1 АТФ |
|
|
реакция3 |
–1 АТФ |
–1 АТФ |
|
|
реакция6 |
+1 НАДН2 |
+3 АТФ |
|
|
реакция7 |
+1 АТФ |
+1 АТФ |
2 молекулы триозы |
|
реакция10 |
+1 АТФ |
+1 АТФ |
||
|
||||
реакция11 |
–1 НАДН2 |
–3 АТФ |
|
|
Итого: –2 + 2 (3 + 1 + 1 – 3) = 2 АТФ. |
|
|||
55
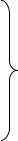
3.3.3. Расчет выхода АТФ при аэробном окислении
Большинство животных и растительных клеток в норме находится в аэробных условиях, и глюкоза полностью окисляется до СО2 и Н2О.
При наличии вклеткекислородаНАДН2, возникающий на 6-й стадии, направляетсявмитохондриинапроцессокислительногофосфорилирования.Тамегоокисление сопровождается синтезом 3 молекул АТФ.
Образовавшийся в гликолизе пируват в аэробных условиях под действием пируватдегидрогеназного комплекса превращается в ацетил-SКоА, при этом образуется 1 молекула НАДН2.
Ацетил-SКоАвовлекаетсяв циклКребса и,окисляясь,дает3молекулыНАДН2, 1молекулуФАДН2 и 1молекулуГТФ. При окислении НАДН2 и ФАДН2 в дыхательной цепи образуется еще 11 молекул АТФ. В целом при сгорании 1 ацетильного остатка образуется 12 молекул АТФ.
Суммируя «гликолитический» АТФ, результаты окисления «гликолитического»и пируватдегидрогеназногоНАДН2, энергетический выходцикла Кребса и умножая все на 2, получаем 38 молекул АТФ:
реакция1 |
–1 АТФ |
–1 АТФ |
|
реакция3 |
–1 АТФ |
–1 АТФ |
|
реакция6 |
+1 НАДН2 |
+3 АТФ |
|
реакция7 |
+1 АТФ |
+1 АТФ |
|
реакция10 |
+1 АТФ |
+1 АТФ |
|
ПВК-дегидрогеназа |
+1 НАДН2 |
+3 АТФ |
2 молекулы триозы |
ЦТК |
+1ГТФ |
+1 АТФ |
|
ЦТК |
+3 НАДН2 |
+9 АТФ |
|
ЦТК |
+1 ФАДН2 |
+2 АТФ |
|
Итого: –2 + 2 (3 + 1 + 1 + 3 +1 + 9 + 2) = 38 АТФ.
Очевидно, что в энергетическом отношении полное расщепление глюкозы является более эффективным процессом, чем анаэробный гликолиз (рис. 16).
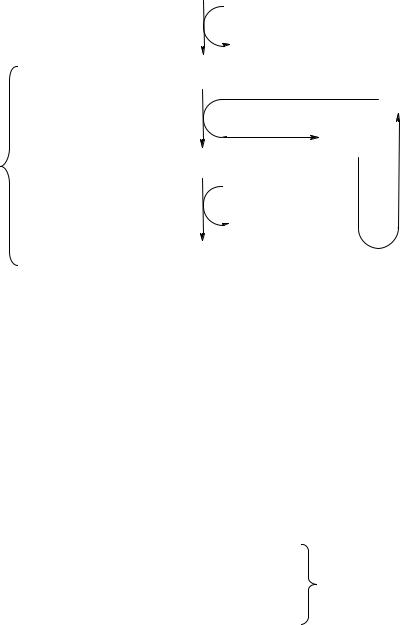
Однако мембрана митохондрий непроницаема для НАДН2, поэтому перенос водорода с цитозольного НАДН2 в митохондрии осуществляется за счет челночного транспорта. Суть этого механизма сводится к тому, что НАДН2 в цитозоле восстанавливает некоторое соединение, способное проникать в митохондрию. В митохондрии это соединение окисляется, восстанавливая внутримитохондриальный НАД+, и вновь переходит в цитозоль. В качестве челнока работает глицеролфосфатный механизм или малат-аспартатная система (рис. 17, 18).
Если перенос водорода с НАДН2 происходит за счет глицеролфосфатного механизма, то реальное количество синтезируемых молекул АТФ меньше, так как энергия расходуется на транспорт НАДН2 из цитозоля через митохондриальную мембрану. Цитозольный НАДН2 сначала реагируетсцитозольнымдигидроксиаце- тонфосфатом,образуяглицерол-3-фосфат, который легкопроникаетчерезмембрану
56
|
Глюкоза |
|
|
2 АТФ |
|
|
Гексокиназа |
|
|
Фосфофруктокиназа |
|
|
2 АДФ |
|
|
Фосфоглицеральдегид |
|
|
НАД+ |
|
|
ГАФ-дегидрогеназа |
|
|
НАДН2 |
|
|
1,3-Дифосфоглицерат |
|
|
2 АДФ |
|
|
Фосфоглицераткиназа |
|
|
Пируваткиназа |
|
|
2 АТФ |
|
|
Пируват |
|
|
НАД+ |
|
2 |
ПВК-дегидрогеназа |
|
НАДН2 |
||
|
||
|
Ацетил-SКоА |
Цикл Кребса
ГТФ |
|
|
НАД + |
3 |
НАДН |
3 |
|
|
2 |
1 |
ФАД |
1 |
ФАДН2 |
Дыхательная цепь митохондрий
Рис. 16. Участкиаэробногоокисления глюкозы, связанные с затратой и образованием АТФ
митохондрии. Внутри митохондрии глицерол-3-фосфат окисляется до диоксиацетонфосфата с участием неНАД, а ФАД-зависимой глицерол-3-фосфат-дегидроге- назы. Восстановленный флавопротеин (фермент-ФАДН2) вводит приобретенные имэлектронывдыхательнуюцепьна уровнеKoQ. Такимобразом, параэлектронов (из одной молекулы цитозольного НАДН2), вводимая в дыхательную цепь с помощью глицеролфосфатного челночного механизма, дает не 3, а 2 АТФ и общий энергетический выход составляет не 38, а 36 молекул АТФ.
57
Фосфоглицеральдегид  1,3-Бисфосфоглицерат
1,3-Бисфосфоглицерат
НАД+ НАДН2
Цитозоль
1
-Глицерофосфат |
Диоксиацетонфосфат |
|
|
2 |
|
Внутренняя |
3 |
|
мембрана |
|
|
митохондрий |
ФАД2 |
в ЦПЭ |
ФАД |
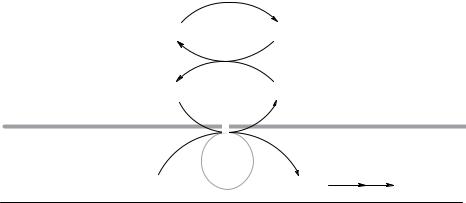
Рис. 17. Глицеролфосфатныйчелнок:
1, 2 – окислительно-восстановительные реакции, обеспечивающие транспорт водорода из цитозоля
вмитохондрии на дыхательную цепь; 3 – ФАД-зависимая глицеролфосфатдегидрогеназа
Спомощьюданногочелночногомеханизма переносвосстановленныхэквива-
лентов от цитозольного НАДН2 в митохондрии осуществляется лишь в скелетных мышцах и мозге.
В клетках печени, почек и сердца действует более сложная малат-аспартатная челночная система (см. рис. 18).
Действие такого челночного механизма становится возможным благодаря присутствиюмалатдегидрогеназыиаспартатаминотрансферазыкаквцитозоле,так
ив митохондриях. Цитозольный НАДН2 восстановливает оксалоацетат домалата при участии фермента малатдегидрогеназы.
Малат с помощью системы, транспортирующей дикарбоновые кислоты, проходит через внутреннюю мембрану митохондрии в матрикс. Здесь малат за счет внутримитохондриального НАД+ окисляется в оксалоацетат, а восстановленный
НАДН2 передает свои электроны в цепь дыхательных ферментов.
В свою очередь, образовавшийся оксалоацетат в присутствии глутамата и фермента АСТ вступает в реакцию трансаминирования. Образующиеся аспартат
и-кетоглутарат спомощью специальныхтранспортных системспособны проходить через мембрану митохондрий. Трансаминирование в цитозоле регенерирует оксалоацетат, что вызывает к действию следующий цикл.
В целом процесс включает легкообратимые реакции, происходит без потребления энергии, в результате полного окисления одной молекулы глюкозы может образоваться не 36, а 38 молекул АТФ.
При переходе от анаэробных условий к аэробным накопление лактата в клетке прекращается в связи с его окислением в пируват. Первым это явление отметил Л. Пастер, сформулировав тезис о том, что с началом дыхания (т. е. потребления кислорода) брожение останавливается. Он определял брожение как жизнь без доступа кислорода.
58
Фосфоглицеральдегид  1,3-Бисфосфоглицерат
1,3-Бисфосфоглицерат
ÍÀÄ + |
ÍÀÄÍ2 |
|
1 |
|
Малат |
Оксалоацетат |
|
|
|
|
Глутамат |
Циòîçîлü |
|
|
|
|
|
-Кетоглутарат |
|
|
|
Аспартат |
|
Внутренняя |
3 |
|
4 |
мембрана |
|
||
ìиòîхîíдðий |
|
|
|
Мàòðикñ |
|
Аспартат |
|
ìиòîхîíдðий |
|
|
|
|
-Кетоглутарат |
||
|
|
||
|
Малат |
Оксалоацетат |
Глутамат |
|
|
||
|
|
2 |
|
|
ÍÀÄ + |
ÍÀÄÍ2 |
â ЦÏЭ |
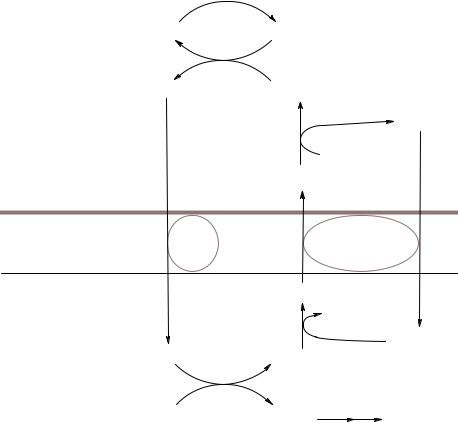
Рис. 18. Малат-аспартатный челнок:
1, 2 – окислительно-восстановительные реакции, обеспечивающие транспорт водорода из цитозоля
âмитохондрии на дыхательную цепь; 3, 4 – транслоказы, обеспечивающие транспорт малата, аспартата
èглутамата через мембрану митохондрий
Механизм эффекта Пастера (блокирование брожения дыханием, сопровождаемое резким падением скорости утилизации глюкозы) объясняется тем, что в присутствии кислорода НАДН2 и пируват сразу после их образования утилизируются митохондриями. При переключении на аэробное окисление происходит убыль ранее накопленного лактата. Утилизация лактата, накопившегося в период дефицита кислорода, лежит в основе явления, которое получило название «ликвидация кислородной задолженности». Суть этого явления состоит в том, что после интенсивной мышечной работы легочное дыхание не сразу возвращается к норме, а некоторое время остается усиленным. Избыточное потребление кислорода в этот период определяется количеством лактата, накопившегося во время работы, недостаточно обеспеченной кислородом.
Таким образом, в отсутствие или при недостатке кислорода лактат не может не образоваться, а при достаточном снабжении кислородом он не может образоваться (ðèñ. 19).
59
