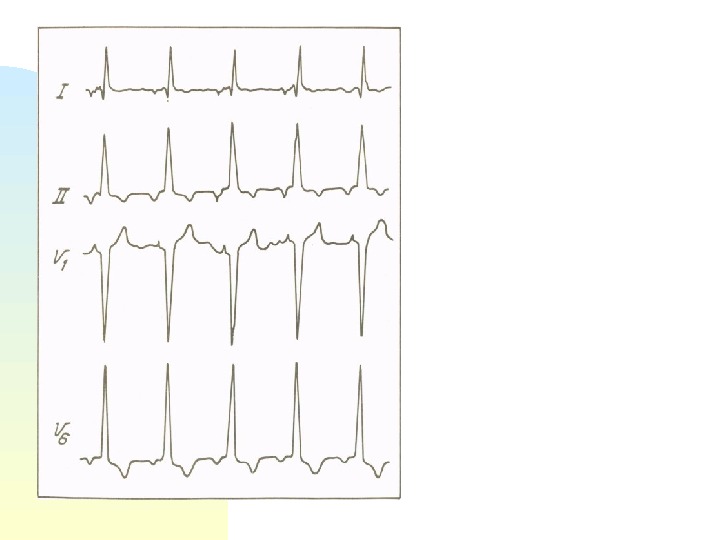
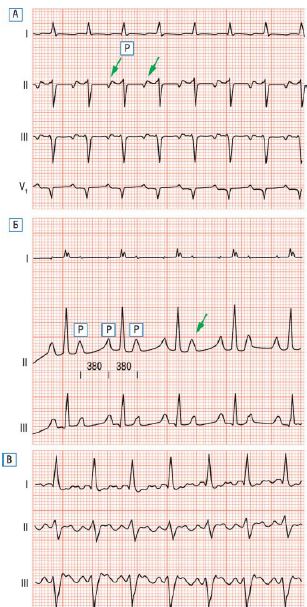
- •Трепетание предсердий, в большинстве случаев, является правильной формой нарушения ритма, т.Е. Кратность ав-проведения является одинаковой (с равными интервалами r-r).
- •Трепетание предсердий, проведение 3:1
- •Трепетание предсердий, проведение 3:1, 2:1
- •Для купирования приступа трепетания предсердий возможно использование электрической кардиоверсии.
- •Для купирования приступа фибрилляции предсердий возможно использование электрической кардиоверсии.
Для адекватного функционирования миокарда при меняющихся физиологических условиях организма важна правильная скоординированная работа проводящей системы сердца (ПСС). ПСС представляет собой комплекс анатомических образований, регулирующих возникновение электрического импульса, последовательную передачу волны возбуждения по отделам сердца, с формированием синхронного сокращения миокарда. Иерархия ПСС представлена водителями ритма нескольких порядков.
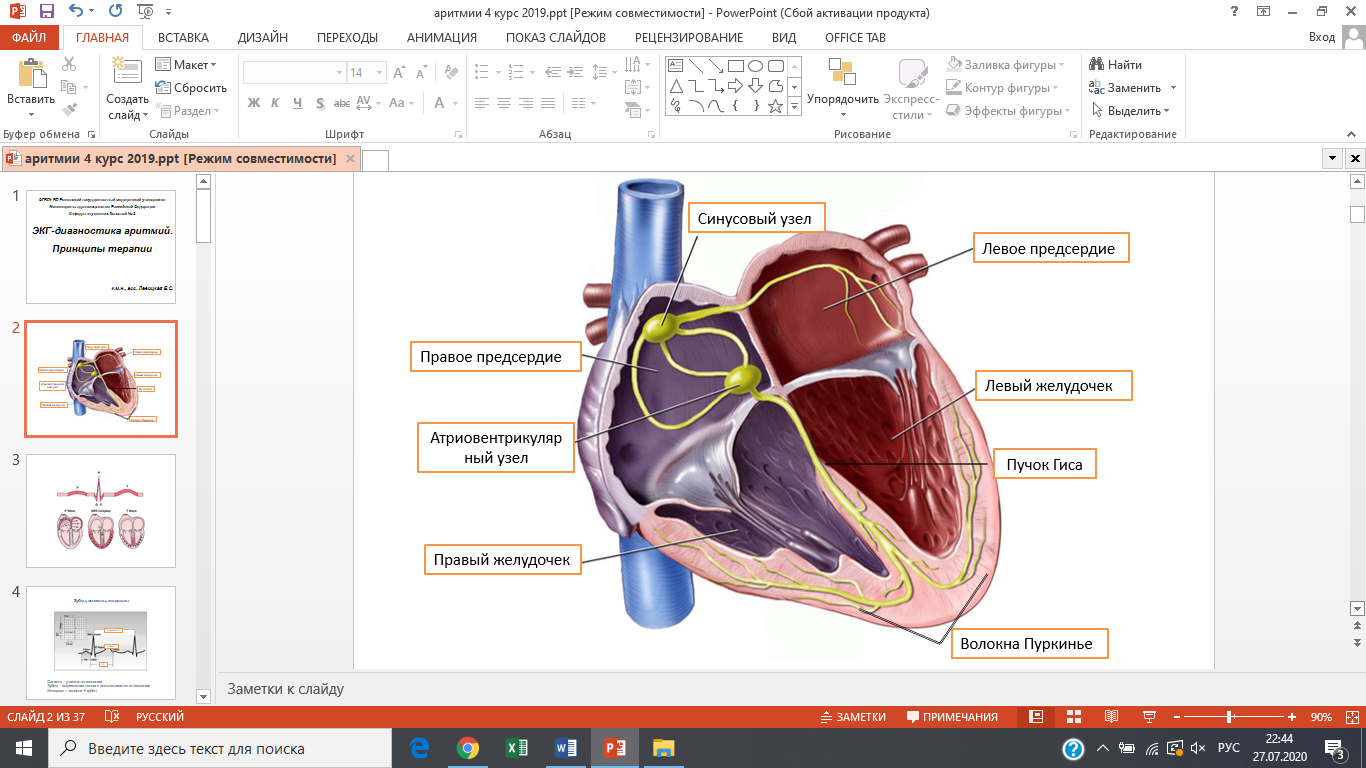
Водителем ритма первого порядка является синусовый узел (узел Кис-Фляка), главной функцией которого является спонтанное возбуждение миокарда для обеспечения работы организма в различных физиологических ситуациях. Синусовый узел располагается субэпикардиально в стенке правого предсердия, в непосредственной близости от устья верхней полой вены. Кровоснабжение синусового узла происходит из синоатриальной артерии, являющаяся, в большинстве случаев, ветвью левой коронарной артерии. Клетки синусового узла являются атипичными клетками миокарда, характеризующиеся высокой возбудимостью и отличительными гистологическими свойствами от обычных кардиомиоцитов. В структуре синусового узла различают Р- и Т-клетки. Р-клетки выполняют функцию автоматизма, т.е. способны к спонтанному возбуждению и генерации импульса. Т-клетки осуществляют пейсмекерную функцию – проведения возбуждения. Знание строения синусового узла дает представление не только о инициирующих этапах сердечного цикла, но и распространенной патологии проводимости сердца – синдроме слабости синусового узла, причинами которого являются нарушение кровоснабжения в синоатриальной артерии или дегенеративные изменения миокарда синусового узла.
Электрический импульс, генерированный клетками синусового узла, проходит по трем проводящим путям: переднему, среднему и заднему межузловым путям.
Передний межузловой путь представлен двумя ветвями. Первая ветвь, называемая пучком Бахманна, достигает левого предсердия, вторая – по межпредсердной перегородке атриовентрикулярного узла.
Пучок Венкебаха представляет средний межузловой путь и анастамозируя с клетками переднего межузлового пути проходит позади верхней полой вены, по межпредсердной перегородке к клеткам атриовентрикулярного узла.
Пучок Тореля формирует задний межузловой путь, являясь наиболее длинным пучком межузловых путей. Начинаясь от синусового узла, достигает коронарного синуса и далее следует к задней части атриовентрикулярного узла.
Необходимо обратить внимание, что все межузловые пути на анастомозируют друг с другом, создавая единую систему проведения импульса по предсердиям. Важно отметить существование дополнительных межузловых проводящих путей, ускоряющих время проведения импульса от предсердия к желудочкам и, являющихся потенциальной причиной высокочастотных нарушений ритма сердца.
Атриовентрикулярное соединение (атриовентрикулярный узел, узел Ашоффа-Тавара) состоит из клеток проводящей системы, способных проводить импульсы далее по проводящей системе сердца от предсердий к желудочкам. Более того, клетки атриовентрикулярного узла обладают способностью к спонтанному автоматизму, в случае дисфункции синусового узла, являясь водителем ритма второго порядка. Важно отметить роль «биологического фильтра» атриовентрикулярного соединения, которая обусловлена необходимостью клеток к восстановлению трасмембранного потенциала и перехода в фазу деполяризации, т.е. способности проводить электрический импульс. Данная функция имеет очень важное значение в препятствии высокочастотных жизнеугрожающих желудочковых нарушениях ритма при наличии предсердных тахиаритмий.
Атриовентрикулярный узел расположен справа от межпредсердной перегородки, над трикуспидальным клапаном. По аналогии со строением синусового узла, атриовентрикулярное соединение представлено Р- (меньшее количество по сравнению с синусовым узлом) и Т-клетками. Кровоснабжение в большинстве случаев происходит из ветви правой коронарной артерии, называемой артерией атриовентрикулярного узла.
Система волокон Гиса, является водителем ритма третьего порядка проводящей системы сердца, которая состоит из пучка Гиса и его ножек. Пучок Гиса начинается от соединительнотканого пучка между предсердиями и желудочками и продолжается по межжелудочковой перегородке. В мышечной части межжелудочковой перегородки происходит деление (бифуркация) пучка Гиса на правую и левую ножки. Кровоснабжение пучка Гиса происходит из артерии атриовентрикулярного узла.
Ножки пучка Гиса проходят субэдокардиально по соответствующей стороне сердечной мышцы. Правая ножка пучка Гиса более тонкое образование проводящей системы по сравнению с толстой и короткой левой ножкой. В большинстве случаев правая ножка не имеет ветвлений или они малоразвиты. Конечным этапом правой ножки являются сосочковые мышцы правого желудочка, после которых происходит разветвление и соединение с системой Пуркинье.
Левая ножка пучка Гиса практически сразу отдает ветви – переднюю и заднюю. Существует несколько мнений о количестве ветвей левой ножки пучка Гиса. Общепринятым считается наличие передней и задней ветви левой ножки пучка Гиса. Передняя ветвь левой ножки пучка Гиса более длинная и тонкая и достигает передней сосочковой мышцы левого желудочка, задняя ветвь напротив имеет меньшую длину, но больше в диаметре и подходит к задней сосочковой мышцы левого желудочка. Далее происходит анастомозирование ветвей левой ножки пучка Гиса с ситемой Пуркинье. Кровоснабжение ножек происходит из передней (правая ножка и две трети левой ножки) и задней (одна треть левой ножки) нисходящей артерии.
Волокна Пуркинье представляют собой сеть мелких волокон проводящей системы сердца, связывающиеся с сократительными клетками миокарда. Клетки волокон Пуркинье являются водителями ритма четвертого порядка, но обладают малыми эффектами автоматизма и способности к спонтанной генерации импульса. Поскольку волокна Пуркиньей связываются с сократительными клетками миокарда, то кровоснабжение их происходит из капиллярной сети соответствующей области сердечной мышцы.
Аритмия сердца –патологическое состояние, при котором происходят нарушения частоты, ритмичности и последовательности возбуждения и сокращения сердца. Аритмия – любой ритм сердца, отличающийся от нормального синусового ритма. При некоторых аритмиях может существенно нарушаться нормальная сократительная активность сердца, что может привести к целому ряду серьёзных осложнений.
Под влиянием одного или нескольких этиологических факторов нарушается одна или несколько функций сердца:
автоматизм (автоматическая генерация импульсов кардиомиоцитамиводителем ритма)
возбудимость (способность кардиомиоцитов генерировать потенциал действия в ответ на раздражение)
проводимость (проведение импульса по проводящей системе сердца)
сократимость (сокращение сократительных кардиомиоцитов)
рефрактерность (электрическая инертность КМЦ некоторое время после проведения импульса, не допускающая возврат проведенного импульса и наложение последующего)
абберантность (возможность проведения импульса по дополнительным путям проводящей системы сердца)
В основе возникновения всех аритмий лежит нарушение образования или нормального проведения импульсов. Причиной может являться развитие как одного патологического механизма, так и их комплексное воздействие.
К основным механизмам нарушений ритма сердца относят:
- механизм «re-entry» (повторного входа волны возбуждения) – многократная круговая циркуляция волны возбуждения, возникшая от одного импульса, на одном участке миокарда. Условие формирования механизма«re-entry» - однонаправленная блокада вначале движения импульса. Затем, этот импульс, обходя невозбудимый участок, возвращается через первоначальное место, замыкая петлю возбуждения и двигаясь с многократным совершением одной траектории движения. Необходимо обратить внимание, что петля возбуждения может развиваться одна или несколько. На основании этого выделяют микро- и макро-механизмы «re-entry».
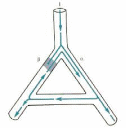
Схема механизма «re-entry»
- эктопический автоматизм – ритм сердца, возникающий в других отделах миокарда или проводящей системе сердца. Эктопический очаг в таком случае принимает на себя работу основного водителя ритма. Существует разновидности эктопического автоматизма, согласно зоне инициации импульса. Эктопический автоматизм может быть причиной как тахикардий, так и ритмов с замедлением частоты сердечных сокращений. Снижение частоты проведения импульса возникает в том случае, когда водителем ритма являются клетки проводящей системы сердца, имеющие меньшую способность к автоматизму.
- триггерная активность – нарушение ритма сердца, связанное с возникновением автоматизма в клетках в фазе постдеполяризации, т.е. после прохождения потенциала действия остаточные электрические процессы могут привести к развитию потенциала действия. В зависимости от фазы потенциала действия, в период которой развилась триггерная активность выделяют раннюю и позднюю постдеполяризацции. Причиной возникновения триггерной активности считают недостаточная калиевая проводимость и повышенное содержание внутриклеточного кальция. Необходимо отметить, что характерными признаками аритмий, формированных по типу триггерной активности, является постепенное начало и окончание пароксизма, а также инициация и купирование при воздействии электростимуляции.
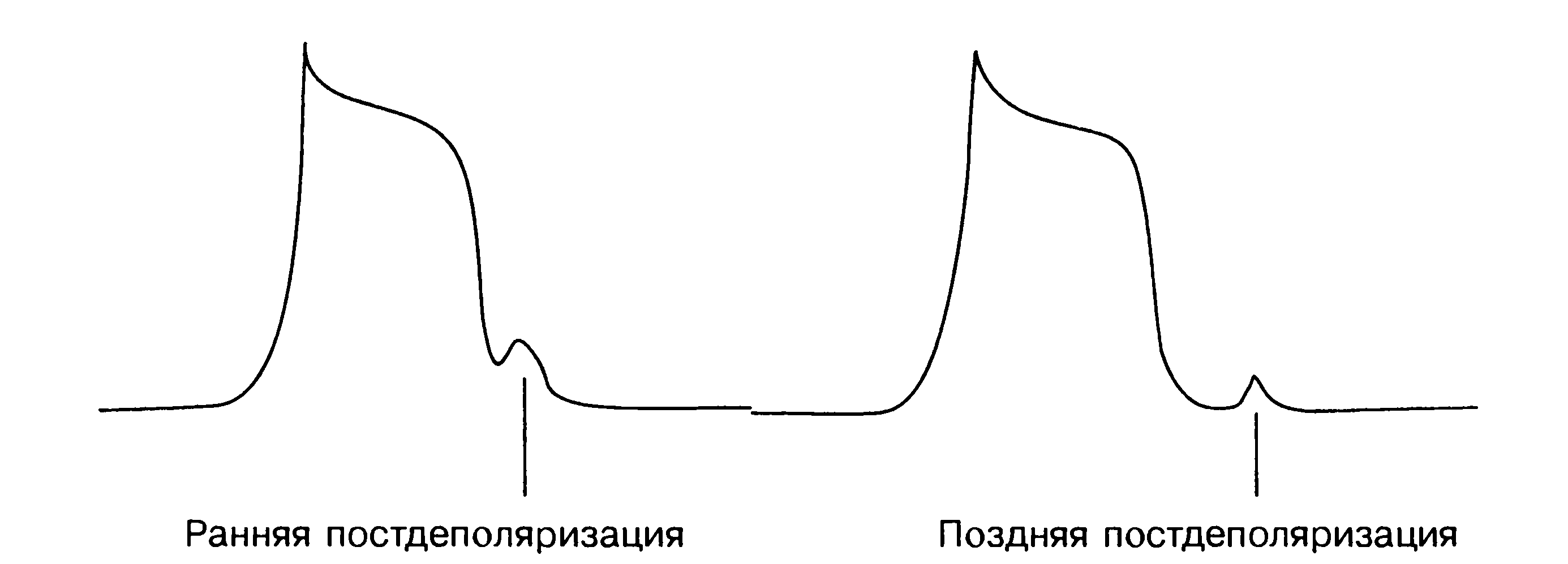
Схема развития вариантов триггерной активности в зависимости от фазы потенциала действия
Наиболее частые причины нарушений сердечного ритма и проводимости:
1. Кардиальные причины:
ИБС, в том числе инфаркт миокарда и нестабильная стенокардия
Сердечная недостаточность
Кардиомиопатия
Приобретённые пороки сердца
Врождённые пороки сердца
Миокардиты
Пролапс митрального клапана
2. Внесердечные причины:
заболевания бронхолегочной системы, центральной и периферической НС, патология ЖКТ
- лекарственные воздействия:
Сердечные гликозиды
Антиаритмические препараты (проаритмическое действие)
Диуретики
Симпатомиметикии другие
Электролитные нарушения:
Гипокалиемия
Гиперкалиемия
Гипомагниемия
Гиперкальциемия и другие
Токсические воздействия:
Курение
Наркотические вещества (в том числе алкоголь)
Тиреотоксикоз
Идиопатические аритмии
Разные заболевания, сопровождающиеся нарушением анатомической структуры сердца или происходящих в нем обменных процессов, вызывают различные по продолжительности и характеру виды аритмии, и установить диагноз может только врач, выводы которого основываются на клинико-электрокардиографических данных.
Классификация по виду нарушений ритма и проводимости:
1. Преждевременные комплексы (экстрасистолы и парасистолы):
1.1. Наджелудочковые;
1.2. Желудочковые;
2. Тахиаримии:
2.1. Наджелудочковые:
- синусовая тахикардия;
- синоатриальная реципрокная тахикардия;
- предсердная тахикардия;
- трепетание предсердий;
- фибрилляция предсердий;
- атриовентрикулярные тахикардии;
- атриовентрикулярные тахикардии с дополнительными путями проведения.
2.2. Желудочковые:
- желудочковые тахикардии;
- фибрилляция и трепетание желудочков.
3. Дисфункция синусового узла:
3.1. Синусовая брадикардия;
3.2. Синоатриальные блокады;
4. Нарушение атриовентрикулярной и желудочковой проводимости:
4.1. Атриовентрикулярные (АВ) блокады:
- АВ блокада I степени;
- АВ блокада II степени МобицI;
- АВ блокада II степени МобицII;
- АВ блокада IIIстепени.
4.2. Внутрижелудочковые блокады:
- Блокада левой ножки пучка Гиса (полная, неполная)
- Блокада правой ножки пучка Гиса (полная, неполная)
Вместе с тем, дискуссия об основаниях, которые следует положить в основу классификации аритмий, всё ещё продолжается в силу того, что за прошедшие уже более ста лет научного изучения аритмий сердца всё ещё не удалось достичь желаемого уровня эффективности проводимого лечения.
Методы обследования пациентов с аритмиями
Первым этапом в диагностике нарушений ритма и проводимости сердца является сбор жалоб и анамнеза, а также методы физикального обследования пациента.
Особенностью клинической картины аритмий является то, что проявления заболеваний могут широко варьировать от бессимптомного до тяжелого течения имеющихся симптомов. Наиболее распространенными жалобами пациента являются ощущение сердцебиения или перебоев в работе сердца. Наличие внезапного начала и прекращения приступа сердцебиения характерно для пароксизмальной тахикардии. Жалобами пациентов также могут быть выделение большого количества светлой мочи после завершения эпизода сердцебиения. Данный симптом наиболее характерен для пароксизмальной наджелудочковой тахикардии. Для пациентов с исходным органическим повреждением сердца, высокочастотными тахиаримиями или желудочковыми нарушениями ритма возможно появление одышки. Более того, при исходном наличии систолической функции сердца нередко наблюдаются головокружения, потеря сознания, синдром Морганьи-Адамса-Стокса. Такие же симптомы характерны для пациентов с брадиаритмиями, которые нередко являются единственными жалобами у таких больных. Вегетативные проявления в виде потливости, гиперемии лица, чувства страха более вероятны для пациентов с желудочковыи нарушениями ритма сердца.
Физикальное обследование больных с аритмиями направлено на выявление учащенного или замедленного, и/или неправильного ритма сердца методом пальпации артерий или аускультации сердца.
Наиболее информативным, позволяющим определить нозологическую форму аритмий, является метод обследования электрокардиографии (ЭКГ).
Регистрация ЭКГ возможна двумя методами – одномоментной записью или суточным мониторированием ЭКГ по Холтеру (Холтеровскоемониторирование – ХМ).
ЭКГ, записанная с использованием стандартных отведений, информативна в случае развития пароксизма нарушений ритма сердца или в случае персистирующего характера аритмий. В иных ситуациях показано проведение ХМ-ЭКГ.
Стандартным временем ХМ-ЭКГ является 24-часовая запись. Однако, возможен и более длительный анализ ЭКГ, составляющий 48 часов, выполняющийся в ситуациях с более редким появлением симптомов нарушений ритма сердца.
Диагностические возможности длительного анализа ЭКГ на сегодняшний день включают несколько методов регистрации:
1. событийные регистраторы для выявления причин симптомов:
наружные петлевые регистраторы (НПР);
имплантируемые петлевые регистраторы (ИПР).
2. дистанционная телеметрия.
НПР – типичные или модифицированные наружные устройства для ХМ-ЭКГ, позволяющие регистрировать ЭКГ по типу «петли» или «кольца», т.е. непрерывно записывая и удаляя фрагменты записи, если за истекшее время не произошла активация прибора пациентом.
ИПР – имплантируемые (подкожные) регистраторы с наличием микроэлементной кольцевой памятью, хранящая запись ЭКГ при активизации пациентом или свидетелем симптомов аритмии. Срок эксплуатации ИПР составляет до 36 месяцев.
Обычно НПР и ИПР используются при наличии редких симптомов аритмий (реже 1 раза в месяц), включая синкопальные состояния. Польза таких методов диагностики при синкопе является предметом дискуссии ряда исследователей. По результатам исследования Linzer M. etal, использование НПР было полезным у 25% респондентов, тогда как Schuchert Aetal в своем исследовании, длившимся 1 месяц, сделали вывод об отсутствии информативности выявления причин синкопальных состояний. Мета-анализ 9 исследований ИПР установили эффективность диагностики синкопе в 35% случаев среди обследованных пациентов.
Дистанционная телеметрия – метод регистрации ЭКГ, основанный на беспроводной передаче в сервисный центр с приборов холтеровского монитора по методу непрерывной 24-часовой записи или устройств ИПР или НПР.
Важно отметить, что наличие особых клинических ситуаций требует применения провокационных проб нарушения ритма сердца методом электрофизиологического исследования (ЭФИ). Суть метода заключается в том, чтобы с помощью электрического разряда разной мощности (пороги стимуляции), наносимых в области предсердий или желудочков, спровоцировать развитие аритмий и определить их происхождение.
Различают несколько методик проведения ЭФИ – инвазивное и неинвазивное (чреспищеводное).
Объем проведения инвазивного ЭФИ различен и зависит от тяжести течения аритмий, сопутствующих клинических состояниях больного и возможности доступа. Выделяют несколько вариантов установления электродов при выполнении инвазивного ЭФИ:
1. эндокардиальное (выполняется для диагностических целей в условиях стационара, без введения наркоза и, в большинстве случаев без премедикации);
2. эпикардиальное (выполняется во время операций на сердце);
3. комбинированное (по показаниям).
С помощью инвазивного (эпикардиального) ЭФИ возможно выполнение электрокардиостимуляции всех четырех камер сердца, а также области пучка Гиса и коронарного синуса.
Чреспищеводная электростимуляция сердца (ЧПЭС)получила более широкое распространение в клинической практике, ввиду того, что данный метод является менее травматичным и более безопасным при его проведении. В большинстве случаев электрический стимул наносится в область левого предсердия. При наличии специальных электродов (большей длинны) электрическое воздействие может быть оказано на левый желудочек.
Лечение высокочастотных нарушений ритма проводится антиаритмическими препаратами.
Классификация антиаритмических препаратов (EMVaughanWilliams)
Класс I. Блокаторы быстрых натриевых каналов (мембраностабилизирующие)
A. Препараты, умеренно замедляющие деполяризацию и реполяризацию (хинидин, прокаинамид, дизопирамид, аймалин).
B. Препараты, незначительно замедляющие деполяризацию и ускоряющие реполяризацию (лидокаин, мексилетин, токаинид, фенитоин).
C. Препараты, значительно замедляющие скорость деполяризации и минимально влияющие на реполяризацию (пропафенон, флекаинид,энкаинид, этацизин, алапинин).
Класс II. Блокаторы β-адренергических рецепторов без внутренней симпатомиметической активности (пропранолол, метопролол, атенолол, бетаксолол, бизопролол, невиболол, эсмолол).
Класс III. Препараты, замедляющие реполяризацию и действующие на калиевые каналы (амиодарон, соталол, ибутилид, дофетилид, азимилид, дронедарон).
Класс IV. Блокаторы кальциевых каналов (верапамил, дилтиазем).
Синусовая тахикардия регистрируется при учащении синусового ритма сердца более 90 уд/мин.
Источником генерации импульсов является синусовый узел – водитель ритма первого порядка. В связи с этим, синусовая тахикардия может быть проявлением физиологических реакций, возникающих в ответ на увеличение симпатического или уменьшения вагусного влияния, а также быть следствием компенсаторных механизмов при различных патологических явлениях кардиального или некардиального генеза, возникающих в организме (сердечная недостаточность, лихорадка, анемия, тиреотоксикоз и т.д.).
Диагностика
Методы диагностики включают выявление признаков синусовой тахикардии и, возможно, причин ее появления.
ЭКГ-признаки синусовой тахикардии:
- наличие нормального зубца Р;
- ЧСС более 90 уд/мин;
- одинаковое расстояние R-R (может быть различным в случае тахикардии при синусовой аритмии);
- неизмененные комплексы QRS.
ХолтеровскоемониторированиеЭКГ (ХМ ЭКГ) информативно для выявления периодов синусовой тахикардии, потенцирующих факторов для ее развития, определения диапазона ЧСС, сочетания с другими нарушениями ритма сердца. Характерным является постепенное начало учащения ритма сердца и окончания тахикардии.
Лечение. Синусовая тахикардия, как правило, не требует специфического лечения. Назначаемая терапия носит симптоматический характер, с целью достижения нормокардии. Важно подчеркнуть, что необходима коррекция основного состояния, вызвавшего синусовую тахикардию и/или устранение факторов, обуславливающих ее развитие.
Препаратами выбора при лечении синусовой тахикардии являются БАБ, с индивидуально подобранными дозировками – бисопролол (5-10 мг 1 раз в день), небивалол (5-10 мг 1 раз в день), метапрололасукцинат (50-100 мг 1 раз в день), а также возможно назначение других БАБ при отсутствии патологии сердечно-сосудистой системы.
У пациентов с ИБС показано назначение ингибиторов if-каналов, дополнительно к БАБ. Ингибиторы if-каналов (Кораксан) назначают по 5-7,5 мг 2 раза в сутки (утром, вечером).
В клинической практике с целью коррекции синусовой тахикардии может быть использован АК недигидроперидинового ряда – верапамил (40-80 мг 2-3 раза в сутки). Дозировку верапамила подбирают индивидуально, с учетом наличия или отсутствия артериальной гипертензии. Клинической нишей верапамила при синусовой тахикардии является наличие противопоказаний к назначению БАБ.
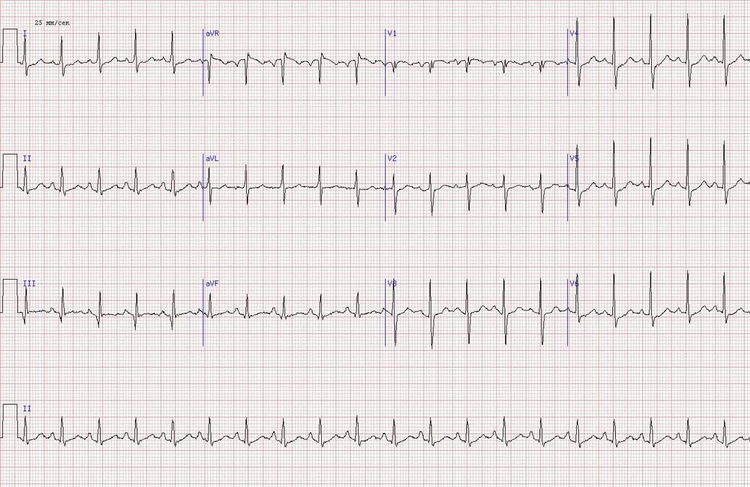
Синусовая тахикардия
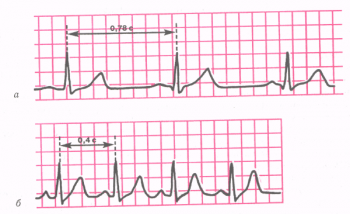
а – нормокардия, б – синусовая тахикардия
Предсердными тахикардиями называют нарушения ритма сердца, при которых эктопический участок генерации импульсов находится в предсердиях.
Диагностика предсердной тахикардии включает регистрацию одномоментной записи ЭКГ, ХМ-ЭКГ и ЭФИ.
ЭКГ-критерии предсердной тахикардии:
- наличие зубца Р перед каждым комплексом QRS измененной полярности и/или формы;
- наличие неизмененных комплексов QRS;
- R-R одинаковый;
- ЧСС – более 90 уд/мин, обычно 150-200 уд/мин.
ХМ-ЭКГ проводится с целью определения длительности течения пароксизмов предсердной тахикардии, их количества за период мониторирования, частотную характеристику, выявления инициирующего фактора их развития.
Метод ЭФИ может быть использован в качестве диагностики предсердной тахикардии, поскольку электростимуляция предсердий инициирует развитие эпизода аритмии. Также ЭФИ используют для купирования приступа тахикардии.
|
|
Фрагменты ЭКГ предсердной тахикардии
Купирование приступа предсердной тахикардии: вагусные пробы: Вальсальвы, Ашнера, массаж области каротидного синуса, ЭФИ, с целью нанесения разряда электрического тока и купирования приступа тахикардии, Прокаинамид (Новакаинамид) [в/в, струйно, медленно или капельно в дозе до 17 мг/кг (обычно 1000мг)], Пропафенон (в/в,струйно, в дозе 1мг/кг в течение 3-6 минут), Амиодарон (Кордарон) (в/в 450-600 мг).
Для профилактики приступов предсердной тахикардии: БАБ [Бисопролол (5-10 мг/сут), небивалол (5-10 мг/сут), метапрололасукцинат (50-100 мг/сут)], Пропафенон (150 мг 3 р/д), Аллапинин (25 мг 3 р/д), Этацизин (50 мг 3 р/д), Соталол (80 мг 2 р/д), Амиодарон [по схеме: 600 мг/сут (200 мг 3 р/д) – 1 неделя, 400 мг/сут (200 мг 2 р/д) – 1 неделя, 200-100 мг/сут длительно, возможно с перерывами (5 дней прием, 2 дня перерыв)].
При реферактерности к лечению предсердной тахикардии показано хирургическое лечение – радиочастотная аблация (деструкция очага АВ-узловой тахикардии).
Узловые тахикардиями (АВ-уловые тахикардии) называют нарушения ритма сердца, при которых эктопический участок генерации импульсов находится в АВ узле.
Диагностика АВ-узловой тахикардии включает регистрацию одномоментной записи ЭКГ, ХМ-ЭКГ и ЭФИ.
ЭКГ-критерии АВ-узловой тахикардии:
- отсутствие зубца Р перед каждым комплексом QRS;
- наличие неизмененных комплексов QRS;
- R-R одинаковый;
- ЧСС – более 90 уд/мин, обычно 150-200 уд/мин.
ХМ-ЭКГ проводится с целью определения длительности течения пароксизмов, их количества за период мониторирования, частотную характеристику, выявления инициирующего фактора их развития.
Метод ЭФИ может быть использован в качестве диагностики АВ-узловой тахикардии, поскольку электростимуляция предсердий инициирует развитие эпизода аритмии в АВ-узле. Также ЭФИ используют для купирования приступа тахикардии.
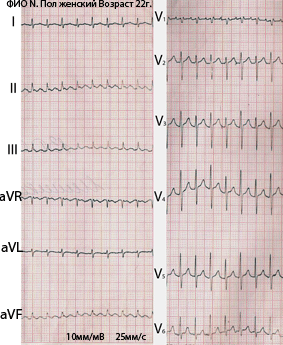
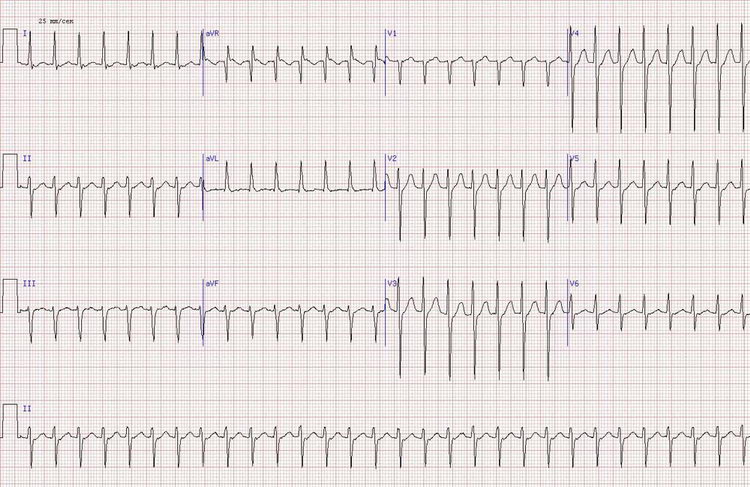
АВ-узловая тахикардия
Купирование приступа АВ-уловой тахикардии: вагусные пробы: Вальсальвы, Ашнера, массаж области каротидного синуса, ЭФИ, с целью нанесения разряда электрического тока и купирования приступа тахикардии, Прокаинамид (Новакаинамид) [в/в, струйно, медленно или капельно в дозе до 17 мг/кг (обычно 1000мг)], Пропафенон (в/в,струйно, в дозе 1мг/кг в течение 3-6 минут), Амиодарон (Кордарон) (в/в 450-600 мг).
Для профилактики приступов АВ-узловой тахикардии: БАБ [Бисопролол (5-10 мг/сут), небивалол (5-10 мг/сут), метапрололасукцинат (50-100 мг/сут)], Пропафенон (150 мг 3 р/д), Аллапинин (25 мг 3 р/д), Этацизин (50 мг 3 р/д), Соталол (80 мг 2 р/д), Амиодарон [по схеме: 600 мг/сут (200 мг 3 р/д) – 1 неделя, 400 мг/сут (200 мг 2 р/д) – 1 неделя, 200-100 мг/сут длительно, возможно с перерывами (5 дней прием, 2 дня перерыв)].
При реферактерности к лечению АВ-узловой тахикардии показано хирургическое лечение – радиочастотная аблация (деструкция очага АВ-узловой тахикардии).
Желудочковые тахикардии (ЖТ) – нарушения ритма сердца, характеризующиеся наличием эктопического очага, находящегося в различных участках миокарда желудочков и запускающего механизм повторного входа волны возбуждения (re-entry).
Важным диагностическим признаком наиболее тяжелых ЖТ (прогностически неблагоприятных) является наличие выраженной клинической картины, проявляющейся признаками острой левожелудочковой недостаточности, обмороками, остановкой кровообращения.
Диагностика
ЭКГ-признаки пароксизмальной мономорфной ЖТ:
- отсутствие зубца Р;
- расширенные (измененные, абберантные) комплексы QRS;
- интервалы R-R одинаковые.
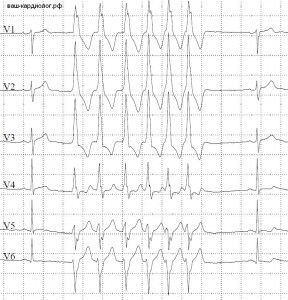
Пароксизм желудочковой тахикардии
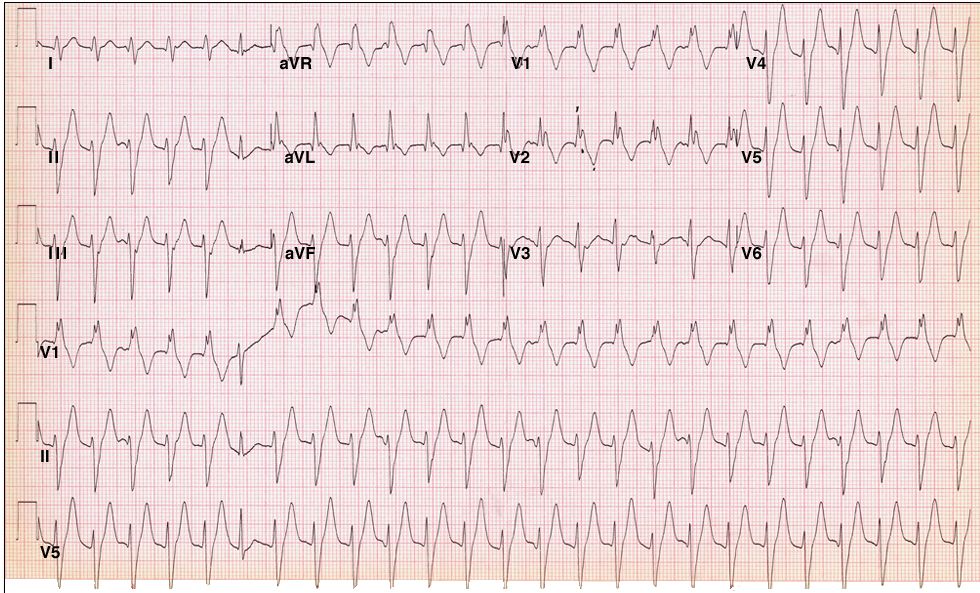
Желудочковая тахикардия
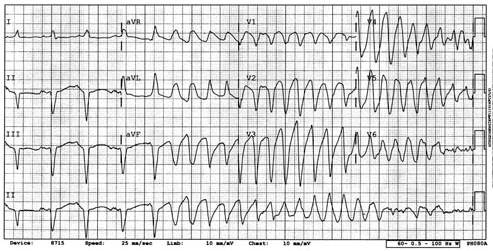
Желудочковая тахикардия
Для выявления пароксизмальной формы ЖТ методом диагностики может являться ХМ-ЭКГ.
Для купирования приступов ЖТ может быть использованы препараты: верапамил[в/в, струйно, в течение 1-2 мин – по 2-4 мл 0,25% раствора (5-10 мг)], лидокаин (в/в струйно 50–100 мг, затем капельно со скоростью 1-4 мг/мин), прокаиномид (500-1000 мг однократно в/в медленно), пропафенон (2 мг/кг в/в в течение 10 мин или 450-600 мг внутрь), амиодарон (в/в, 600-1200 мг/сут), аденозин (в/в, болюсно – 6 мг, максимальная суточная доза – 12 мг), соталол (в/в, суточная доза – 1,5 мг/кг).
Для профилактики приступов ЖТ:Этацизин 50 мг 3 р/д, Аллапинин 25 мг 3 р/д, Пропафенон 150 мг 3 р/д, Амиодарон [по схеме: 600 мг/сут (200 мг 3 р/д) – 1 неделя, 400 мг/сут (200 мг 2 р/д) – 1 неделя, 200-100 мг/сут длительно, возможно с перерывами (5 дней прием, 2 дня перерыв)], Соталолпо 80 мг 2 раза в сутки, поддерживающая – 160-320 мг/сут.
При рефрактерных к терапии ЖТ показано хирургическое лечение – радиочастотная аблация (деструкция очага ЖТ), установка кардиовертерадефибрилятора.
Трепетание предсердий – нарушение ритма сердца, характеризующееся наличием эктопического очага высокой генерации импульсов, достигающей 200-400 ударов в минуту.
Необходимо отметить, что циркуляция волны возбуждения, возникающая в эктопическом очаге, имеет большую траекторию, охватывающую крупные анатомические области правого или левого предсердий, т.е. механизмом трепетания предсердий является макро-re-entry. Данная особенность имеет важное значение в понимании ЭКГ-признаков трепетания предсердий.
Важно обратить внимание, что проведение возбуждения на желудочки не соответствует частоте сокращения предсердий, за счет блокирования импульсов в области АВ-соединения, т.е. формирования АВ-блокады.
Исходя из частоты сокращения желудочков различают бради-, нормо- и тахисистолическую форму трепетания предсердий.
Трепетание предсердий, в большинстве случаев, является правильной формой нарушения ритма, т.Е. Кратность ав-проведения является одинаковой (с равными интервалами r-r).
Важно отметить, что трепетание предсердий имеет пароксизмальную и персистирующую (постоянную) формы.
Диагностика
Диагностика трепетания предсердий включает регистрацию одномоментной записи ЭКГ, ХМ-ЭКГ и ЭФИ.
ЭКГ-признаки трепетания предсердий:
- отсутствие зубца Р;
- наличие пилообразных волн трепетания – волны F;
- комплекс QRS не изменен;
- одинаковый интервал R-R.
В заключении ЭКГ необходимо указать проведение предсердной импульсации на желудочки, которое определяется по количеству положительных пиков волн F (2:1, 3:1 и т.д.).
ХМ-ЭКГ выполняют с целью определения формы трепетания предсердий, в случае пароксизмальной формы – его регистрация, продолжительность и, возможно, инициирующие факторы.
С помощью ЭФИ возможна провокация эпизода трепетания предсердий, с целью выявления данного нарушения ритма, а также применение ЭФИ возможно для купирования пароксизма трепетания предсердий.
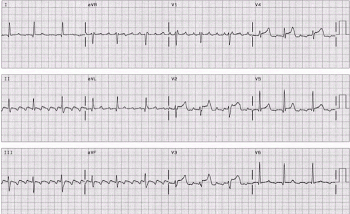
Трепетание предсердий, проведение 3:1
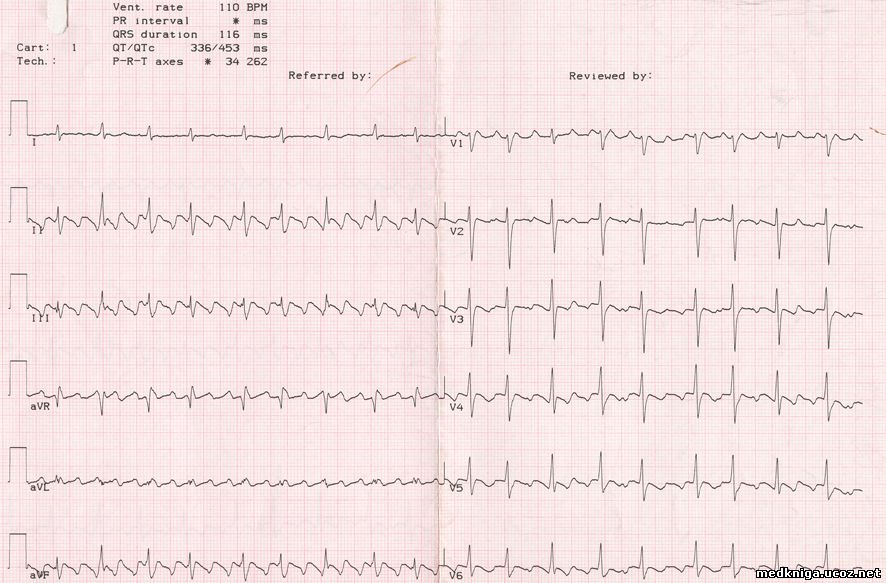
Трепетание предсердий, проведение 3:1, 2:1
Лечениетрепетания предсердий состоит из нескольких стратегий:
- восстановление синусового ритма (по показаниям) (Амиодарон - в/в капельно, 600 - 1200 мг/сут);
- контроль ЧСС (БАБ: бисопролол, небиволол, метапрололасукцинат);
- профилактика тромбоэмболий (варфарин – 2,5-5 мг до МНО = 2-3, дабигатранаэтексилат (Прадакса) - 150 мг 2 раза в сутки, ривароксабан (Ксарелто) - 20 мг 1 раз в сутки, апиксабан (Эликвис) - 5 мг 2 раза в сутки).
Для купирования приступа трепетания предсердий возможно использование электрической кардиоверсии.
Методом хирургического лечения трепетания предсердий является радиочастотная катетернаяаблация эктопического очагав правом предсердии в зоне перешейка.
Фибрилляция предсердий является одной из наиболее распространенных форм нарушений ритма сердца.
Фибрилляция предсердий – нарушение ритма сердца, характеризующееся хаотической электрической активностью предсердий с частотой 300-700 уд/мин.
Отличием фибрилляции от трепетания предсердий являются различные механизмы данных тахиаритмий. Если при трепетании предсердий эктопический очаг возбуждения миокарда предсердий является макро-re-entry, то основой фибрилляции предсердий – множественные очаги микро-re-entry, при которых волны возбуждения движутся по неопределенному, изменяющемуся пути. Данные механизмы положены в основу понимания ЭКГ-критериев фибрилляции предсердий.
В зависимости от возможности АВ-проведения патологических импульсов из предсердий различают тахи-, нормо-, брадисистолическую формы фибрилляции предсердий.
Важно отметить еще одну особенность механизма формирования фибрилляции предсердий – высокий риск тромбоэмболических осложнений, обусловленный высокочастотным, хаотичным сокращением миокарда левого предсердия, создающего нарушение турбулентности потока крови.
При нерегулярном пульсе следует всегда подозревать фибрилляцию предсердий, однако для подтверждения диагноза необходимо зарегистрировать ЭКГ.
В диагностике фибрилляции предсердий применяют ЭКГ в стандартных отведениях, ХМ-ЭКГ, ЭФИ.
ЭКГ-критерии фибрилляции предсердий:
- нерегулярный ритм, интервалы R-R не имеют одинаковой продолжительности;
- отсутствие зубцов Р;
- наличие множественных волн фибрилляции – волн f, характеризующиеся мелкочастотными колебаниями от изоэлектрической линии;
- комплекс QRS не изменен.
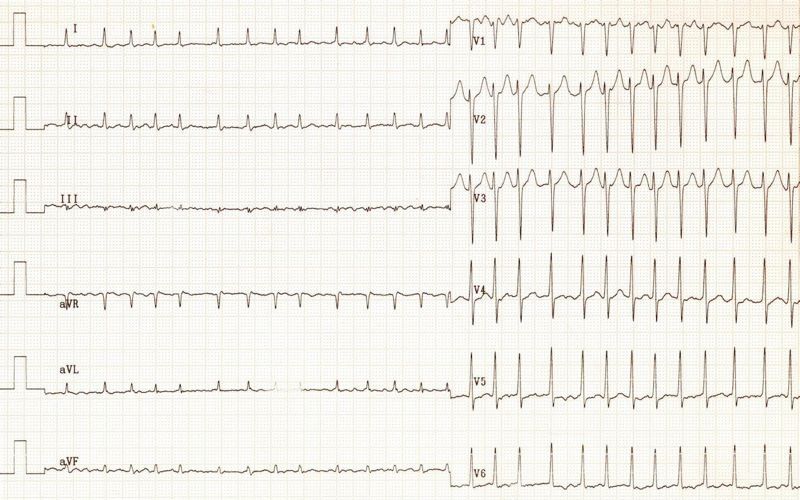
Фибрилляция предсердий
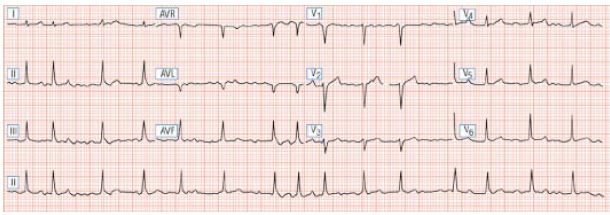
Фибрилляция предсердий
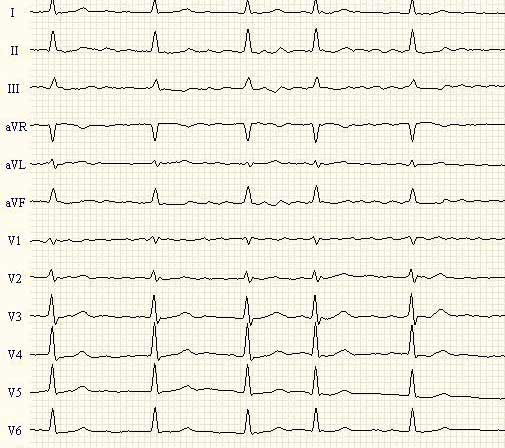
Фибрилляция предсердий
Необходимо отметить, что по продолжительности фибрилляции предсердий различают впервые выявленную, пароксизмальную, персистирующую, длительно персистирующую, постоянную формы.
Лечениефибрилляции предсердий аналогично трепетанию предсердий, а именно состоит из нескольких стратегий:
- восстановление синусового ритма (по показаниям) (Амиодарон - в/в капельно, 600 - 1200 мг/сут);
- контроль ЧСС (БАБ: бисопролол, небиволол, метапрололасукцинат);
- профилактика тромбоэмболий (варфарин – 2,5-5 мг до МНО = 2-3, дабигатранаэтексилат (Прадакса) - 150 мг 2 раза в сутки, ривароксабан (Ксарелто) - 20 мг 1 раз в сутки, апиксабан (Эликвис) - 5 мг 2 раза в сутки).