
304-_Organicheskaya_khimia_Chernykh_V_P_i_dr_Kh__2007_-776s
.pdf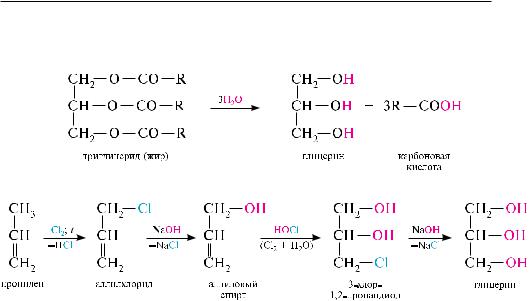
ГИДрОКСИлЬнЫе ПрОИЗВОДнЫе УГлеВОДОрОДОВ. ПрОСТЫе ЭФИрЫ
351
кислотным или щелочным гидролизом жиров (сложных эфиров глицерина и высших гомологов карбоновых кислот) может быть получен наиболее важный представитель триолов — глицерин (1,2,3-пропантриол):
в промышленности синтез глицерина осуществляют из пропилена по схеме:
22.2.2. ФИЗИЧеСКИе СВОЙСТВа
низшие члены гомологического ряда диолов представляют собой вязкие жидкости, высшие — кристаллические вещества. Жидкие гликоли имеют большую плотность и более высокие температуры плавления и кипения, чем одноатомные спирты; хорошо растворяются в воде. трехатомные спирты — вязкие жидкости или трудно кристаллизующиеся твердые вещества. Вязкость, растворимость в воде,
температуры плавления и кипения гидроксильных производных алифатических углеводородов увеличиваются в ряду: одноатомные спирты < гликоли < глицерины. такая зависимость является следствием усиления ассоциации молекул за счет образования межмолекулярных водородных связей.
отличительной особенностью гидроксильных производных углеводородов с несколькими он-группами является их сладковатый вкус, как правило, усиливающийся с увеличением числа гидроксильных групп в молекуле.
22.2.3. хИмИЧеСКИе СВОЙСТВа
двухатомные спирты вступают в те же реакции, что и одноатомные, с той лишь разницей, что они могут протекать с участием одной или двух гидроксильных групп. еще большее разнообразие продуктов возможно для реакций с участием трех- и полиатомных спиртов. Глицерин образует три ряда производных: моно-, ди- и тризамещенные продукты. При этом для моно- и дизамещенных производных возможны структурные изомеры, обусловленные различным положением заместителей.
Образование алкоголятов. Гликоли являются более сильными он-кислотами,
чем одноатомные спирты, поэтому они образуют алкоголяты (гликоляты) не только со щелочными металлами, но и с другими активными металлами (Al, Mg и др.), а также со щелочами и гидроксидами тяжелых металлов. Повышение кислотных
Глава 22
352
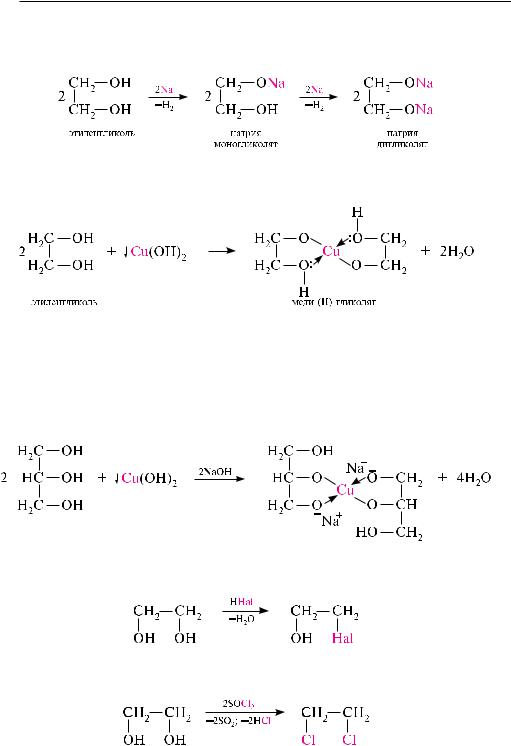
свойств гликолей связано с электроноакцепторным влиянием одной гидроксильной группы на другую (–I-эффект). При взаимодействии с активными металлами безводные гликоли образуют неполные и полные гликоляты:
-Гликоли реагируют с меди (II) гидроксидом с образованием меди (II) гликолята — комплексного соединения синего цвета:
с увеличением числа гидроксильных групп в молекуле кислотные свойства соединения усиливаются. так, глицерин, по сравнению с этиленгликолем, имеет более выраженные кислотные свойства. в водном растворе щелочи глицерин легко образует моноглицераты [HOCH2—CH(ONa)—CH2OH]. При взаимодействии с меди (II) гидроксидом глицерин образует меди (II) глицерат (раствор синего цвета). хорошая растворимость глицератов в воде обьясняется их комплексным строением:
Взаимодействие с галогеноводородами. При взаимодействии гликолей с галоге-
новодородами (HCl или HBr) образуются хлорили бромгидрины:
вторая гидроксильная группа замещается труднее (лучше использовать PCl5
или SOCl2):
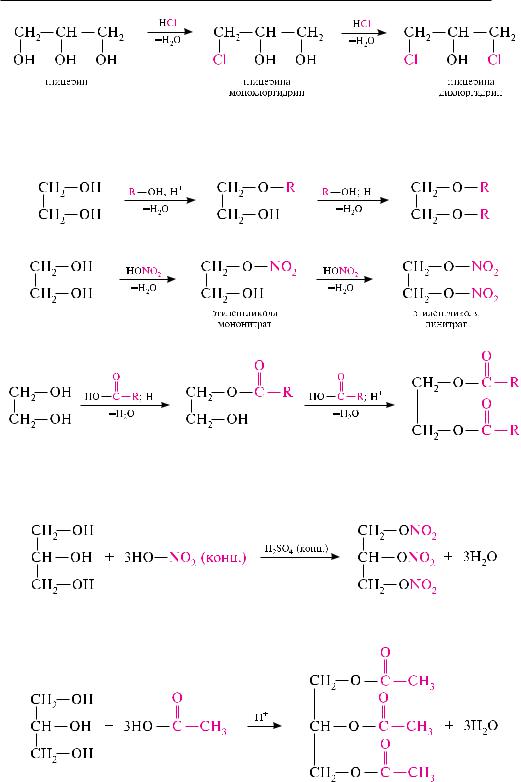
При взаимодействии глицерина с галогеноводородами образуется смесь моно- и дигалогенозамещенных продуктов:
ГИДрОКСИлЬнЫе ПрОИЗВОДнЫе УГлеВОДОрОДОВ. ПрОСТЫе ЭФИрЫ
353
Образование простых и сложных эфиров. При взаимодействии гликолей со спиртами, минеральными или органическими кислотами образуется два ряда производных:
а) неполные и полные простые эфиры
б) неполные и полные сложные эфиры
для глицерина в этом случае образуется три ряда производных. При взаимодействии глицерина с концентрированной азотной кислотой в присутствии концентрированной серной кислоты получают полный азотнокислый эфир гли-
церина — глицерина тринитрат (нитроглицерин):
аналогично в жестких условиях получается и полный уксуснокислый эфир глицерина — глицеринтриацетат:
ГИДрОКСИлЬнЫе ПрОИЗВОДнЫе УГлеВОДОрОДОВ. ПрОСТЫе ЭФИрЫ
355
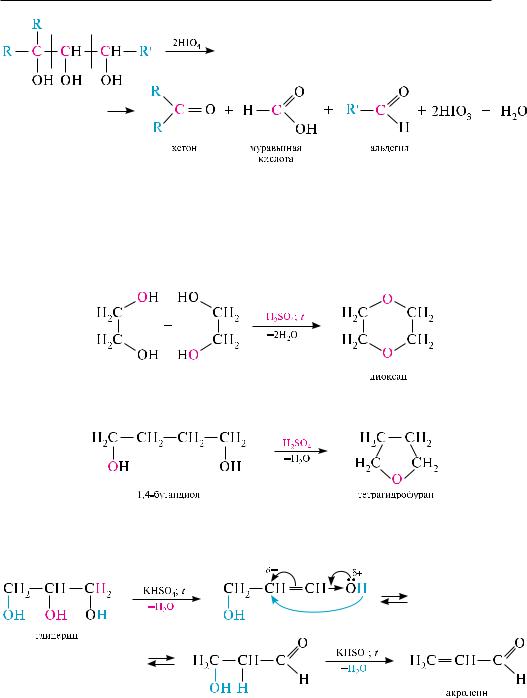
Дегидратация гидроксильных производных с несколькими группами Он. Под действием водоотнимающих реагентов гликоли, как и одноатомные спирты, подвергаются внутримолекулярной или межмолекулярной дегидратации. направление дегидратации зависит от условий проведения реакции.
так, при нагревании этиленгликоля в присутствии концентрированной серной кислоты происходит межмолекулярная дегидратация, и образуется циклический простой диэфир — диоксан:
для 1,4- и 1,5-диолов возможна внутримолекулярная дегидратация с образованием пяти- и шестичленных циклических эфиров:
Глицерин при нагревании с калия гидросульфатом или другими водоотнимающими средствами подвергается внутримолекулярной дегидратации с образованием непредельного альдегида — акролеина:
акролеин (акриловый альдегид) представляет собой жидкость с едким удушливым запахом.
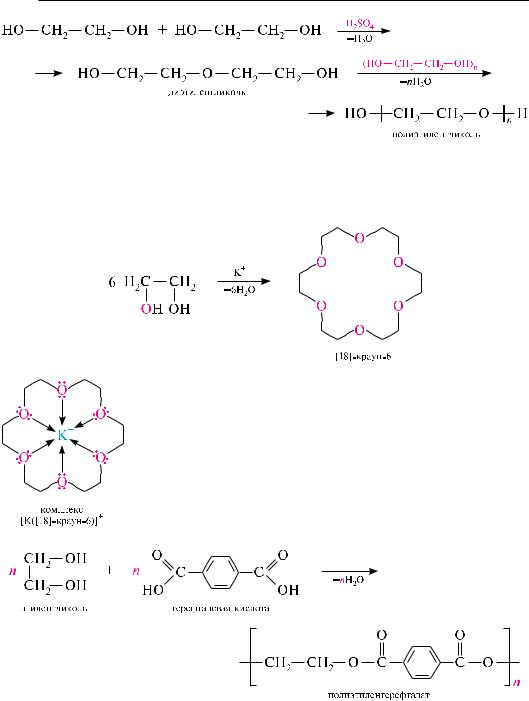
Поликонденсация двухатомных спиртов. Молекулы этиленгликоля в кислой среде вступают в реакцию поликонденсации с образованием полиэфира — полиэтиленгликоля:
Глава 22
35
Полиэтиленгликоль с молекулярной массой до 400 применяется в фармации в качестве растворителя лекарственных веществ, основы для мазей, а также как связывающее вещество в производстве таблеток.
Поликонденсация этиленгликоля в щелочной среде приводит к образованию краун-эфиров (см. с. 385).
важным свойством краун-эфиров является способность образовывать устойчивые липофильные комплексы с катионами щелочных и щелочноземельных металлов. они используются для улучшения растворимости неорганических солей в органических растворителях, в качестве межфазных катализаторов, экстрагентов, как лекарственные препараты, антидоты, пестициды и т. д.
При поликонденсации этиленгликоля с терефталевой кислотой образуется полиэфир — полиэтилентерефталат, который используется для изготовления синтетического волокна — лавсана:
22.2.4. ИДенТИФИКаЦИя ДИОлОВ И ТрИОлОВ
обнаружить гидроксильные группы в диолах и триолах можно по образованию окрашенного в синий цвет раствора комплексной соли меди (см. с. 352).
ГИДрОКСИлЬнЫе ПрОИЗВОДнЫе УГлеВОДОрОДОВ. ПрОСТЫе ЭФИрЫ
357
для обнаружения глицерина может быть использована реакция дегидратации с образованием акролеина — вещества с резким раздражающим запахом
(см. с. 355).
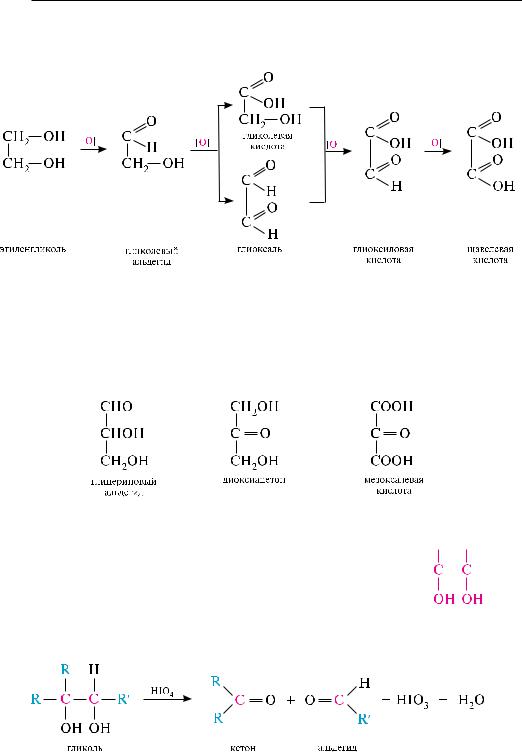
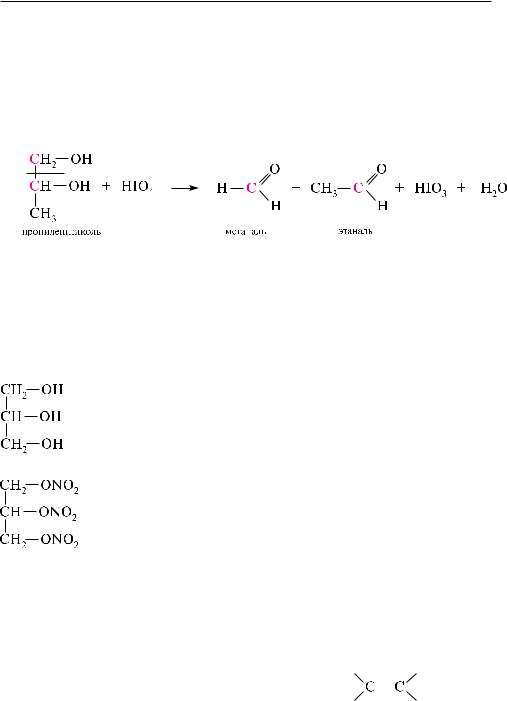
для идентификации -гликолей используют реакцию окисления с йодной кислотой HIO4 (гликольное расщепление) (см. с. 354). При окислении происходит разрыв химической связи между углеродными атомами, связанными с группами
—он, и образуются соответствующие карбонильные соединения, по которым можно установить место расположения диольного фрагмента молекулы:
22.2.5. ОТДелЬнЫе ПреДСТаВИТелИ. ПрИмененИе
Этиленгликоль (1,2-этандиол) но–сн2–сн2–он. бесцветная вязкая жидкость, т. кип. 197,6 °с, т. пл. –11,5 °с, d420 = 1,113. Гигроскопичен, смешивается с водой и этанолом. сильно понижает температуру замерзания воды и используется для приготовления антифриза. очень токсичен. широко используется для получения синтетических волокон.
Глицерин (1,2,3-пропантриол). бесцветная сиропообразная жидкость без запаха, со сладким вкусом, т. пл. 18 °с, т. кип. 290 °с (с разложением). Гигроскопичен, смешивается с водой и этанолом в любых соотношениях. Применяется в качестве основы для мазей
и паст, добавки к мылам. в больших количествах глицерин используется для получения нитроглицерина.
нитроглицерин (глицерина тринитрат). тяжелая маслянистая жидкость со сладковатым жгучим вкусом, при нагревании или ударе взрывается, используется для изготовления динамита. в виде разбавленных спиртовых растворов нитроглицерин оказывает сосудорасширяющее действие и применяется в медицине при стенокардии. выпускается также в таблетках с содержанием 0,0005 г вещества.
22.3. енОлы
Гидроксильные производные углеводородов, содержащие он-группу при двойной углерод-углеродной связи, называют енолами.
в названиях енолов суффикс -ен обозначает |
|
двойную связь, |
|
||
|
||
а -ол — гидроксильную группу). |
|
|
формально енолы можно отнести к ненасыщенным спиртам, у которых он-группа связана с углеродным атомом в sp2-гибридизации. однако по своим свойствам эти гидроксипроизводные углеводородов настолько отличаются от ненасыщенных спиртов с он-группой при sp3-гибридизованном атоме углерода, что рассмотреть их целесообразно отдельно.
Глава 22
358
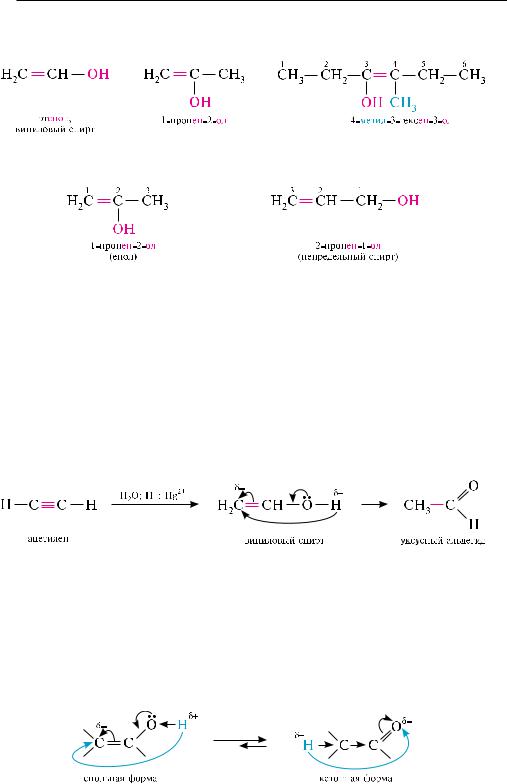
названия енолов по систематической номенклатуре IUPAC образуют из названия алкена, к которому добавляют суффикс -ол:
рассмотрим два изомерных непредельных гидроксильных производных углеводорода:
Эти два изомера очень существенно отличаются по своим физическим и химическим свойствам. Первое вещество относится к енолам (гидроксильная группа при двойной углерод-углеродной связи), а второе — к непредельным спиртам (алкенолам) (гидроксильная группа находится при атоме углерода в sp3-гибриди- зации).
енолы, в отличие от непредельных спиртов, являются неустойчивыми соеди-
нениями. Попытки получить соединения с енольной структурой 
 приводят к соединениям, содержащим карбонильную группу
приводят к соединениям, содержащим карбонильную группу 

 .
.
так, при гидратации ацетилена в качестве промежуточного вещества образуется виниловый спирт (енол), который изомеризуется в уксусный альдегид:
Это свойство енолов отражено в правиле Эльтекова-Эрленмейера.
Соединения, у которых гидроксильная группа расположена при углеродном ато- ме, образующем кратную углерод-углеродную связь, неустойчивы и изомеризуются в соответствующие карбонильные соединения — альдегиды или кетоны.
Причина неустойчивости енолов вызвана миграцией протона от атома кислорода он-группы к соседнему атому углерода, образующему двойную связь. такое явление называется прототропной изомерией, или таутомерией. При этом происходит изомеризация енольной формы в кетонную:

Глава 22
3 0
Поливиниловый спирт применяется в производстве искусственных волокон, лекарственных средств. в частности, он используется при изготовлении саморассасывающихся хирургических ниток, крове- и плазмозаменителей.
22.4. аМинОсПирТы
Аминоспиртами называют производные углеводородов, содержащие аминогруппу (N-алкил- или N,N-диалкиламиногруппу) и спиртовой гидроксил.
устойчивыми являются аминоспирты, у которых аминогруппа и спиртовый гидроксил расположены у разных атомов углерода. для названия аминоспиртов чаще применяют заместительную номенклатуру, согласно которой их называют как производные спиртов, содержащие в качестве заместителя аминогруппу. Положение аминогруппы указывают цифрами или буквами греческого алфавита:
если молекула аминоспирта содержит в своем составе две или три гидроксиалкильные группы, связанные через атом азота, в этом случае за основу берут название амина:
изомерия спиртов обусловлена теми же причинами, что и у дизамещенных углеводородов.
аминоспирты представляют собой ассоциированные соединения, в которых межмолекулярные водородные связи образованы с участием аминогрупп и спиртовых гидроксилов:
