
- •Предмет, задачи общей и неорганической химии. Роль химии в естественных науках.
- •Основные понятия химии
- •Основные понятия химии.
- •Основные стехиометрические законы.
- •Газовые законы: г. Люссака, Авогадро, объединенный газовый закон.
- •Строение атома; развитие учения о строении атома; модели Томсона, Резерфорда, Бора.
- •Характеристика основных квантовых чисел.
- •Важнейшие классы и номенклатура неорганических веществ.
- •Периодический закон и периодическая система элементов.
- •Ковалентная химическая связь. Способы образования ковалентной связи. Основные характеристики.
- •Геометрия структур с ковалентным типом связи (гибридизация sp, sp2, sp3)
- •Метод валентных связей и метод молекулярных орбиталей.
- •Ионная и металлическая связь.
- •Межмолекулярное взаимодействие. Водородная связь.
- •Кристаллическое, жидкое и аморфное состояние веществ.
- •Скорость химических реакций. Константа скорости и ее физические свойства
- •Влияние температуры на скорость химических реакций. Основные положения теории активации Аррениуса.
- •Катализ. Влияние катализаторов на скорость химических реакций.
- •Необратимые и обратимые реакции. Принцип Ле Шателье.
- •Дисперсные системы и их характеристика.
- •3. По агрегатному состоянию дисперсионной среды и дисперсной фазы.
- •Способы выражения концентрации растворов.
- •Энергетика химических связей. Характеристика систем. Функции состояния.
- •Внутренняя энергия. Энтальпия и энтропия.
- •Энергия Гиббса.
- •Закон Генри. Законы Рауля.
- •Осмотическое давление. Закон Ван-Гоффа.
- •Особенности растворов электролитов. Основные положения электролитической диссоциации.
- •Буферные растворы и их характеристика. Уравнение Гендерсона-Хассельбаха.
- •Ионное произведение воды. Водородный показатель.
- •Произведение растворимости. Реакции обмена в растворах электролитов.
- •Гидролиз солей. Количественные характеристики гидролиза.
- •Теория овр. Важнейшие окислители и восстановители. Метод электронного баланса.
- •Ионно-электронный метод (метод полуреакций).
- •Классификация овр.
- •Электрохимические процессы. Электронный потенциал. Водородный электрод.
- •Электрохимический ряд напряжения металлов. Уравнение Нернста.
- •Гальванический элемент и его влияние на протекание овр.
- •Электролиз растворов и расплавов.
- •Комплексные соединения. Номенклатура и классификация.
- •Константа устойчивости и константа неустойчивости (характеристика кс)
Теория овр. Важнейшие окислители и восстановители. Метод электронного баланса.
Положения теории ОВР:
Окислением называется процесс отдачи электронов атомом, молекулой или ионом. При окислении степень окисления повышается.
Восстановлением называется процесс присоединения электронов атомом, молекулой или ионом. При восстановлении степень окисления понижается.
Атомы, молекулы или ионы, отдающие электроны называются восстановителями. Во время реакции они окисляются. Атомы, молекулы или ионы, присоединяющие электроны, называются окислителями. Во время реакции они восстанавливаются.
Окисление всегда сопровождается восстановлением, и наоборот, восстановление всегда связано с окислением
Ме в свободном состоянии – только окислители
Не Ме (искл F) – в свободном виде как окислители, так и восстановители
К числу сильных окислителей, широко используемых на практике, относятся галогены (Fe2, Cl2, Br2, I2), оксид марганца Mn+4O2, перманганат калия KMn+7O4, манганат калия K2Mn+6O4, оксид хрома (хромовый ангидрид) Cr+6O3, хромат калия K2Cr+6O4, бихромат калия K2Cr2+6O7, азотная кислота HN+5O3 и ее соли, кислород О2, озон О3, перекись водорода Н2О2, концентрированная серная кислота Н2S+6О4, оксид меди (II) Сu+2О, оксид серебра Ag2+1O, оксид свинца Рb+4О2, гипохлориты (например, NaCl-1O) и другие соединения.
Щелочные и щелочноземельные металлы являются сильными восстановителями. К числу других восстановителей относятся: водород, углерод, оксид углерода С+2О, сероводород Н2S-2, оксид серы S+4О2, сернистая кислота Н2S+4О3 и ее соли, галогенводороды (кроме HF), хлорид олова (II) Sn+2Cl2, сульфат железа (II) Fe+2SO4.
Суть метода электронного баланса заключается в:
Подсчете изменения степени окисления для каждого из элементов, входящих в уравнение химической реакции
Элементы, степень окисления которых в результате произошедшей реакции не изменяется - не принимаются во внимание
Из остальных элементов, степень окисления которых изменилась - составляется баланс, заключающийся в подсчете количества приобретенных или потерянных электронов
Для всех элементов, потерявших или получивших электроны (количество которых отличается для каждого элемента) находится наименьшее общее кратное
Найденное значение и есть базовые коэффициенты для составления уравнения.
![]()
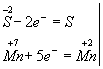
5Н2S + 2КМnО4 + ЗН2SО4 = 5S + 2МnSО4 + К2SО4 + 8Н2О
Ионно-электронный метод (метод полуреакций).
Классификация овр.
Межмолекулярные – в ходе которых окислитель и восстановитель находятся в разных веществах:
MnO2 + 4HCl = MnCl2 + Cl2 + 2H2O
Внутримолекулярные – в ходе которых окислитель и восстановитель находятся в одном веществе.
KClO3 = KCl + O2
Диспропорционирование – атомы одного и того же элемента являются и окислителем и восстановителем.
Cl2 + H2O = HCl + HClO
