
экзамены и коллоквиумы / Ответы на вопросы к коллоквиуму 2
.pdf
ёВопросы
1. Термодинамическая система (ТС)
2. Термодинамические процессы
3. Уравнение состояния идеального газа
4. Теплота и работа, внутренняя энергия.
5. Первое начало термодинамики
6. Теплоемкость
7. Уравнение Майера
8. Адиабатический процесс
9. Теплота и работа при изопроцессах
10. Второе начало термодинамики
11. Второе начало термодинамики
12. Третье начало термодинамики
13. Распределение Максвелла
14. Распределение энергии по степеням свободы
15. Теплоемкость многоатомных газов
16. Распределение Максвелла для компонент импульса
17. Распределение Больцмана
18. Распределение Максвелла-Больцмана
19. Фермионы и бозоны: распределение Бозе-Эйнштейна
20. Фермионы и бозоны: распределение Ферми-Дирака

2. Задачи тепловых машин (формула и формулировка)
Задача тепловой машины – совершение работы Ао над внешними телами за счет подведённого тепла Qо, в течении каждого кругового процесса.
3. Вечный двигатель 1-го, 2-го и 3-го рода
Вечный двигатель 1-го рода – тепловая машина, совершающая работу над внешними телами за цикл большую, чем подведенное к системе количество тепла. НЕВОЗМОЖЕН.
Вечный двигатель 2-го рода – тепловая машина, способная совершать работу без теплообмена с холодильником . НЕВОЗМОЖЕН.
Вечный двигатель 3-го рода – тепловая машина, температура холодильника которой Т2 = 0 К
4. Задачи тепловой машины, холодильной машины и теплового насоса
Задача теплового насоса – передача тепла Q1 к горячему телу за счёт работы А вн. сил над ней.
Задача холодильной машины – передача тепла Q2 от холодного тела за счёт работы А вн. сил над ней. 
5. Схема тепловой машины
6. Что позволяют вычислить распределения Максвелла, Больцмана и Максвелла-Больцмана ?
Распределение Максвелла позволяет вычислить элементарное количество частиц идеального газа, имеющих компоненты скорости/импульса в элементарном диапазоне: от pi до pi+dpi
Распределение Больцмана позволяет вычислить элементарное количество частиц идеального газа, находящихся в элементарном объёме в потенциальном поле.
Распределение Максвелла-Больцмана позволяет вычислить элементарное количество частиц идеального газа, находящихся в элементарном объёме в потенциальном поле и имеющих компоненты импульса в элементарном диапазоне: от pi до pi+dpi
7. Постулат Л. Де Бройля (формула и формулировка)
Любую микрочастицу можно моделировать волновым процессом с длиной волны h – постоянная Планка
р – относительный импульс микрочастицы (отн. объекта, с которым частица взаимод-т)

Вопросы к коллоквиуму № 2 для студентов 1-го курса
1. Термодинамическая система (ТС)
- любой воображаемый объём пространства, которому прописаны все термодинамические параметры (P,V,T и т.д.) данного тела.
2. Термодинамические процессы (определение ТС, Уравнение состояния, термодинамический процесс, равновесный термодинамический процесс, изопроцесс)
Уравнение состояния – уравнение, устанавливающее взаимосвязь ТП для РТС изучаемой ТС.
Равновесное термодинамическое состояние (РТС) – состояние ТС, при котором она должна бесконечно медленно изменять своё состояние с течением времени так, чтобы значение любого ТП в каждой точке объема ТС было равно его среднему значению по всему объему.
Термодинамический процесс (ТПр) – процесс в ТС, сопровождаемый изменением хотя бы 1 ТП.
Равновесный термодинамический процесс (РТПр) – процесс, при котором ТС бесконечно медленно проходит непрерывный ряд бесконечно близких РТС.
Изопроцесс – РТПр, происходящий в ТС с постоянной массой, при условии, что один ТП данной системы остаётся неизменным.
3.Уравнение состояния идеального газа – ур-е Менделеева-Клапейрона для идеального газа.
Идеальный газ – ТС, состоящая из очень большого количества материальных точек, которые взаимодействуют м/у собой только механически.
P,V,T – ТП, давление, объём и абсолютная температура и. газа m, M - масса и молярная масса и. газа
R – универсальная газовая постоянная.
4.Теплота и работа, внутренняя энергия.
Кол-во тепла – общее кол-во энергии, переданной ТС внешними телами при теплообмене.
Работа, совершённая над системой – кол-во энергии, переданное ТС внешними телами за счёт их силового взаимодействия на ТС.
Работа расширения – работа, которую система производит против внешних сил, при РТПр. 
Внутренняя энергия ТС – сумма кинетических энергий всех его молекул, зависящая только от термодинамического состояния ТС.
5. Первое начало термодинамики (тепловая машина, вечный двигатель 1-го рода)
Тепловая машина – ТС (периодически повторяющая круговой процесс), задачей которой является совершение работы над внешними телами за счёт количества тепла Qo, подведенного к системе в течении каждого кругового процесса.
Вечный двигатель 1-го рода – тепловая машина, совершающая работу над внешними телами за цикл большую, чем количество тепла, подведенное к системе. НЕВОЗМОЖЕН.
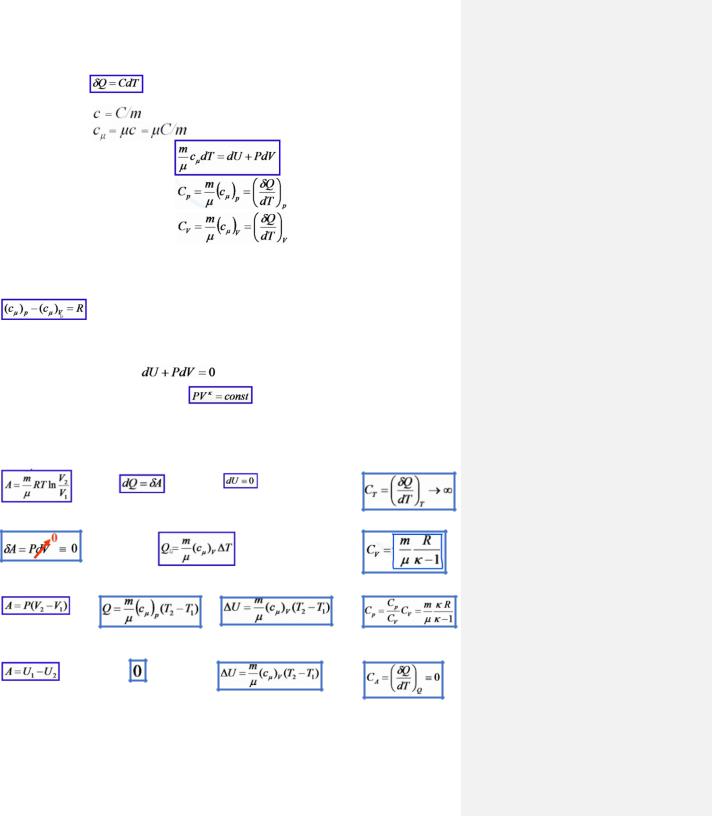
6. Теплоемкость (теплоемкость при постоянном давлении, теплоемкость при постоянном объеме)
Теплоёмкость ТС -
Удельная т-ть -
Молярная т-ть -
Первое начало ТМ с молярной т-тью -
Т-ть при постоянном давлении –
Т-ть при постоянном объёме –
7. Уравнение Майера
Хотим связать теплоёмкости при постоянном давлении и постоянном объёме. Их разность даёт универсальную газовую постоянную R.
8. Адиабатический процесс
РТПр, протекающий постоянном количестве тепла. Q=const.
Первое начало ТМ для него –
Уравнение адиабатического процесса –
9. Теплота и работа при изопроцессах (изотермический, изохорический, изобарический, адиабатический)
Работа |
Теплота |
Вн. Энергия |
Теплоёмкость |
Изотермический (T=const)
Изохорический (V=const)
Изобарический (Р=const)
Адиабатический (Q=const)

10. Второе начало термодинамики – прямой цикл (цикл Карно, вечный двигатель 2-го рода, схема тепловой машины)
Прямой цикл – если работа за цикл больше 0
Цикл Карно – круговой процесс, состоящий из 2 изотерм и 2 адиабат Изот-й процесс идеален для теплообмена Адиаб-й процесс идеален для изменения вн. энергии рабочего тела.
Идеальная ТмП – 
11. Второе начало термодинамики – обратный цикл (холодильная машина, тепловой насос)
Обратный цикл – если работа за цикл меньше 0
Идеальная тепловая машина, работающая по обратному циклу (ТмО) – тепловая м., рабочее тело которой совершает круговой процесс, описываемый обратным циклом Карно.
Холодильная машина – м., задача которой – передача тепла Q2 от холодного тела за счёт работы А вн. сил над ней.
Тепловой насос – м., задача которой передача тепла Q1 к горячему телу за счёт работы А вн. сил над ней.
12. Третье начало термодинамики (вечный двигатель 3-го рода, принцип Нернста +формулировка Планка)
Вечный двигатель 3-го рода – тепловая машина, температура холодильника которой Т2 = 0 К
Принцип Нернста – при любом изотермическом процессе, при Т очень близкой к 0, изменение энтропии строго равно 0 и при приближении к абс. нулю забирать тепло у ТС забирать сложнее
Формулировка Планка – при температуре абсолютного нуля, энтропия любой ТС равна 0 (S=0)

13. Распределение Максвелла (функция распределения частиц по скоростям, вычисление средних значений, среднее значение относительной скорости, среднее значение кинетической энергии)
Функция распр-я частиц по скоростям – показывает относительное число частиц, скорости которых лежат в интервале от u до u+du
Где |
- относительная скорость |
- наиболее вероятная скорость частиц и.г. |
Вычисление средних значений – |
, необходима формула |
|
, где
Среднее значение относительной скорости u частиц газа -
Среднее значение кинетической энергии ε частиц газа -
14. Распределение энергии по степеням свободы
Число степеней свободы физ. Объекта – минимальное кол-во независимых координат, необходимых для описания движений этого объекта.
Частицы и.г. имеют 3 степени свободы, значит на каждую степень -»
2-атомная молекула – материальные точки имеют 2 внутренних степени свободы Итого i=3+2=5 
Искусственно можно создать ситуацию с 4 степенями свободы, если 2-атомную молекулу зажать между 2 плоскостями, тогда она сможет совершать движение лишь в какой-то 1 плоскости. Максимум – 6 степеней свобод ы.
Полная энергия частиц идеального газа вычисляется по формуле:
15. Теплоемкость многоатомных газов
Внутренняя энергия газа –
Теплоёмкость при постоянном объёме –
Теплоёмкость при постоянном |
давлении |
- |
Добавлено примечание ([ТМ1]): Уравнение майера |
записано не правильно, между теплоемкостями должен стоять минус
16. Распределение Максвелла для компонент импульса
17. Распределение Больцмана (при T=const)
выч-ем элем-е кол-во частиц газа в элем-м объёме в потенц-м поле
константа на экспоненту в степени (пот. Энергия делёная на тепловую энергию)

18. Распределение Максвелла-Больцмана
 элемент фазового объёма–элем-й объём 6-мерного пространства
элемент фазового объёма–элем-й объём 6-мерного пространства
19. Фермионы и бозоны: распределение Бозе-Эйнштейна
Бозоны – частицы, с целым спином(собственный момент движения), полностью эквивалентные м/у собой.
Фермионы – частицы, с полуцелым спином, подчиняющиеся принципу Паули
Принцип Паули – в каждой ячейке μ - пространства м.б. не > 1 фермиона и хоть сколько бозонов μ – пространство, 6-тимерное пространство, т.е. имеющее 6 измерений px, py, pz, x, y, z
шестимерное координатно-импульсное пространство
Распределение Бозе-Эйнштейна для бозонов: - -»
Вероятное кол-во частиц в каждом квантовом состоянии - -» Е – полная энергия системы
20. Фермионы и бозоны: распределение Ферми-Дирака для фермионов.

Доказательства ко 2 коллоквиуму:
7. Уравнение Майера –
доказательство в 12 лекции 1:24:00
8. Адиабатический процесс Доказательство в 12 лекции 1:26:30

9. Теплота и работа при изопроцессах
Изотермический (T=const) -
Элементарная работа -»  - подставим Р из ур-я М-К –»
- подставим Р из ур-я М-К –»
Проинтегрируем -»
Внутренняя энергия через т-ть при V=const -»
Первое начало ТМ -»
Изохорический (V=const) Элементарная работа -»
Тогда из первого н. ТМ -» |
-» Интегрируем -» |
Для т-ти используем ур-е Майера -» |
|
Адиабатический (Q=const)
Первое начало ТМ -»  Тогда элем. Работа -»
Тогда элем. Работа -»
Интегрируем -» 
13. Среднее значение кинетической энергии ε частиц газа

16. Распределение Максвелла для компонент импульса
