
- •Экзаменационные вопросы по дисциплине «Биология» для студентов 1 курса лечебного и педиатрического факультетов Раздел «Общая биология»
- •3. Клетка – элементарная и генетическая, структурно-функциональная и биологическая единица живого. Клетка Эукариот, Прокариот, Архей. Основные положения современной клеточной теории.
- •4. Современные представления об организации эукариотической клетки. Сравнительный анализ клеточной организации животных и растений.
- •Значение работ г.Менделя. Закономерности наследования при моногибридном скрещивании. Дигибридное и полигибридное скрещивание. Менделирующие признаки человека.
- •Основы классической генетики. Хромосомная теория т.Моргана. Сцепление генов. Кроссинговер. Метод соматической гибридизации клеток и его применение для картирования генов человека в хромосомах.
- •Взаимодействие аллельных генов. Характер взаимодействия аллелей в детерминации групп крови системы аво у человека.
- •Понятие о неаллельных генах. Их локализация в хромосомах. Эпистаз. Полимерия.
- •13. Основные этапы репликации днк эукариотических клеток.
- •14. Репарация генетического материала. Фотореактивация. Темновая репарация, её этапы. Мутации, связанные с нарушением репарации и их роль в патологии.
- •15. Кодирование и реализация биологической информации в клетке. Кодовая система днк и белка. Центральная догма молекулярной биологии.
- •16. Экспрессия генов в процессе биосинтеза белка. Этапы биосинтеза белка. Особенности транскрипции у эукариот.
- •1. Транскрипция днк.
- •17. Биосинтез белка. Этапы трансляции у эукариот. Сравнительный анализ биосинтеза белка у про- и эукариот.
- •19. Значение генной инженерии для медицины. Схема получения генно-инженерного инсулина. Принципы генной терапии.
- •20. Регуляция экспрессии генов у прокариот. Структурные и регуляторные гены. Особенности регуляции работы генов у эукариот.
- •22. Норма реакции генетически детерминированных признаков. Фенокопии. Адаптивный характер модификации. Роль наследственности и среды в развитии, обучении и воспитании человека.
- •28. Факторы дифференцировки: ооплазматическая сегрегация, эмбриональная индукция. Роль наследственности и среды в онтогенезе. Критические периоды развития. Тератогенные факторы.
- •29. Размножение – универсальное свойство живого, обеспечивающее непрерывность в ряду поколений. Эволюция и формы размножений.
- •30. Гаметогенез. Мейоз: цитологическая и цитогенетическая характеристика.
- •32. Способы регенерации органов и тканей. Репаративная регенерация патологически изменённой печени. Способы стимуляции (хирургические, физические, биологические).
- •Классификация регенерации по масштабу процессов:
- •33. Проблема трансплантации органов и тканей. Виды трансплантации. Трансплантация жизненно важных органов. Тканевая несовместимость и пути её преодоления. Главный комплекс гистосовместимости.
- •35. Терапевтическое клонирование. Стволовые клетки.
- •37. Антропогенез. Качественные отличия человека от животных. Биосоциальная природа человека. Характеристика основных этапов антропогенеза: протантропов, архантропов, палеоантропов, неоантропов.
- •38. Понятие о расах и видовое единство человечества. Современная классификация и распространение человеческих рас. Роль факторов географической среды.
- •40. Учение о биосфере. Концепции биосферы. Границы, структура и функции. Типы круговорота веществ. Значение трудов в. И. Вернадского. Эволюция биосферы.
- •41. Человек и биосфера. Ноосфера – высший этап эволюции биосферы. Необходимые условия для становления и существования ноосферы. Медико-генетические аспекты ноосферы.
- •42. Определение науки экологии. Среда как экологическое понятие. Факторы среды. Экосистема, биогеоценоз, антропобиоценоз.
- •43. Типы биотических взаимоотношений в сообществах. Экологические стратегии выживания. К-стратеги и r-стратеги.
- •46. Адаптация человека к условиям жизнедеятельности и к среде обитания. Адаптивные типы человека. Хронология адаптивных типов человека (Алексеева т.И.).
- •История становления эволюционных идей. Додарвинский период (к. Линней, ж.Б.Ламарк, ж.Кювье, э.Ж.Сент-Илер). Сущность представления ч. Дарвина о механизмах органической эволюции.
- •Становление эволюционной теории. Сущность представлений ч. Дарвина и а.Р. Уоллеса о механизмах органической эволюции. Сравнительный анализ ламаркизма и дарвинизма.
- •52. Микроэволюция. Пути и механизмы видообразования. Способы видообразования.
- •53. Понятие о биологическом виде. Критерии вида. Популяционная структура вида. Генетическая структура популяции. Правило Харди-Вайнберга.
- •54. Элементарные эволюционные факторы: мутационный процесс, популяционные волны, изоляция, дрейф генов, естественный отбор. Взаимодействие эволюционных факторов.
- •55. Естественный отбор. Формы естественного отбора. Специфическое действие естественного отбора в человеческих популяциях.
- •56. Закономерности макроэволюции. Пути биологической эволюции по Северцову. Типы, формы, правила эволюции групп. Темпы эволюции групп.
- •57. Общая схема филогенетического цикла. Принципы эволюции органов. Морфофункциональные преобразования органов.
- •Сводная схема филогенетического цикла (составил а.С.Раутиан)
- •58. Филогенез. Методы изучения эволюционного процесса. Филэмбриогенезы (анаболии, девиации, архаллаксисы)
- •2. Эмбриологические методы:
- •4. Биогеографические методы:
- •5. Методы систематики:
- •60. Сравнительный обзор сердечно-сосудистой системы позвоночных животных. Пороки развития сердца и магистральных сосудов у человека.
- •61. Филогенез хордовых (в виде схемы изобразите эволюцию позвоночных животных). Сравнительный обзор скелета и покровов тела.
- •62. Сравнительный обзор нервной системы позвоночных животных. Типы головного мозга позвоночных. Онтофилогенетически обусловленные пороки развития нервной системы человека.
- •63. Филогенез выделительной системы позвоночных животных. Сравнительная характеристика типов нефронов почек Хордовых.
- •67. Популяционный уровень взаимодействия паразитов и хозяев. Паразитоценоз. Жизненные циклы паразитов и хозяев на примере био- и гео-протистов и био- и геогельминтов.
- •68. Принцип взаимодействия паразита и хозяина на уровне особей. Влияние паразита на хозяина и ответная реакция хозяина. Пути морфологической адаптации паразитов.
- •69. Межвидовые биотические связи в биоценозах. Паразитизм как биологический феномен. Происхождение паразитизма. Распространение паразитических форм в животном мире.
- •70. Понятие об инвазии и инвазионной стадии. Реинвазия. Пути проникновения паразитов и способы передачи возбудителей.
- •71. Жизненные циклы паразитов. Чередование поколений и феномен смены хозяев. Промежуточные, основные, резервуарные, дополнительные хозяева. Пути расселения паразитов: биогельминты и геогельминты.
- •74. Тип Простейшие. Классификация, характерные черты организации. Циклы развития. Типы ассимиляции и способы питания простейших. Формы бесполого и полового размножения.
- •75. Балантидий. Систематическое положение, морфология, цикл развития, пути заражения. Обоснование методов лабораторной диагностики, профилактика.
- •76. Дизентерийная амёба. Систематическое положение, морфология, цикл развития. Обоснование методов лабораторной диагностики, профилактика.
- •77. Малярийный плазмодий. Систематическое положение, виды плазмодиев, цикл развития в организме комара и человека. Пути заражения, методы лабораторной диагностики, профилактика.
- •79. Систематика, морфология и биология возбудителей лейшманиозов. Обоснование методов лабораторной диагностики и мер профилактики.
- •80. Трихомонады, трипаносомы, лямблии. Систематическое положение, морфология, цикл развития, пути заражения. Обоснование методов лабораторной диагностики.
- •81. Методы гельминтоовоскопии. Принципы дегельминтизации и девастации. Организация борьбы с био- и геогельминтами.
- •82. Тип Круглые черви. Характерные черты организации. Понятие о био- и геогельминтах. Очаг геогельминта. Условия возникновения истинного очага. Ложные очаги.
- •83. Анкилостомиды. Систематическое положение, морфология, циклы развития, обоснование лабораторной диагностики. Пути заражения анкилостомидозами. Профилактика. Распространение очагов анкилостомидозов.
- •84. Ришта. Систематическое положение, цикл развития, диагностика, профилактика. Работы л. М. Исаева по ликвидации дракункулеза в Средней Азии.
- •85. Аскарида. Систематическое положение, морфология, цикл развития, пути заражения. Обоснование методов лабораторной диагностики; профилактика. Очаги аскаридозов.
- •86. Власоглав. Систематическое положение, морфология. Особенности цикла развития по сравнению с аскаридой. Обоснование методов диагностики, профилактика.
- •87. Острица. Систематическое положение, морфология, цикл развития, пути заражения. Обоснование методов диагностики, профилактика. Обоснование безмедикаментозного лечения энтеробиоза.
- •88. Угрица кишечная. Систематическое положение, морфология, цикл развития (прямой, непрямой, внутрикишечный), инвазионная стадия. Обоснование методов лабораторной диагностики, профилактика.
- •89. Трихинелла. Систематическое положение, морфология, цикл развития. Пути заражения; обоснование методов лабораторной диагностики, профилактика. Очаги трихинеллёза (синантропные, природноочаговые).
- •90. Лёгочный сосальщик. Систематическое положение, морфология, цикл развития, пути заражения, инвазионная стадия для окончательного хозяина. Обоснование методов лабораторной диагностики, профилактика.
- •Шистосомы. Систематическое положение, морфология, цикл развития. Обоснование методов лабораторной диагностики, профилактика.
- •Печёночный сосальщик. Систематическое положение, циклы развития, пути заражения. Обоснование методов лабораторной диагностики, профилактика. Понятие о транзитных яйцах.
- •Ланцетовидный сосальщик. Систематическое положение, циклы развития, пути заражения, инвазионная стадия для окончательного хозяина. Обоснование методов лабораторной диагностики и профилактики.
- •Бычий цепень. Систематическое положение, морфология, цикл развития. Пути заражения, методы лабораторной диагностики и профилактика тениаринхоза.
- •Лентец широкий. Систематическое положение, морфология, цикл развития, пути заражения дифиллоботриозом. Обоснование методов лабораторной диагностики дифиллоботриоза, профилактика.
- •Карликовый цепень. Систематическое положение, морфология, цикл развития, пути заражения, диагностика, профилактика.
- •100. Тип Членистоногие. Систематика. Характерные черты организации. Медицинское значение. Медицинское значение класса ракообразных.
- •102. Класс насекомые. Систематика. Характерные черты организации. Идиоадаптации насекомых. Медицинское значение.
- •Вши, блохи. Систематическое положение, морфология, развитие, эпидемиологическое значение, меры борьбы.
- •Комары и москиты. Систематическое положение, морфология, развитие, медицинское значение, меры борьбы.
19. Значение генной инженерии для медицины. Схема получения генно-инженерного инсулина. Принципы генной терапии.
Значение генной инженерии для медицины:
Генная инженерия представляет собой новое направление в сфере молекулярной биологии, которое получило широкое распространение во многих сферах медицины и биологии относительно недавно.
Генная инженерия позволяет целенаправленно, по заранее намеченной программе, экспериментально модифицировать геном с использованием генетической информации из разных гетерологических систем: вирусов, бактерий, насекомых, животных и человека. Применяя методы генной инженерии, ученые способны модифицировать структуру генов, а также создавать гибридные гены.
Благодаря генной инженерии стало возможным создание новых диагностических препаратов, вакцин и препаратов для заместительной терапии, а также лечение наследственных заболеваний.
Применение генной терапии в лечении такой патологии как первичные иммунодефициты является единственным терапевтическим методом, обеспечивающим полное излечение, что значительно улучшает качество жизни пациентов и снижает риск летального исхода. В последнее время рассматриваются новые варианты применения генной инженерии в трансплантологии и редактировании генома эмбрионов. Возможность применения этой инновационной технологии порождает множество биоэтических вопросов.
Среди многих достижений генной инженерии, получивших применение в медицине, наиболее значимое — получение человеческого инсулина в промышленных масштабах. Генные инженеры в качестве первой практической задачи решили клонировать ген инсулина. Клонированные гены человеческого инсулина были введены с плазмидой в бактериальную клетку, где начался синтез гормона, который природные микробные штаммы никогда не синтезировали. Инсулин используют для лечения больных диабетом. Традиционно его получают из панкреатических желез свиней и коров, но гормоны этих животных слегка отличаются от инсулина человека. Считают, что инсулин животных часто вызывает побочные эффекты. Сейчас получают дешевый инсулин с помощью генно-инженерного метода путем химико-ферментативного синтеза гена инсулина с последующим введением этого гена в кишечную палочку, которая затем синтезирует гормон. Такой инсулин более «биологичен», так как химически идентичен инсулину, вырабатываемому клетками поджелудочной железы человека.
Сферы использования генной инженерии в медицине значительно расширяются. Так актуальной является
Генная терапия наследственных заболеваний заключается в замене мутантных генов на гены «дикого типа», в которых отсутствуют мутации. Разрабатывается и другой подход, когда введенный ген не заменяет дефектный, а компенсирует его функцию, встраиваясь в хромосому в другом месте.
Еще одной сферой использования генной инженерии в медицине является CAR-T-терапия. На сегодняшний день одним из наиболее перспективных направлений в терапии онкологических заболеваний является адоптивная клеточная иммунотерапия. При проведении такой терапии выделяют, активируют и размножают аутологичные T-лимфоциты, а затем вводят их обратно пациенту, что приводит к частичной регрессии или эрадикации опухоли. Введение Т-клеток, модифицированных химерными антигенными рецепторами (CAR-T-клеток), является одним из наиболее активно развивающихся направлений иммуноонкологии [6]. CAR-T-клетки представляют собой генетически модифицированные собственные Т-клетки пациентов, которые содержат химерный антигенный рецептор. Этот рецептор содержит в себе часть антитела, специфического к антигену опухоли и часть, рецептора Т-клеток. С использованием CAR-T-терапии получены обнадеживающие результаты при гематологических опухолевых заболеваниях. Так, клинические испытания CAR-T-клеток, направленных против В-лимфоцитарного антигена CD19, показали их эффективность при лечении резистентных к химиотерапии опухолей В-клеточного происхождения.
Схема получения генно-инженерного инсулина:
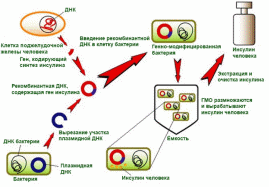
Для получения человеческих инсулинов используются генно-инженерные технологии: участок генома человека, ответственный за синтез инсулина, ассоциируют с геномом E. coli или дрожжевой культуры, в результате чего последние начинают продуцировать человеческий инсулин. Создание аналогов инсулина при помощи перестановок различных аминокислот имело цель получения препаратов с заданной и наиболее благоприятной фармакокинетикой. Так, у аналогов инсулина ультракороткого действия (лизпро, аспарт, глулизин) сахароснижающий эффект развивается уже спустя 15 мин после инъекции, которую можно делать непосредственно перед едой (или даже сразу после), тогда как инъекции простого человеческого инсулина необходимо делать за 30 мин до еды, что значительно менее удобно. Аналоги инсулина гларгин, детенир и деглудек, наоборот, характеризуются длительным действием, которое продолжается на протяжении суток, при этом особенность кинетики препаратов - отсутствие выраженных пиков концентрации в плазме. Используемые в настоящее время препараты инсулина и его аналогов выпускаются в концентрации 100 Ед/мл. По длительности действия инсулины подразделяются на четыре основные группы:
• ультракороткого действия (лизпро, аспарт, глулизин);
• короткого действия (простой человеческий инсулин);
• средней продолжительности действия (инсулины на нейтральном протамине Хагедорна, изофан);
• длительного действия (гларгин, детемир, деглудек);
• смеси инсулинов различной продолжительности действия.
Принципы генной терапии:
Основными методами генной терапии являются:
• добавление гена;
• ингибирование гена;
• заместительная генная терапия;
• уничтожение специфических генов.
Пути доставки генов в пораженные клетки:
1. ex vivo – пораженные клетки выделяют из организма, генетически модифицируют в культуре и снова вводят в организм пациента.
2. in vivo – в случае недоступности клеток или невозможности их эффективно культивировать используют прямое введение ДНК в клетки, находящиеся в организме.
Условия успешной генотерапии:
• обеспечение эффективной доставки чужеродного гена в клетки–мишени;
• обеспечение длительного функционирования его в этих клетках;
• создание условий для полноценной работы гена (его экспрессии).
Эффективность генотерапии определяется прежде всего механизмом доставки терапевтического генетического материала – так называемой «векторной системой».
Существуют вирусные и невирусные векторные системы. В настоящее время наиболее эффективной считается вирусная доставка генов (трансдукция), которая представляет собой упаковку ДНК в вирусную частицу. Перенос генов осуществляется путем нормальной вирусной инфекции, поэтому он эффективен и селективен по отношению к клеткам.
При невирусной доставке (трансфекция) клетки заставляют поглощать ДНК из окружающей среды. ДНК не упаковывается в вирусный вектор, а часто присутствует в составе плазмиды. В некоторых случаях плазмида сконструирована таким образом, что не способна реплицироваться в человеческих клетках, и тогда единственный путь достижения долгосрочной экспрессии – стабильная интеграция ДНК в геном.
