
Laboratornye_raboty_po_fome / 2 Зонная плавка (попроходная) / Методические указания - Зонная плавка
.pdf
необходимо «протиснуться» между соседними атомами. В результате зависимость коэффициента диффузии от температуры имеет вид:
D = D0 |
|
, |
(13) |
|
где энергия активации Q = Ev + Em. Примерно половина величины Q соответствует энергии образования вакансии Ev. А другая половина энергии перемещения Em.
Среднее расстояние Z, на которое распространяется диффундирующее
вещество за время t задается формулой: |
|
L ~ |
(14) |
Диффузия в жидкой среде чрезвычайно важна при проведении зонной плавки и при выполнении других операции. Которые применяются для изготовления полупроводников p-n-типа и кристаллических триодов p-n- типа. При одинаковой температуре диффузия в жидкости происходит гораздо быстрее, чем в твердых телах.
Вжидкостях существует некоторый геометрический порядок. В расположении ближайших соседей: данный атом имеет примерно такое же количество ближайших соседей, как в кристалле этого же вещества. При этом ближайшие соседи и в жидкости, и в кристалле находятся примерно на одинаковых расстояниях. Однако на далеких расстояниях расположение атомов в жидкости является сильно неупорядоченным по сравнению с твердыми телами.
Вто же время и в жидкостях, как и в газах, хаотическое тепловое движение молекул (атомов) содержит в себе «поступательную составляющую». Молекулы перемещаются по занимаемому телом объему. В жидкостях, как и в газах, под действием поля сил тяжести может происходить выравнивание состава среды, сопровождающееся ее движением. Это явление называется конвекцией в направлении конвекционных потоков выравнивание концентрации происходит гораздо быстрее, чем за счет истинной диффузии.

В тех направлениях, где конвекционный перенос отсутствует, выравнивание концентрации происходит только за счет диффузии, при этом уравнения (11) и (14) одинакова применимы как к твердым телам, так и к жидкостям. (Уравнение (14) впервые вывел Эйнштейн для описания броуновского движения мельчайших частиц в жидкости).
Интересная особенность всех экспериментальных данных, полученных для простых жидкостей, состоит в том, что вблизи точки плавления значения коэффициентов диффузии всегда находятся в интервале от 1*



 до 10*
до 10*



 м/с.
м/с.
Эти значения в подавляющем большинстве случаев гораздо выше, чем коэффициенты диффузии в твердой фазе в непосредственной близости от точки плавления. [7]
2.5 Пример условия равновесия фаз бинарной смеси
Рассмотрим в качестве примера вещество A, содержащие примесь B. Обозначим через Cs концентрацию примеси в твердой фазе, выпадающей осадок из жидкой фазы, где концентрация примеси равна CL согласно (10).
Изображенный на рисунке 1 расплавленный стержень длиной L, концентрация примеси B в котором равна C0 охлаждается с левого конца и затвердевает.
Рисунок 1 – Распределение примесей в расплавленном стержне Предполагается, что в твердой фазе диффузия атомов примеси не
происходит, а в жидкой диффузия происходит так быстро, что концентрация все время остается однородной. Это предположение представляется весьма правдоподобным, так как коэффициенты диффузии примеси в твердой и жидкой фазах отличаются в сотни тысяч раз.
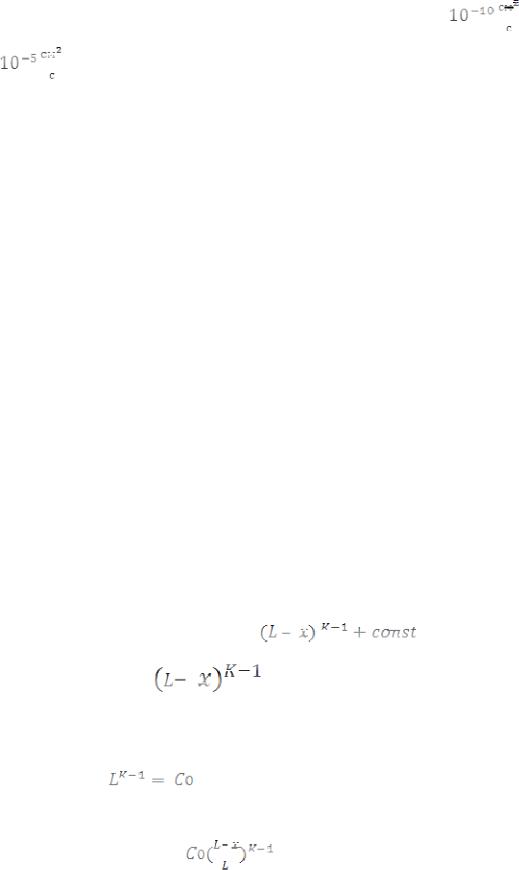
Например, при температуре плавления алюминия (660 °С)
коэффициент диффузии цинка в алюминии: Ds =5* |
|
; Dz = |
|||||
2.5* |
|
|
|
|
. |
|
|
|
|
|
|
||||
|
|
|
|||||
|
Найдем распределение концентрации примеси после того, как граница |
||||||
фаз сместится к правому концу стрежня, и он весь затвердеет.
Примем поперечное сечение стержня равным единице и обозначим через CL(x) концентрацию примесей в жидкой части стержня. Когда длина затвердевшей части, отсчитывается от левого конца равна x. Пусть процесс затвердевания продолжается и длина затвердевшей части увеличится на dx. При этом количестве примесей, перешедшее из жидкой фазы в твердую согласно (10) KCLCx.
Эта величина равна изменению d[CL (x)( L – x )] количества примесей в жидкой фазе равного ввиду однородности распределения примеси в
жидкости |
CL (x)( L – x) таким образом: |
|
|
|
|
||||||||||||||||
|
d[CL (x)( L –x )] = – kCL (x)dx, |
(15) |
|||||||||||||||||||
|
dCL (x)( L – x)/Cx – CL(x) = – KCL(x), |
(16) |
|||||||||||||||||||
или |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
dCx(x)( L – x)/dx = – (K–1)CL (x) |
(17) |
|||||||||||||||||||
После разделения переменных: |
|
|
|
|
|||||||||||||||||
|
|
|
dCL (x)/CL (x) = – (K–1)dx/L– x, |
||||||||||||||||||
и интегрирования lnCL (x) = ln |
|
|
|
|
|
|
|
, получаем |
|||||||||||||
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||
|
CL(x) = A |
|
|
|
|
|
|
|
|
|
|
(18) |
|||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
||||||||||||||||||||
Где А - постоянная, определяемая из того условия, что концентрации |
|||||||||||||||||||||
примесей в исходной фазе равна C0. |
|
|
|
|
|||||||||||||||||
|
M |
|
|
|
|
|
|
|
|
(19) |
|||||||||||
|
|
||||||||||||||||||||
и, следовательно, |
|
|
|
|
|||||||||||||||||
|
|
CL(x) = |
|
|
|
|
|
|
(20) |
||||||||||||
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
||||||||||||||||||
|
|
|
|||||||||||||||||||

Концентрация примесей в твердой фазе, выпадающей в точке x определяется следующим образом:
Cs(x) = KCL(x) = K ( |
|
|
|
(21) |
Эта функция изображена на рисунке 2.
Рисунок 2 – Зависимость концентрации в твердой примеси Cs(x) от х.
Для случая K < 1. Из полученной формулы следует, что x→∞, при x→L. Это не вполне точно. Ошибка обусловлена использованием предложения о постоянстве величины K, что справедливо лишь для слабых растворов, т.е. С концентрация меньшей единицы.
Мы видим, что примеси собираются в правом конце стержня, а его левый конец очищается от них. При K > 1 очистился бы правый конец стержня [14].
2.6 Зонная очистка. Попроходная плавка.
При очистке материалов от примесей данным методом стержень этого материала пропускают чрез катушку индукционного нагревателя (рисунок 1). При этом часть стержня, находящаяся вблизи катушки, плавится и перекристаллизируется. А примеси собираются на одном из его концов (смотря по тому, больше или меньше единицы коэффициент сегрегации К.) Расплавленная часть сохраняет свою форму благодаря силам поверхностного натяжения. Процесс плавления (рисунок 3).

Рисунок 3 – Процесс плавления стержня При медленном движении загрязненного алюминия в графитовой
лодочке относительно индукционных нагревателей вдоль слитка перемещаются расплавленные зоны, переносящие накапливающиеся в них примеси к его концу. 1 - примеси; 2 - графитовая лодочка; 3 - индукционные нагреватели; 4 - чистый алюминий; 5 - расплавленная зона.
Метод получения очень чистых веществ, основанный на повторении несколько раз такой зонной плавки, называется попроходной зонной очисткой. Этот метод широко применяется при очистке полупроводников, используемых в электронной промышленности для изготовления полупроводниковых приборов, где требования к чистоте очень велики. Например, так называемый технический кремний, являющийся исходным материалом для зонной очистки, содержит примерно 1% примесей. Его получают из природных оксидов кремния – песка и кварца, восстановлением в пламени электрической дуги. По мере увеличения числа проходов расплавленной зоны степень очистки значительно возрастает. Однако эффективность оттеснения примеси при каждом новом проходе падает. В конце концов достигается некоторое предельное распределение примеси по длине образца. Поскольку зонная плавка - процесс весьма длительный, желательно, естественно, получить распределение близкое к предельному, за минимальное число проходов. После многопроходной зонной плавки удается

очистить кремний до уровня 




 %, соответствующего 1 атому примеси на 15 миллиардов атомов кремния.
%, соответствующего 1 атому примеси на 15 миллиардов атомов кремния.
В металлургической промышленности методом зонной плавки получают сверхчистый алюминий с содержанием примесей не более 0.001 % сегрегации. С явлением сегрегации примесей, лежащим в основе метода зонной очистки, хорошо знакомы полярники. Отправляясь в путешествие по Северному ледовитому океану, пресную воду они с собой не берут. Для получения пресной воды достаточно растопить кусок льда, образовавшегося из очень соленой воды. Лед, кристаллизующийся из соленой морской воды, сам практически не содержит соли.
Прежде чем, рассмотреть математическую модель процесса зонной плавки сделаем несколько замечаний, относящихся к деталям физического механизма перераспределения примесей в результате такой направленной кристаллизации.
Если нагреватель перемещается вдоль образца очень быстро, примесь не успевает диффундировать в объеме жидкой фазы и тогда вместо равновесного соотношения между концентрациями по разные стороны межфазной границы мы получаем CL= Cs, т.е K = 1. Это не удивительно, поскольку процесс в этом случае идет неравновесно. Напротив, если граница раздела фаз перемещается медленно, отношение Cs/CL→K0.
Для процесса направленной кристаллизации можно ввести представление об эффективном коэффициенте K, определив его как отношение концентрации компонента B в точке x после перекристаллизации Cs в средней концентрации компонента B в расплаве CL в тот момент, когда фронт кристаллизации проходил через эту точку. Очевидно, что K0<K<1.
Основные допущения в модели зонной очистки заключается в предположении о том, что при постоянной скорости кристаллизации коэффициент K не меняется при движении межфазной границы вдоль стержня. А перераспределение примеси в расплавленной зоне происходит мгновенно [5].

Скорость нагревания будем считать совпадающей со скоростью движения фронта кристаллизации. Итак, пусть длина нагревателя – l. Начальное распределение примеси C0= const. Рассмотрим баланс примесного компонента при перекристаллизации слоя шириной ∆x. (рисунок 4)
Рисунок 4 – Баланс примесного компонента при перекристаллизации. Изменение содержания примеси в твердой фазе слева от нагревателя-
KCL∆x.
Изменение содержания примеси в расплавленной зоне нагревателя-
∆CLl.
Изменение содержания примеси в твердой фазе справа от нагревателя – C0(x+l) ∆x.
Ввиду того, что общее количество примеси не изменилось, сумма всех
изменений равна нулю. |
|
KCL (x) ∆x + ∆CL (x) l – C0(x + l) ∆x = 0, |
(22) |
Откуда |
|
dCL/dx = [C0(x+ l) – KCL(x)]/ l |
(23) |
Уравнение (11) записано для первого прохода нагревателя, поэтому CL (x+l) = C0. Линейное дифференциальное уравнение первого порядка (11) в стандартном виде запишется следующим образом:
dCx(x)/dx + KCL (x)/ l = C0/ l |
(24) |
После переобозначений |
|
CL (x) = y, |
|
K/ l =p, |
(25) |
C0/ l =Q. |
(26) |
Оно примет канонический вид, |
|
y’ + yp = Q. |
(27) |

Решение его можно найти, например известным методом вариации произвольного постоянного:








 [y(0) +
[y(0) + 







 dx] (28) После возвращения к исходным обозначениям получим решение:
dx] (28) После возвращения к исходным обозначениям получим решение:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CL (x) = C0 [1 + |
|
|
|
]. |
|
|
|
|
|
(29) |
|||
И после простых преобразованийрешение для Cs(x): |
|
||||||||||||
Cs(x) = KCL (x) = [1 (1 K) |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
||||||||
|
|
|
|
||||||||||
]. |
(30) |
||||||||||||
Решая (11 и 18), получаем график для распределения примеси после первого прохода. (рисунок 5)
Рисунок 5 - Распределения примеси после первого прохода. Уравнение (11) можно обобщить для любого прохода. Пусть на
предыдущем n-ом переходе распределение примеси - 










 , тогда
, тогда
(31)
Уравнение (19) необходимо дополнить граничными условиями. Для начальной точки образца:
(g)dg |
(32) |
Указание CL’ = 






 (g)dg , концентрация в расплавленной зоне от 0 до l ,из которой в твердую фазу перейдет лишь KCL’. Мы предполагаем, что равномерное распределение примесей в расплавленной зоне устанавливается мгновенно.
(g)dg , концентрация в расплавленной зоне от 0 до l ,из которой в твердую фазу перейдет лишь KCL’. Мы предполагаем, что равномерное распределение примесей в расплавленной зоне устанавливается мгновенно.

2.Для конечного участка образца (L l,l), граничное условие определяется условиями кристаллизации на этом участке. Обычно нагреватель постепенно сходит с образца, тогда можно положить что:
|
|
|
|
|
|
|
(L l)( |
|
|
|
, L – l < x < L |
(33) |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
||||||
Указание, в данном случае вместо |
C0 в (20) надо |
подставить |
||||||||||
концентрацию примеси в расплавленной зоне L – l, l .Она равна 


 (L – l)/K. Иногда зонный нагреватель включают сразу после расплавления последней части образца. В этом случае последняя зона кристаллизуется не направленно и примесь в ней распределяется приблизительно равномерно.
(L – l)/K. Иногда зонный нагреватель включают сразу после расплавления последней части образца. В этом случае последняя зона кристаллизуется не направленно и примесь в ней распределяется приблизительно равномерно.
Этому решению соответствует граничное условие:
, L – l < x < L. |
(34) |
Вточке x = L – l происходит скачкообразное изменение концентрации
в1/K раз.
2.7 Моделирование и изучение процесса многопроходной зонной очистки
По мере увеличения числа проходов расплавленной зоны степень очистки значительно возрастет, однако эффективность оттеснения примеси при каждом новом проходе падает. В конце концов достигается некоторое предельное распределение примеси по длине образца. Поскольку зонная плавка-процесс весьма длительный, желательно, естественно, получить распределение, близкое к предельному, за минимальное число проходов. Кроме того, представляет интерес изучить влияние технологических параметров: ширины нагревателя – l ,скорости перемещения нагревателя – Vн (она влияет на K), числа проходов – N.
Ввиду того, что аналитическое решение зацепляющейся цепочки уравнений зонной очистки (31) с граничными условиями (32-34) практически невозможно. Проследить все происходящие процессы лучше всего с помощью решения задачи на ЭВМ. Для расчетов мы примем следующую,

весьма распространенную формулу, связывающую коэффициент разделения со скоростью перемещения нагревателя
(35)
Где Vн –скорость нагревателя, V0 – некоторая постоянная, зависящая от скорости диффузии жидкости в расплаве. График зависимости коэффициента разделения от скорости перемещения нагревателя. (рисунок 6)
Рисунок 6 - Зависимость коэффициента разделения от скорости перемещения нагревателя
Уравнение (31) представляет собой линейное дифференциальное уравнение 1-го порядка относительно неизвестной функции 










 .Если известно начальное распределение примесей
.Если известно начальное распределение примесей 








 ,то последовательным интегрированием уравнения (31) можно определить распределение примесей после любого числа проходов зоны.
,то последовательным интегрированием уравнения (31) можно определить распределение примесей после любого числа проходов зоны.
Итак, уравнения (31-34) представляют собой математическую модель процесса зонной перекристаллизации, исходя из которой возможно поставить численный эксперимент на ЭВМ.
