
12_Laboratornaya_fizika
.docxПЕРВОЕ ВЫСШЕЕ ТЕХНИЧЕСКОЕ УЧЕБНОЕ ЗАВЕДЕНИЕ РОССИИ

МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ Федеральное государственное бюджетное образовательное учреждение высшего образования «САНКТ-ПЕТЕРБУРГСКИЙ ГОРНЫЙ УНИВЕРСИТЕТ»
Лабораторная работа №12
По дисциплине |
ФИЗИКА |
(наименование учебной дисциплины согласно учебному плану) |
|
Тема: Исследование эффекта Джоуля-Томпсона при адиабатическом истечении газа. |
Вариант №6
Автор: студент гр. ЭРБ-18-1 |
|
________________ |
/_Сковородкин И.И.._/ |
|
|
|
(подпись) |
|
|
ОЦЕНКА: ___________ |
|
|
|
|
Дата: ________________ |
|
|
|
|
ПРОВЕРИЛ |
ассистент |
______________ |
/ Скалецкая И.Е. / |
|
|
(должность) |
(подпись) |
(Ф.И.О.) |
|
Санкт-Петербург 2018 год
Цель работы:
определение изменения температуры углекислого газа при протекании через малопроницаемую перегородку при разных начальных значениях давления и температуры;
вычисление по результатам опытов коэффициентов Ван-дер-Ваальса "a" и "b"
Краткое теоретическое содержание:
Явление, лежащее в основе работы: эффект Джоуля-Томсона.
Определение основных физических понятий, объектов, процессов и величин:
Эффект Джоуля-Томсона - изменение температуры газа, медленно протекающего из области высокого в область низкого давления в условиях хорошей тепловой изоляции.
Адиабатический процесс - термодинамический процесс, который осуществляется в системе без теплообмена с внешним миром.
Идеальный газ – теоретическая модель газа, в которой между молекулами отсутствуют силы взаимного притяжения и сами молекулы принимаются за материальные точки.
Тепловое расширение - изменение размеров тела в процессе его нагревания.
Температура инверсии - повышение температуры воздуха с высотой в некотором слое атмосферы.
Критическая температура - температура, при которой исчезают различия физических свойствах между жидкостью и ее насыщенным паром.
a и b – константы Ван-дер-Ваальса, которые являются характеристикой каждого газа
Законы и соотношения, описывающие изучаемые процессы, на основании которых получены расчётные формулы:
Первый закон термодинамики – теплота, сообщаемая системе, расходуется на изменение внутренней энергии системы и на совершение системой работы против внешних сил. Q=∆U+A, где Q – количество теплоты, Дж; U – внутренняя энергия, Дж; A – работы, Дж
Уравнение Менделеева-Клапейрона (идеального газа) – формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой идеального газа, имеющая вид:

где P – давление [Па] V – объём [м^3] R – универсальная газовая постоянная,
R=8,31 [Дж/(моль∙К)] T – температура, [К]
Уравнение Ван-дер-Ваальса (реального газа) – формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой реального газа при помощи коэффициентов Ван-дер-Ваальса, имеющая вид:

Поправка
a
( )
– поправка, учитывающая силы притяжения
между молекулами (давление на стенку
уменьшается, т.к. есть силы, втягивающие
молекулы приграничного слоя внутрь).
)
– поправка, учитывающая силы притяжения
между молекулами (давление на стенку
уменьшается, т.к. есть силы, втягивающие
молекулы приграничного слоя внутрь).
Поправка b — поправка, учитывающая силы отталкивания (из общего объёма вычитается объём, занимаемый молекулами).
Схема установки:
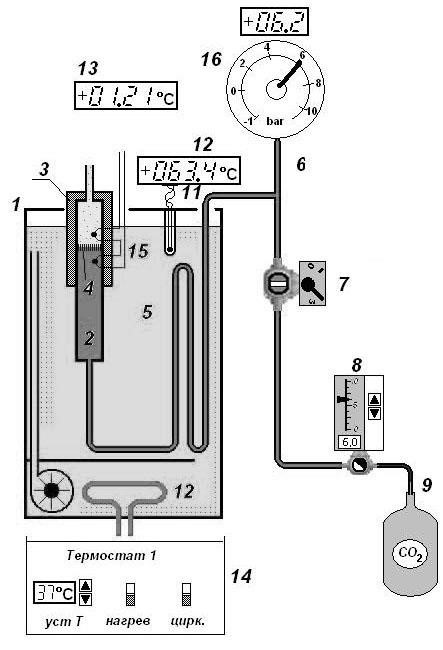
теплоизоляционная защит
каналы пористой перегородки
трубка с пористой перегородкой
пористая перегородка
теплообменник
магистраль
кран
редуктор
балон с газом
индикатор температуры воды
термопара
термостат
индикатор, отображающий дифференциальную температуру
пульт
дифференциальный термометр
манометр
Расчётные формулы:
1.Перепад давлений в теплоизолированной трубке:
 ,
где
,
где
 -
разность давлений, [
-
разность давлений, [ =Па,
=Па,
 начальное
давление,
начальное
давление,
 -
атмосферное давление
-
атмосферное давление
2.Коэффициент Джоуля-Томсона:
 где
–
где
–
 коэффициент Джоуля –Томсона [C/Па]
коэффициент Джоуля –Томсона [C/Па]
 -
Разность температур [C]
-
Разность температур [C]
a
- постоянная Ван-дер-Ваальс [
R - универсальная газовая постоянная [Дж/(моль*К)]
b- постоянная Ван-дер-Ваальса [(м^3)/моль]
3.Температура инверсии:


Экспериментальные данные
Физ.величина |
|
|
|
µ |
a |
b |
Tинв |
Tкр |
Ед. изм. |
|
|
|
|
|
|
|
|
Номер опыта |
||||||||
1 |
20 |
9,0 |
9,87 |
1,097 |
0.356 |
35,203 |
|
|
2 |
8,0 |
8,74 |
1,093 |
|||||
3 |
7,5 |
8,18 |
1,091 |
|||||
4 |
6,5 |
7,07 |
1,088 |
|||||
5 |
5 |
5,41 |
1,082 |
|||||
6 |
40 |
9,0 |
8,80 |
0,978 |
||||
7 |
8,0 |
7,81 |
0,976 |
|||||
8 |
7,5 |
7,31 |
0,975 |
|||||
9 |
6,5 |
6,32 |
0,972 |
|||||
10 |
5,0 |
4,85 |
0,970 |
|||||
11 |
75 |
9,0 |
7,49 |
0,832 |
||||
12 |
8,5 |
7,07 |
0,832 |
|||||
13 |
8,0 |
6,65 |
0,831 |
|||||
14 |
7,5 |
6,24 |
0,832 |
|||||
15 |
6,5 |
5,40 |
0,831 |
|||||








Погрешности
Прямые
 ;
;

Косвенные

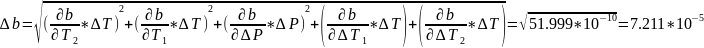

Вывод
В ходе проведенной лабораторной работы было определено изменение температуры углекислого газа при протекании через малопроницаемую перегородку при разных начальных значениях давления и температуры; по результатам опытов определены коэффициенты Ван-дер-Ваальса.


 P
P