
Лекции УГМУ / Печень
.pdfПатофизиология печени
Анализ любого патологического процесса в органе становится возможным при четком представлении о структуре и функции последнего.
Вместе с тем элементарная структура органа, как правило, является понятием умозрительным, зависящим от примененного подхода. В
выделении такой структуры для печени отталкивается от вида сосуда,
помещаемого в центр ее.
Морфофункциональная характеристика печени
При выделении классической печеночной дольки в ее центр помещают центральную печеночную вену, то есть первичный венозный коллектор,
сосуд, по которому кровь оттекает от органа, а портальный тракт находится на периферии.
Однако введение понятия «функциональный элемент» требует рассматривать элементарную структуру как часть паренхимы, ограниченную микроциркуляторным руслом, в котором центральное место занимает терминальная артериола, то есть кровь приносящий сосуд. Особенностью печени является наличие двух приносящих сосудов: артериального – терминальная веточка печеночной артерии; венозного – терминальная веточка портальной вены. Их-то и помещают в центр функционального элемента.
Общее строение печени аналогично общему строению любого крупного железистого органа и похоже на строение «древесной кроны».
Ветви кроны соответствуют ветвлениям воротных сосудов и желчных ходов,
все промежутки между которыми заполнены без остатка паренхимой.
Структурнофункциональной единицей органа (или функциональным элементом) является простой печеночный ацинус. Обычно терминальные
1
ветви печеночной вены делятся на три веточки – три расходящихся осевых синусоида. Ориентированные вокруг осевого синусоида клетки паренхимы и формируют простой печеночный ацинус. На некотором расстоянии вглубь паренхимы осевой синусоид сопровождает артериола – терминальный участок разветвлений печеночной артерии. Вместе с ним проходят и начальные участки мельчайших желчных протоков, так называемые внутриацинарные желчные ходы, или дуктулы. В паренхиме осевой синусоид постепенно делится на сеть синусоидов, пронизывающих паренхиму и представляющих широкоанастомозирующую разветвленную сеть, – «муралиум». Синусоиды паренхимы направлены преимущественно к лежащим на стыках соседних ацинусов первичным печеночным венозным коллекторам – мельчайшие разветвления печеночных вен. Кровь из синусоидной сети каждого ацинуса поступает в два-три (иногда более)
первичных венозных коллектора.
Всоответствии с реально существующими условиями кровообращения
впаренхиме следует различать три зоны печеночных клеток в простом ацинусе: первая зона представлена клетками, лежащими вблизи осевых синусоидов ацинуса и получающих кровь, наиболее насыщенную кислородом и питательными веществами, то есть находящимися в оптимальных условиях кровоснабжения; вторая зона представлена клетками с постепенно ухудшающимися условиями кровоснабжения; третья зона циркуляторной периферии, периферического кровоснабжения ацинуса.
Клетки первой зоны первыми вступают в контакт с различными поступающими в кровь вредностями. Они наиболее резистентны и наиболее регенераторно потентны. Клетки же третей зоны наименее резистентны к любым повреждениям. Печеночные клетки, расположенные в непосредственной близости от портальных трактов (в месте отхождения осевого синусоида от терминальных ветвей портальной вены), оказываются
2
в худших условиях кровообращения, а расположенные вдали от портальных трактов в первой зоне ацинуса в местах отхождения синусоидов паренхимы от осевого синусоида, оказываются в оптимальных условиях кровоснабжения.
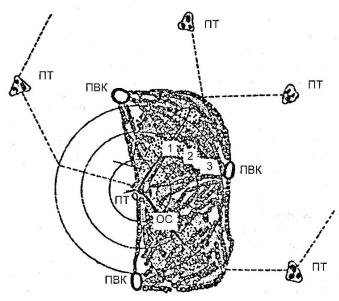
Рис. 102
Схема строения паренхимы печени, структурно-функциональная
единица – печеночный ацинус (по Rappaport, 1969)
ПТ – портальный тракт; ПВК – первичный венозный коллектор; ОС – осевой синусоид ацинуса; 1,2, 3 – зоны кровоснабжения ацинуса. Сплошная линия – граница зон «портальной» дольки; пунктирная – граница
«классической» гексагональной дольки.
Группа простых ацинусов, расположенных по ходу терминальных ветвлений воротной вены и отходящих из одного портального тракта,
составляют сложный, или комплексный, ацинус. В свою очередь, группы сложных ацинусов, исходящих из соседних терминальных ветвлений портальных трактов, составляют вокруг более крупных портальных трактов ацинарные агломераты, объединяющихся в группы агломератов, которые
3
располагаются вокруг еще более крупных стволов воротной вены. Последние образуют в сумме уже доли печени.
Печеночные клетки в ацинусе располагаются переплетением однорядными пластинами (балками). Благодаря такому строению микроциркуляторное русло кроветворной системы (синусоиды)
непосредственно соприкасается каждой паренхиматозной клеткой. Стенка синусоидов печени не имеет свойственной капиллярам других органов базальной мембраны и построена из одного ряда лежащих на каркасе ретикулярных волокон Купферовских клеток, лишь соприкасающихся либо частично черепицеобразно заходящих друг на друга, между краями которых имеются щелевидные пространства. Между Купферовскими клетками и поверхностью печеночных клеток имеются свободное пространство − пространство Диссе.
Выведение продукта внешней секреции печеночных клеток (желчи)
осуществляется со стороны другого билиарного полюса печеночной клетки в желчные капилляры, представляющие собой щелевидные ходы между двумя или тремя клетками, которые образованы углублениями в наружных клеточных мембранах билиарных полюсов клеток. Желчные капилляры не имеют собственных стенок. Желчные капилляры герметически замкнуты специальным замыкающим аппаратом, связывающим по их краю наружные клеточные мембраны соседних печеночных клеток. Существует небольшая возможность диффузии сквозь него некоторых веществ в тончайшие межклеточные щели, расположенные между смежными клетками и разобщенными с пространством Диссе с другого полюса клетки таким же замыкающим аппаратом.
Гепатоциты отделены от желчных капилляров базолатеральной мембраной, а от синусоидов − синусоидальной. Из-за разницы в строении
4
синусоидальной мембраны и мембраны, обращенной к желчному капилляру, гепатоцит является полярной клеткой.
Синусоидальная мембрана вовлечена в процесс двухстороннего переноса веществ. Транспортные процессы включают захват аминокислот,
глюкозы, органических анионов, таких как желчные, жирные кислоты и билирубин, для последующих рецепторопосредованных внутриклеточных реакций. На синусоидальной мембране гепатоцита находятся специфические транспортеры, в частности Na+-, K+-АТФ-аза, и проходят процессы выделения альбуминов, липопротеинов и факторов свертывания крови.
Основной функцией мембраны, обращенной в желчные капилляры,
является секреция желчи, но всасывающая способность этой мембраны ограничена. На этой части мембраны гепатоцитов расположены специфические ферменты: щелочная фосфатаза, лейцинаминопептидаза, -
глютамилтранспептидаза.
Зональное расположение клеток в ацинусе определяет и их функциональную гетерогенность. Так, клетки первой зоны, первыми встречающие поступающую в печень кровь воротной вены, характеризуются высокой активностью окислительно-восстановительных энзимов цикла Кребса, наиболее высокими показателями энергетического потенциала,
углеводного обмена (прежде всего глюконеогенеза), максимальным накоплением лабильного гликогена в цитоплазме. Наиболее высоким уровнем протеинового обмена. В клетках этой зоны интенсивно осуществляются процессы детоксикации. В этих клетках преобладают процессы синтеза собственных структур белков клеток и ферментов. Для них характерно наличие фигур митоза. В нормальных условиях гепатоциты делятся почти исключительно в этой зоне, которую можно считать своеобразным камбием (ростковой зоной) печеночной паренхимы, затем постепенно перемещаются по направлению от портального тракта к
5
первичному венозному коллектору со скоростью 1,4 мкм в сутки,
преодолевая 0,3% диаметра ацинуса. Если исходить из того, что гепатоциты соединены между собой плотными контактами, то следует признать, что весь комплекс печеночных клеток, объединенных в пластинку (балку),
движется вместе с синусоидальными клетками (аналогично ленте транспортера или эскалатора). Элиминация подвергающихся инволюции клеток происходит путем апоптоза (1-я стадия − конденсация хроматина с кариопикнозом и кариорексисом; 2-я стадия − фрагментация и образование апоптозных телец, выходящих в межклеточное пространство; 3-я стадия − фагоцитоз апоптозных телец интактными гепатоцитами и частично макрофагами; 4-я стадия − разрушение фагоцитированных апоптозных телец лизосомами гепатоцитов).
При усиленном обновлении гепатоцитов может наступить частичная недостаточность апоптоза. В этих условиях отдельные гепатоциты могут проникать в эндотелиальное пространство, а затем в просвет первичного венозного коллектора (центральной вены). Следует также помнить, что делящиеся гепатоциты теряют способность выполнять другие функции, в
частности метаболизировать токсические вещества.
В противоположность клеткам первой зоны, в клетках третьей зоны ацинуса, через которую протекает кровь с относительно бедным содержанием кислорода, более выражены процессы синтеза основных
«экспортируемых» клеткой белков − альбумины плазмы крови, фибриноген и т.п., высок уровень гликолитических процессов и процессов дегидрогенизации. Эти клетки в первую очередь накапливают печеночные пигменты, в большинстве своем содержащие липиды. В них формируются липидные накопления.
Из желчных капилляров желчь попадает в терминальные желчные протоки, каналы Геринга, выстланные полигональными клетками
6
«закрытой» связи с расположенными рядом гепатоцитами. Эти короткие протоки постепенно соединяются в более крупные протоки, затем интралобулярные протоки, выстланные кубическим эпителием и имеющие диаметр 30−40 мкм. Из них желчь поступает в общий желчный проток и далее в желчный пузырь и двенадцатиперстную кишку.
Основные функции желчного пузыря: концентрация и депонирование желчи между приемами пищи; эвакуация желчи посредством сокращения гладкомышечной стенки желчного пузыря в ответ на стимуляцию холецистокинином; поддержание гидростатического давления в желчных путях. Желчный пузырь обладает способностью десятикратно концентрировать желчь. В результате этого образуется пузырная,
изотоничная плазме желчь, но содержащая более высокие концентрации натрия, калия, желчных кислот, кальция и более низкие − хлоридов и бикарбонатов, чем печеночная желчь.
Печень и адаптивные реакции организма
Об участии печени в формировании адаптивных реакций организма свидетельствует тот факт, что уже в первые минуты воздействия экстремального фактора (например, травмы) на организм в ней развиваются явления возбуждения внутриклеточных метаболических процессов. Это иллюстрируется стимуляцией потребления кислорода печеночными клетками, активацией сукцинатдегидрогеназы и цитохромоксидазы,
накоплением в них восстановленного глутатиона, большинства аминокислот,
убылью аскорбиновой кислоты. При продолжительном действии экстремального фактора или при его чрезмерной силе наступает дезинтеграция метаболических реакций. Сначала отмечается депрессия потребления кислорода и выделение углекислоты, а затем и ингибиция ферментов.
7
Белковый обмен. В печени осуществляется как анаболические
(синтетические), так и основные катаболические процессы обмена белков.
Синтез белков осуществляется в печени прежде всего из свободных аминокислот, которые поступают в обменный фонд печени из трех источников:
1.Экзогенные аминокислоты, поступающие с кровью воротной вены из кишечника. Приток этих веществ зависит от времени суток, фазы пищеварения, количества и качественного состава пищи, активности пищеварительных ферментов желудочно-кишечного тракта и т. п.
2.Эндогенные свободные аминокислоты и другие продукты эндогенного белкового распада возникают в организме как постоянные метаболиты физиологического клеточного распада в других органах. Приток этих веществ в печень относительно постоянен в нормальных условиях,
суточные его колебания не очень велики, но в условиях патологии поступление их в печень может значительно изменяться качественно и количественно.
3. Аминокислоты, образующиеся в процессе обмена из углеводов и жирных кислот. Этот процесс в организме совершается преимущественно в самой печени в относительно небольшом объеме путем аминирования и трансаминирования.
Печеночные клетки синтезируют большинство протеинов плазмы крови – практически весь альбумин, основную массу - и значительную часть
-глобулинов, фибриноген и основные белки системы свертывания крови
(она – единственный орган, синтезирующий протромбин, в ней синтезируется конвертин), антикоагулянт прямого действия – гепарин.
Купферовские клетки печени способны синтезировать определенное количество -глобулинов.
8
Не менее существенна для организма и роль печени в катаболизме белков. В печени осуществляются все этапы расщепления белковых веществ до образования аммиака и мочевины. У млекопитающих печень единственный орган, в котором образуется мочевина. Печеночная паренхима осуществляет также и катаболизм нуклеопротеидов с расщеплением их до аминокислот, пуриновых и пиримидиновых оснований.
В печени происходит превращение последних в мочевую кислоту,
выделяемую затем почками.
При действии на организм чрезвычайных факторов (стресс-факторов)
развивается комплекс биохимических изменений, проявляющихся, в
частности, генерализованным катаболизмом белков органов и тканей, что рассматривается как адаптивная неспецифическая реакция, выработанная в процессе эволюции. При этом в большинстве случаев в печени увеличивается содержание свободных аминокислот (прежде всего незаменимых) и РНК, то есть имеет место усиление мобилизации аминокислот из тканей и накопление их в печени с последующим усилением глюконеогенеза и синтеза плазменных белков, в том числе наиболее важных, определяющих онкотическое давление и состояние гемостаза крови. При истощении адаптивных реакций наступает катастрофическое падение уровня большинства аминокислот в печеночных клетках.
Углеводный обмен. Печень является главным органом углеводного обмена, регулирующим поступление углеводов – важнейшего источника энергетических ресурсов организма. Эта регуляция осуществляется координированным, обратимым двусторонним процессом – глюконеогенеза и гликогенолиза, то есть образования гликогена из поступивших в печень из кишечника моносахаридов и образования глюкозы крови из депо гликогена в ткани печени. Образование гликогена в печени идет не только за счет поступления моносахаров из кишечника, но и путем восстановления из
9
поступающих в кровь продуктов распада гликогена в мышцах (молочная кислота), а также из некоторых аминокислот и образующихся в обменных циклах белкового и липидного обмена пировиноградной кислоты. В
результате активного процесса глюконеогенеза (при увеличении инсулина) в
печени образуется значительное депо гликогена, которое может достигать
1/5 массы органа.
При стрессовых ситуациях, при развитии гипоксических состояний происходит усиленная мобилизация углеводов из печени для покрытия энергетических потребностей органов и тканей. Это же имеет место при голодании.
Обмен липидов. Печени принадлежит ведущая роль в обмене липидных веществ – нейтральных жиров, жирных кислот, фосфолипидов,
холестерина. Она, с одной стороны, благодаря желчеобразовательной и желчевыделительной функции регулирует всасывание липидов в кишечнике,
с другой – является центральным местом метаболизма жирных кислот (в ней происходит как синтез жирным кислот, так и их расщепление до кетоновых тел, насыщение ненасыщенных жирных кислот, включение последних в ресинтез липидов в виде нейтральных жиров и фосфолипидов с последующим выведением их в кровь и желчь). Основная масса жирных кислот синтезируется в печени и поступает в нее с нейтральными жирами из кишечника и периферических жировых депо организма, но они синтезируются также из глюкозы, через образование уксусной кислоты и ацетилуксусной кислоты, при участии коэнзима-А и из белковых веществ путем дезаминирования аминокислот. Процесс накопления жирных кислот в печени регулируется гипофизарно-надпочечниковой системой и осуществляется главным образом в виде синтезирующихся в печени нейтральных жиров и фосфолипидов.
10
