
Гипоталамус
Гипоталамус (hypothalamus) занимает вентральный отдел промежуточного мозга. В его состав входит комплекс образований, расположенных под дном III желудочка. Гипоталамус спереди ограничивается зрительным перекрестом (хиазмой), латерально – передней частью субталамуса, внутренней капсулой и зрительными трактами, отходящими от хиазмы.
В гипоталамусе различают большую по размерам переднебоковую часть и меньшую заднюю часть. Гипоталамус кроме того включает в себя преоптическую область, серый бугор и воронку с гипофизом, пограничную (терминальную) мозговую пластинку, сосцевидные (маммиллярные) тела. Микроскопически в гипоталамусе выделяют до 40 парных ядер, которые подразделяются на несколько групп. Сзади гипоталамус является ростральным продолжением покрышки среднего мозга.
Рис.12. Гипоталамус и гипофиз на срединном разрезе головного мозга.
Серый бугор – это тонкая, выпуклая снизу часть нижней стенки III желудочка, расположенная между перекрестом зрительных нервов спереди и сосцевидными телами сзади. В стенке серого бугра расположены вегетативные ядра, которые причисляют к эмоциогенным зонам мозга. Истонченное продолжение передней стенки серого бугра кверху и назад представляет собой пограничную пластинку, образующую переднюю стенку III желудочка. Вентрально и чуть кпереди серый бугор образует воронку с присоединенным к ней гипофизом. Подбугорная область расположена под таламусами чуть выше серого бугра и частично внутри между его стенками. Сверху она отделена от таламусов гипоталамической бороздой. Подбугорная область содержит множество ядер, функциональная роль которых очень важна.
В гипоталамусе выделяют три основные группы ядер:
1) Передняя группа содержит медиальное преоптическое, супрахиазматическое, супраоптическое, паравентрикулярное и переднее гипоталамическое ядра. Паравентрикулярное ядро располагается под эпендимой вдоль стенки III желудочка, преоптическое ядро – спереди ближе к латеральной стенке гипоталамуса над серым бугром, группа супраоптических и супрахиазматических ядер – чуть ниже над хиазмой и зрительным трактом своей стороны. В
нейронах паравентрикулярного и супраоптического ядер образуется нейросе-
крет, который по их аксонам перемещается в задний отдел гипофиза, или нейрогипофиз, где высвобождается в виде нейрогормонов. вазопрессина и окситоцина, поступающих в кровь. Вазопрессин, или антидиуретический гормон, стимулирует обратное всасывание (реабсорбцию) воды в почечных канальцах. Повреждение передних ядер гипоталамуса приводит к прекращению выделения вазопрессина, вследствие чего развивается несахарный диабет. Окситоцин оказывает влияние на мускулатуру матки.
2) Средняя (или туберальная) группа включает в себя дорсомедиальное, вентромедиальное, аркуатное (дугообразное) и латеральное гипоталамические ядра;
3) Задняя группа включает в себя супрамаммиллярное, премаммиллярное, маммиллярные ядра, задние гипоталамическое и перифорникатное ядра.
Ядра гипоталамуса образуют многочисленные связи друг с другом, а также с выше- и нижележащими структурами головного мозга. Главные афферентные пути в гипоталамус идут от лимбической системы, коры больших полушарий, базальных ганглиев и ретикулярной формации ствола. Основные эфферентные пути гипоталамуса идут в ствол мозга – его ретикулярную формацию, моторные и вегетативные центры, в вегетативные центры спинного мозга. От маммиллярных тел волокна направляются к передним ядрам таламуса и далее, в лимбическую систему, от супраоптического и параветрикулярного ядер – к нейрогипофизу, от вентромедиального и аркуатного ядер к аденогипофизу, а также эфферентные выходы к лобной коре и полосатому телу.
Важной физиологической особенностью гипоталамуса является высокая проницаемость его сосудов для различных веществ, в том числе и для крупных полипептидов. Это обусловливает большую чувствительность гипоталамуса к сдвигам во внутренней среде организма и способность реагировать на колебания концентрации гуморальных факторов. В гипоталамусе по сравнению с другими структурами головного мозга имеется самая мощная сеть капилляров (до 2500 капилляров/мм2) и самый большой уровень локального кровотока.
Функции гипоталамуса. Гипоталамус является многофункциональной системой, обладающей широкими регулирующими и интегрирующими влияниями. Однако важнейшие функции гипоталамуса трудно соотнести с его отдельными ядрами. Как правило, отдельно взятое ядро имеет несколько функций, а отдельно взятая функция локализуется в нескольких ядрах. В связи с этим физиология гипоталамуса рассматривается обычно в аспекте функциональной специфики его различных областей и зон.
Гипоталамус является высшим центром интеграции вегетативных функций. Изучение физиологической роли гипоталамуса с начала XX века и по настоящее время показало, что при раздражении или разрушении его структур, как правило, происходит изменение вегетативных функций организма. Многолетние исследования швейцарского физиолога В.Гесса доказали наличие в гипоталамусе двух функционально различных зон регуляции вегетативной сферы.
Стимуляция задней области гипоталамуса вызывала комплекс вегетативных реакций, характерный для симпатической нервной системы: увеличение частоты и силы сердечных сокращений, подъем артериального давления, повышение температуры тела, расширение зрачков, гипергликемию, торможение перистальтики кишечника и другие реакции. Полученные данные свидетельствуют о роли заднего гипоталамуса в интеграции деятельности различных симпатических центров. Эта область была названа Гессом эрготропной системой мозга, обеспечивающей мобилизацию и расходование энергетических ресурсов организма при активной его деятельности.
Таблица.1
Главные функции отделов гипоталамуса
Функции |
Передний гипоталамус и преоптическя область |
Промежуточный гипоталамус |
Задний гипоталамус |
Нормальные Регуляция цикла Энергетический Поддержание
сон/бодрствование, и водный баланс, уровня сознания,
терморегуляция, эндокринные функции. терморегуляция.
эндокринные функции.
Острые Бессонница, Гипертермия, Сонливость,
поражения гипертермия, несахарный эмоциональные
несахарный диабет, и вегетативные
диабет эндокринные нарушения,
нарушения пойкилотермия.
Хронические Бессонница, Нарушения памяти, Эмоциональные
поражения сложные эндокринные эмоциональные расстройства нарушения,
расстройства гиперфагия, ожирение, потеря аппетита,
(раннее половое эндокринные нарушения. истощение,
созревание), отсутствие
эндокринные расстройства, чувства жажды.
гипотермия,
отсутствие чувства жажды
Раздражение преоптической области и переднего гипоталамуса сопровождалось признаками активации парасимпатической нервной системы: урежением ритма сердца, снижением артериального давления, сужением зрачков, увеличением перистальтики и секреции желудка, кишечника и прочего. Эта область гипоталамуса была обозначена В.Гессом как трофотропная система, обеспечивающая процессы отдыха, восстановления и накопления энергетических ресурсов организма. Однако в дальнейшем было показано, что эрготропная и трофотропная области перекрывают друг друга, и можно только говорить о преобладании их в заднем и переднем гипоталамусе соответственно. Таким образом, приведенные данные свидетельствуют об интеграции вегетативных (симпатических и парасимпатических) центров в пределах гипоталамуса.
Вместе с тем на уровне гипоталамуса происходит не только интеграция деятельности различных вегетативных центров, но и включения их как компонента в более сложные физиологические системы различных форм биологического поведения, направленного на выживание организма.
Поддержания гомеостаза и сохранения вида. Вазомоторные вегетативные реакции, обеспечивающие саморегуляцию артериального давления, осуществляются сосудодвигательным центром продолговатого мозга, тогда как вазомоторные реакции, связанные с терморегуляцией, эмоциями, агрессивно-оборонительным поведением, реализуются на уровне гипоталамуса и более высоких центров.
Гипоталамо-гипофизарная система. Кроме вегетативного канала регуляции внутренней среды организма гипоталамус имеет мощный гуморальный путь реализации эффекторных реакций. В этом плане главную роль играет взаимосвязь гипоталамуса с гипофизом. Клетки многих ядер гипоталамуса обладают нейросекреторной функцией и могут превратить нервный импульс в эндокринный секреторный процесс.
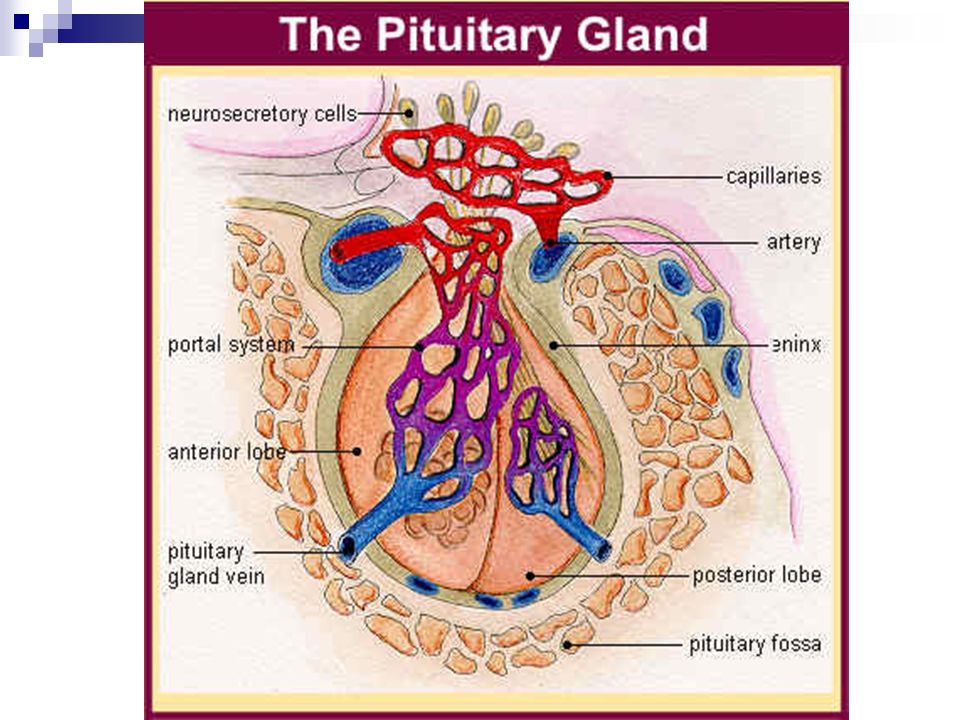
Рис.13. Гипофиз. Видны – передняя доля (anterior lobe), задняя доля (postеrior lobe), нейросекреторные клетки гипоталамуса (neurosecretory cells), вены гипофиза (pituitary gland vein) и портальная сосудистая система (portal system).
Можно выделить две главные эндокринные связи гипоталамуса с гипофизом: гипоталамо-аденогипофизарную и гипоталамо-нейрогипофизарную.
Гипоталамо-аденогипофизарная связь. В 70-х годах XX века усилиями многих исследователей было установлено, что гипоталамус осуществляет контроль над эндокринной функцией аденогипофиза с помощью пептидных гормонов, образуемых мелкоклеточными нейронами в ядрах передней (паравентрикулярное, супраоптическое, супрахиазматическое ядра) и средней (дорсомедиальное, вентромедиальное, аркуатное ядра) групп. В этих ядрах образуется два вида пептидов: одни стимулируют образование и выделение гормонов аденогипофиза и называются рилизинг-гормонами (или либеринами), другие тормозят образование гормонов аденогипофиза и называются статинами. Известны пять либеринов: гонадолиберин стимулирует секрецию лютеинизирующего и фолликулостимулирующего гормонов, кортиколиберин – секрецию АКТГ, тиролиберин – секрецию тиреотропного гормона и пролактина, соматолиберин – секрецию соматотропного гормона, меланолиберин – секрецию меланоцитостимулирующего гормона. Тормозят секрецию аденогипофизарных гормонов: соматостатин, пролактостатин, меланостатин.
Либерины и статины поступают путем аксонного транспорта в срединное возвышение гипоталамуса и выделяются в кровь первичной сети капилляров, образованной разветвлениями верхней гипофизарной артерии. Далее с током крови они поступают во вторичную сеть капилляров, расположенную в аденогипофизе и действуют на его секреторные клетки. Через эту же капиллярную сеть гормоны аденогипофиза поступают в кровоток и достигают периферических эндокринных желез. Эта способность кровообращения гипоталамо-гипофизарной области обозначается как гипофизарная портальная система.
Гипоталамо-нейрогипофизарная связь. В начале 30-х годов XX века было обнаружено, что крупноклеточные нейроны супраоптического и паравентрикулярного ядер гипоталамуса являются эндокринными нейронами, образующими два пептидных гормона: антидиуретический гормон (АДГ, вазопрессин) и окситоцин.
Эти гормоны посредством аксонного транспорта поступают и депонируются в окончаниях аксонов, образующих нейроваскулярные синапсы на капиллярах задней доли гипофиза. Потенциал действия эндокринного нейрона запускает механизм перехода гормонов в капиллярную кровь нейрогипофиза и далее в общий кровоток. Основными мишенями для действия АДГ являются дистальные канальцы и собирательные трубочки почек, в которых он увеличивает реабсорбцию воды и сокращение гладких мышц сосудов (происходит сужение сосудов). Поэтому АДГ называют также вазопрессином. Наряду с этим АДГ оказывает влияние на нейроны гипоталамуса, активируя центр жажды и питьевое поведение. Основным физиологическим эффектом окситоцина является усиление сократительной функции матки и гладкой мускулатуры протоков молочных желез (выделение молока).
Участие гипоталамуса в витальных функциях организма. Гипоталамус принимает участие в обеспечении множества таких функций.
Роль гипоталамуса в терморегуляции. Организм человека, как и высших позвоночных, способен поддерживать постоянную температуру внутренней среды («ядра») тела, несмотря на изменения температуры внешней среды. Проведенные сто лет назад опыты с перерезкой ствола мозга показали, что главной структурой, ответственной за температурный гомеостаз, является гипоталамус.
В гипоталамусе выделено два центра: теплоотдачи и теплопродукции
Центр теплоотдачи локализован в преоптической области и переднем гипоталамусе и включает в себя медиальные преоптические, паравентрикулярные и супраоптические ядра.
Раздражение этих структур вызывает увеличение теплоотдачи в результате расширения сосудов кожи и повышения температуры ее поверхности, увеличения отделения и испарения пота, появления тепловой одышки.
Разрушение центра теплоотдачи приводит к неспособности организма выдерживать тепловую нагрузку.
Центр теплопродукции локализован в заднем гипоталамусе и включает в себя медиальные, латеральные и промежуточные маммиллярные ядра.Его раздражение вызывает повышение температуры тела в результате усиления окислительных процессов, тонуса мышц и появления мышечной дрожи, сужения сосудов кожи. Разрушение этих ядер приводит к потере способности поддерживать температуру тела при охлаждении организма.
Виды нейронов терморегуляторного центра гипоталамуса. С помощью электрофизиологических методик были выявлены нейроны, способные реагировать генерацией потенциалов действия на изменения температуры гипоталамуса – термочувствительные нейроны (термодетекторы). Порого-вая величина изменения температуры для них может быть от 0.2о до 1.0о С. Эти нейроны расположены в основном в центре теплоотдачи, где они составляют от 30 до 70 % нейронов. Значительно меньше их (около 10 %) в центре теплопродукции. Среди термодетекторов количество тепловых нейронов примерно в 3 раза больше, чем холодовых.
Другим видом нейронов терморегуляторного центра являются интегративные нейроны, основная функция которых состоит в суммации температурных сигналов от различных частей организма: терморецепторов гипоталамуса, среднего, продолговатого и спинного мозга, кожи, внутренних органов. Эти нейроны расположены преимущественно в центре теплоотдачи. Переработанная в них информация о тепловом состоянии организма поступает на следующий вид нейронов – эфферентные терморегуляторные нейроны, которые расположены в основном в заднем гипоталамусе. Одни из них регулируют интенсивность механизмов теплопродукции, другие – механизмов теплоотдачи. Еще одна группа нейронов – тормозные интернейроны обеспечивают реципрокность отношений между эфферентными нейронами теплоотдачи и теплопродукции. В центре терморегуляции есть также нейроны, воспринимающие нетемпературные стимулы: влияние экзогенных (бактериальных, вирусных) и эндогенных (интерлейкин 1, простагландин Е1, фактор некроза опухолей) пирогенов.
Роль гипоталамуса в регуляции поведения. Наиболее сложным вариантом интегративной деятельности гипоталамуса является объединение отдельных жизненно важных функций в сложные комплексы, обеспечивающие различные формы биологически целесообразного поведения: пищевого, полового, питьевого, агрессивно-оборонительного и других, направленные на выживание индивидуума и вида. В основе этого поведения лежит возникновение в организме биологических потребностей, которые приводят к формированию в гипоталамических (а также лимбических и корковых) структурах мотивационного возбуждения, что выражается эмоционально окрашенным стремлением человека к удовлетворению соответствующей потребности. Удовлетворение потребности происходит через поведение. Однако в осуществлении даже биологических форм поведения гипоталамус обеспечивает только базовые механизмы. Эмоциональный компонент поведения осуществляется с обязательным участием лимбической системы, корковых структур, а социализция биологического поведения – с участием новой коры, особенно лобной доли.
Пищевое поведение. В клинической практике давно известно, что патологические процессы (опухоль, кровоизлияния, воспаление) в области гипоталамуса вызывают резкие изменения пищевого поведения, то есть увеличение потребления пищи, так и отказ от нее.
Экспериментальные исследования Б.Анада и Дж.Бробека, проведенные в начале 1950-х годов показали, что разрушение небольшой зоны в области латерального гипоталамуса приводило к отказу от приема пищи (афагия), воды (адипсия) и гибели животного от истощения. Электрическая стимуляция этой зоны активизировала пищевое поведение: поиск и прием избыточного количества пищи (гиперфагия), приводящие к ожирению. Эта зона гипоталамуса была названа центром голода.
Разрушение вентромедиальных ядер гипоталамуса приводило к таким же эффектам, которые наблюдались при стимуляции центра голода: поиск пищи, гиперфагия, ожирение. Электрическая стимуляция этих ядер, напротив, прекращала пищевое поведение и прием пищи даже у голодного животного. Эта часть гипоталамуса в зоне вентромедиальных ядер была названа «цент-ром насыщения».
Часть нейронов пищевого центра гипоталамуса обладает хеморецепторной чувствительностью к некоторым веществам (глюкозе, аминокислотам, жирным и органическим кислотам) и гормонам крови (инсулину, гастрину, адреналину и другим), уровень которых влияет на их импульсную активность.
Рис.13. Схема среза, проходящего через гипоталамус крысы, дающая представление о локализации в латеральном гипоталамусе «центра голода». Окаймленные зоны латеральнее свода – области разрушения (B.Anand and J.Brobeck, Proc. Soc. Exp. Biol. Med., v.77, 1951).
Наиболее изучены глюкозочувствительные нейроны гипоталамуса. В «центре голода» выявлены нейроны, которые тормозят свою импульсную активность при увеличении концентрации глюкозы в крови. В «центре насыщения» имеются нейроны, которые, напротив, усиливают свою активность в этих условиях.
Когда была открыта роль латерального и вентромедиального гипоталамуса в регуляции чувства голода, вначале эти участки утвердились, как центры голода и насыщения. Однако с тех пор стало ясно, что понятия «центра голода» и «центра насыщения» оказались слишком упрощенными. Оказалось, что эти участки – не единственные центры голода и насыщения. На самом деле некоторые из эффектов, возникающих голода либо насыщения, можно вызвать, воздействия не на гипоталамус, а на связанными с ним структуры. Например, многие из эффектов воздействия на латеральный гипоталамус можно получить, воздействуя на мезолимбическую дофаминовую систему, которая просто проходит через гипоталамус. Если повредить только этот дофаминэргический пучок волокон, потребление пищи прекращается, что аналогично повреждению латерального гипоталамуса.
В ранних исследованиях эффектов повреждения латерального гипоталамуса, по-видимому, затрагивались не только его собственные нейроны, но и нейроны мезолимбической дофаминовой системы. Речь идет об этом потому, что прекращение потребления пищи при электрической стимуляции или под действием различных препаратов частично зависит также от активации мезолимбической системы.
В ощущениях аппетита и сытости участвует не просто один-два центра, а множество нейроанатомических и нейромедиаторных систем.
Одно из следствий наличия многих нервных систем регуляции аппетита состоит в том, что нельзя остановить потребление пищи, разрушив только один участок. Даже у животных с повреждением латерального гипоталамуса аппетит со временем восстанавливается. Если крыс кормить искусственно несколько недель или месяцев после повреждения, они начинают есть снова, но едят только для поддержания своего веса.
На самом деле крыс можно «защитить» от обычного сокращения количества пищи, наступающего после повреждения латерального гипоталамуса, если перед повреждением их посадить на диету, снижающую их вес (рис.3.49).
Рис.14. Изменение массы тела при повреждении латерального гипоталамуса. Перед операцией одну группу крыс сажали на голодную диету, а другой группе животных позволяли есть свободно. После операции ранее голодавшие животные увеличивали потребление пищи и свой вес, а у свободно питавшейся группы вес падал. У обеих групп через некоторое время (10 дней) вес стабилизировался на одном и том же уровне (По: Powley & Keesey, 1970. Цит: R.C.Atkinson, R.J.Herrnstein, G.Lindzey, R.D.Luce, Eds., Stevens’Handbook of Experimental Psychology, New York: Wiley. v. 1&2, 1988).
Из этого следует, что повреждения гипоталамуса на самом деле не устраняют чувство голода. В действительности повреждения могут опускать или поднимать точку настройки веса, которая обычно контролирует голод. Изменение точки настройки подобно перестройке термостата: система старается достичь нового веса тела. Эффект повреждения вентромедиального гипоталамуса также отвечает этому представлению. Такие животные не набирают вес до бесконе-чности.
Рис.15. Влияние усиленного питания и голодания на массу тела у крыс с повреждением вентромедиального гипоталамуса. После повреждения вентромедиального гипоталамуса крыса начинает переедать и набирает вес, пока он не стабилизируется на новом, более высоком уро-вне. Усиленное питание или голодание изменяют вес только временно, затем вес крысы возвращается на свой стабильный уровень веса (По: Hoebel & Teitelbaum,1966, Цит: R.C.Atkinson, R.J.Herrnstein, G.Lin-dzey, R.D.Luce, Eds., Stevens’Handbook of Experimental Psychology, New York: Wiley. v. 1&2, 1988).
Со временем они останавливаются на новом, более тяжелом весе. В этой нового точке они едят ровно столько, сколько нужно для поддержания новой точки настройки. Но если их посадить на диету, так чтобы их вес упал ниже новой точки настройки, то затем, когда у них будет возможность, они продолжат переедание (рис. 3.50). А после достижения ими своего уровня тучности переедание снова прекратится.
Питьевое поведение. Открытие локализации рецепторных аппаратов жажды было весьма характерным для экспериментальной биологии. Шведский физиолог Б.Андерсен в 1958 году через вживленную в гипоталамус канюлю козы ввел небольшое количество концентрированного солевого раствора. Коза немедленно выпила несколько литров воды. В последущем было установлено, что электрическое раздражение участков гипоталамуса, расположенных сзади и снаружи от супраоптических ядер, вызывает резко выраженную активацию питьевого поведения и потребления воды (полидипсию). Разрушение этой зоны гипоталамуса, названной «центром жажды», напротив, приводит к отказу от приема воды (адипсии), причем эти явления прямо не связаны с изменением секреции антидиуретического гормона.
В дальнейшем было показано, что часть нейронов «центра жажды» обладает осморецептивными свойствами и стимулируется повышением осмотического давления крови. На активность «центра жажды» влияют также импульсы от периферических (сосудистых и тканевых) осморецепторов и концентрация некоторых веществ крови, и в первую очередь – антидиуретического гормона.
Половое поведение. Клинические наблюдения и экспериментальные данные с разрушением или стимуляцией показали, что некоторые структуры гипоталамуса осуществляют регуляцию половой мотивации и поведения. Половая дифференцировка гипоталамуса по женскому или мужскому типу формируется в последние дни внутриутробного развития и первые дни после рождения, хотя реализуется она при половом созревании. Эта дифференцировка приводит к половому диморфизму: в дорсокаудальном отделе медиальной преоптической области у самцов обнаружено компактное скопление клеток – «мужское половое ядро» (MN-RPO), отсутствующее у самок.
Рис.16. На срезе мозга видно «мужское половое ядро», расположенное в дорсальном отделе медиальной преоптической области – MPO.
Кроме того, в гипоталамусе мужского организма функционирует «тонический» половой центр, расположенный в средней области (аркуатные и вентромедиальные ядра). Нейроны этих ядер, выделяя гонадолиберины, оказывают постоянное стимулирующее влияние на секрецию лютеинизирующего и фолликулостимулирующего гормонов гипофиза. В свою очередь, концентрация половых гормонов крови сильно влияет на возбудимость секреторных центров гипоталамуса (повышение их концентрации тормозит секрецию гонадолиберинов и наоборот). В женском организме кроме «тонического» функционирует также «циклический» центр, расположенный в преоптической области и переднем гипоталамусе (особенно в супрахиазматических ядрах) и осуществляющий регуляцию менструального цикла.
В регуляции полового поведения участвуют зоны заднего гипоталамуса и медиальный пучок переднего мозга. Раздражение их в эксперименте с животными, проведенными Дж.Олдсом в средине 1950-х годов, и при операциях у людей показало формирования чувств радости, удовольствия, сопровождающихся эротическими переживаниями. Эти структуры были названы «центром удовольствия» или «позитивного подкрепления». Возбудимость сексуальных центров гипоталамуса существенно зависит от корковых и лимбических влияний, рефлекторной стимуляции с эрогенных генитальных и экстрагенитальных зон, уровня половых гормонов.
Агрессивно-оборонительное поведение. Агрессивные и оборонительные реакции были впервые получены в 1928 году швейцарским физиологом В.Гессом при раздражении различных зон гипоталамуса: передней и задней, вентромедиальной и латеральной областей. Вероятно, это связано с тем, что имеются различные виды агрессивности, направленные на борьбу за самосохранение, лидерство в группе и территорию. Типичный симптомокомплекс этих реакций: яркое проявление отрицательных эмоций (гнев, ярость, страх), резкие вегетативные эрготропные сдвиги, попытки к нападению или бегству. Вместе с тем агрессивное поведение может быть без эмоционального возбуждения («холодная атака») или сопровождаться положительной эмоцией.
Перерезка ствола мозга ниже уровня гипоталамуса ликвидирует агрессивное поведение. При осуществлении агрессивно-оборонительных реакций гипоталамус взаимодействует с центральным серым веществом среднего мозга. В этой структуре Д.Адамс в 1960-х годах обнаружил «нейроны агрессии», которые через гипоталамус запускают реакции агрессии (борьба, драка) и не возбуждаются при других реакциях. При повреждении этих нейронов резко увеличивается порог электрического раздражения гипоталамуса для вызова реакции ярости. Выраженное стимулирующее влияние, вызывающее агрессивное поведение, оказывают андрогены, особенно тестостерон (пороговая величина 1-2 мкг/л).
Перерезка мозгового ствола выше гипоталамуса по данным У.Кеннона показала, что у животных легко возникает агрессивное поведение с реакциями ярости и вегетативными проявлениями симпатического характера. Однако они не направлены на конкретный объект («ложная агрессия и ярость»). Эти данные свидетельствуют о важной роли вышележащих отделов мозга в формировании «осмысленного» агрессивного поведения.
Сон и бодрствование. Изучение больных с поражением гипоталамуса позволило К.Экономо в начале ХХ века сформулировать предположение о том, что «центр сна» расположен в переднем гипоталамусе, а «центр бодрствования» – в заднем. Экспериментальные исследования с повреждением различных участков гипоталамуса проведенные В.Гессом в 1920-1950-е годы, подтвердили эти наблюдения. Электрическое разрушение преоптической области вызывало синхронизацию ЭЭГ и поведенческий сон. В это время активирующая ретикулярная формация ствола реципрокно заторможена. Стимуляция заднего гипоталамуса, напротив, вызывала десинхронизацию ЭЭГ и пробуждение. Пробуждающий эффект заднего гипоталамуса увеличивался при возбуждении активирующей ретикулярной формации ствола мозга.
Роль гипоталамуса не ограничивается только формированием механизмов сна и бодрствования. Выполняя роль внутренних часов, гипоталамус является водителем околосуточного ритма, а важнейшими структурами, обеспечивающими это состояние, являются супрахиазматическое и вентромедиальное ядра, разрушение которых нарушает периодичность многих циркадианных ритмов. Регулируя околосуточные биоритмы, гипоталамус взаимодействует с эпифизом, с которым он имеет выраженные связи.
Роль гипоталамуса в регуляции поведения. Наиболее сложным вариантом интегративной деятельности гипоталамуса является объединение отдельных жизненно важных функций в сложные комплексы, обеспечивающие различные формы биологически целесообразного поведения: пищевого, полового, питьевого, агрессивно-оборонительного и других, направленные на выживание индивидуума и вида. В основе этого поведения лежит возникновение в организме биологических потребностей, которые приводят к формированию в гипоталамических (а также лимбических и корковых) структурах мотивационного возбуждения, что выражается эмоционально окрашенным стремлением человека к удовлетворению соответствующей потребности. Удовлетворение потребности происходит через поведение. Однако в осуществлении даже биологических форм поведения гипоталамус обеспечивает только базовые механизмы. Эмоциональный компонент поведения осуществляется с обязательным участием лимбической системы, корковых структур, а социализция биологического поведения – с участием новой коры, особенно лобной доли.
Пищевое поведение. В клинической практике давно известно, что патологические процессы (опухоль, кровоизлияния, воспаление) в области гипоталамуса вызывают резкие изменения пищевого поведения, то есть увеличение потребления пищи, так и отказ от нее.
Экспериментальные исследования Б.Анада и Дж.Бробека, проведенные в начале 1950-х годов показали, что разрушение небольшой зоны в области латерального гипоталамуса приводило к отказу от приема пищи (афагия), воды (адипсия) и гибели животного от истощения. Электрическая стимуляция этой зоны активизировала пищевое поведение: поиск и прием избыточного количества пищи (гиперфагия), приводящие к ожирению. Эта зона гипоталамуса была названа центром голода.
Разрушение вентромедиальных ядер гипоталамуса приводило к таким же эффектам, которые наблюдались при стимуляции центра голода: поиск пищи, гиперфагия, ожирение. Электрическая стимуляция этих ядер, напротив, прекращала пищевое поведение и прием пищи даже у голодного животного. Эта часть гипоталамуса в зоне вентромедиальных ядер была названа «цент-ром насыщения».
Часть нейронов пищевого центра гипоталамуса обладает хеморецепторной чувствительностью к некоторым веществам (глюкозе, аминокислотам, жирным и органическим кислотам) и гормонам крови (инсулину, гастрину, адреналину и другим), уровень которых влияет на их импульсную активность.
Рис.13. Схема среза, проходящего через гипоталамус крысы, дающая представление о локализации в латеральном гипоталамусе «центра голода». Окаймленные зоны латеральнее свода – области разрушения (B.Anand and J.Brobeck, Proc. Soc. Exp. Biol. Med., v.77, 1951).
Наиболее изучены глюкозочувствительные нейроны гипоталамуса. В «центре голода» выявлены нейроны, которые тормозят свою импульсную активность при увеличении концентрации глюкозы в крови. В «центре насыщения» имеются нейроны, которые, напротив, усиливают свою активность в этих условиях.
Когда была открыта роль латерального и вентромедиального гипоталамуса в регуляции чувства голода, вначале эти участки утвердились, как центры голода и насыщения. Однако с тех пор стало ясно, что понятия «центра голода» и «центра насыщения» оказались слишком упрощенными. Оказалось, что эти участки – не единственные центры голода и насыщения. На самом деле некоторые из эффектов, возникающих голода либо насыщения, можно вызвать, воздействия не на гипоталамус, а на связанными с ним структуры. Например, многие из эффектов воздействия на латеральный гипоталамус можно получить, воздействуя на мезолимбическую дофаминовую систему, которая просто проходит через гипоталамус. Если повредить только этот дофаминэргический пучок волокон, потребление пищи прекращается, что аналогично повреждению латерального гипоталамуса.
В ранних исследованиях эффектов повреждения латерального гипоталамуса, по-видимому, затрагивались не только его собственные нейроны, но и нейроны мезолимбической дофаминовой системы. Речь идет об этом потому, что прекращение потребления пищи при электрической стимуляции или под действием различных препаратов частично зависит также от активации мезолимбической системы.
В ощущениях аппетита и сытости участвует не просто один-два центра, а множество нейроанатомических и нейромедиаторных систем.
Одно из следствий наличия многих нервных систем регуляции аппетита состоит в том, что нельзя остановить потребление пищи, разрушив только один участок. Даже у животных с повреждением латерального гипоталамуса аппетит со временем восстанавливается. Если крыс кормить искусственно несколько недель или месяцев после повреждения, они начинают есть снова, но едят только для поддержания своего веса.
На самом деле крыс можно «защитить» от обычного сокращения количества пищи, наступающего после повреждения латерального гипоталамуса, если перед повреждением их посадить на диету, снижающую их вес (рис.3.49).
Рис.14. Изменение массы тела при повреждении латерального гипоталамуса. Перед операцией одну группу крыс сажали на голодную диету, а другой группе животных позволяли есть свободно. После операции ранее голодавшие животные увеличивали потребление пищи и свой вес, а у свободно питавшейся группы вес падал. У обеих групп через некоторое время (10 дней) вес стабилизировался на одном и том же уровне (По: Powley & Keesey, 1970. Цит: R.C.Atkinson, R.J.Herrnstein, G.Lindzey, R.D.Luce, Eds., Stevens’Handbook of Experimental Psychology, New York: Wiley. v. 1&2, 1988).
Из этого следует, что повреждения гипоталамуса на самом деле не устраняют чувство голода. В действительности повреждения могут опускать или поднимать точку настройки веса, которая обычно контролирует голод. Изменение точки настройки подобно перестройке термостата: система старается достичь нового веса тела. Эффект повреждения вентромедиального гипоталамуса также отвечает этому представлению. Такие животные не набирают вес до бесконе-чности.
Рис.15. Влияние усиленного питания и голодания на массу тела у крыс с повреждением вентромедиального гипоталамуса. После повреждения вентромедиального гипоталамуса крыса начинает переедать и набирает вес, пока он не стабилизируется на новом, более высоком уро-вне. Усиленное питание или голодание изменяют вес только временно, затем вес крысы возвращается на свой стабильный уровень веса (По: Hoebel & Teitelbaum,1966, Цит: R.C.Atkinson, R.J.Herrnstein, G.Lin-dzey, R.D.Luce, Eds., Stevens’Handbook of Experimental Psychology, New York: Wiley. v. 1&2, 1988).
Со временем они останавливаются на новом, более тяжелом весе. В этой нового точке они едят ровно столько, сколько нужно для поддержания новой точки настройки. Но если их посадить на диету, так чтобы их вес упал ниже новой точки настройки, то затем, когда у них будет возможность, они продолжат переедание (рис. 3.50). А после достижения ими своего уровня тучности переедание снова прекратится.
Питьевое поведение. Открытие локализации рецепторных аппаратов жажды было весьма характерным для экспериментальной биологии. Шведский физиолог Б.Андерсен в 1958 году через вживленную в гипоталамус канюлю козы ввел небольшое количество концентрированного солевого раствора. Коза немедленно выпила несколько литров воды. В последущем было установлено, что электрическое раздражение участков гипоталамуса, расположенных сзади и снаружи от супраоптических ядер, вызывает резко выраженную активацию питьевого поведения и потребления воды (полидипсию). Разрушение этой зоны гипоталамуса, названной «центром жажды», напротив, приводит к отказу от приема воды (адипсии), причем эти явления прямо не связаны с изменением секреции антидиуретического гормона.
В дальнейшем было показано, что часть нейронов «центра жажды» обладает осморецептивными свойствами и стимулируется повышением осмотического давления крови. На активность «центра жажды» влияют также импульсы от периферических (сосудистых и тканевых) осморецепторов и концентрация некоторых веществ крови, и в первую очередь – антидиуретического гормона.
Половое поведение. Клинические наблюдения и экспериментальные данные с разрушением или стимуляцией показали, что некоторые структуры гипоталамуса осуществляют регуляцию половой мотивации и поведения. Половая дифференцировка гипоталамуса по женскому или мужскому типу формируется в последние дни внутриутробного развития и первые дни после рождения, хотя реализуется она при половом созревании. Эта дифференцировка приводит к половому диморфизму: в дорсокаудальном отделе медиальной преоптической области у самцов обнаружено компактное скопление клеток – «мужское половое ядро» (MN-RPO), отсутствующее у самок.
Рис.16. На срезе мозга видно «мужское половое ядро», расположенное в дорсальном отделе медиальной преоптической области – MPO.
Кроме того, в гипоталамусе мужского организма функционирует «тонический» половой центр, расположенный в средней области (аркуатные и вентромедиальные ядра). Нейроны этих ядер, выделяя гонадолиберины, оказывают постоянное стимулирующее влияние на секрецию лютеинизирующего и фолликулостимулирующего гормонов гипофиза. В свою очередь, концентрация половых гормонов крови сильно влияет на возбудимость секреторных центров гипоталамуса (повышение их концентрации тормозит секрецию гонадолиберинов и наоборот). В женском организме кроме «тонического» функционирует также «циклический» центр, расположенный в преоптической области и переднем гипоталамусе (особенно в супрахиазматических ядрах) и осуществляющий регуляцию менструального цикла.
В регуляции полового поведения участвуют зоны заднего гипоталамуса и медиальный пучок переднего мозга. Раздражение их в эксперименте с животными, проведенными Дж.Олдсом в средине 1950-х годов, и при операциях у людей показало формирования чувств радости, удовольствия, сопровождающихся эротическими переживаниями. Эти структуры были названы «центром удовольствия» или «позитивного подкрепления». Возбудимость сексуальных центров гипоталамуса существенно зависит от корковых и лимбических влияний, рефлекторной стимуляции с эрогенных генитальных и экстрагенитальных зон, уровня половых гормонов.
Агрессивно-оборонительное поведение. Агрессивные и оборонительные реакции были впервые получены в 1928 году швейцарским физиологом В.Гессом при раздражении различных зон гипоталамуса: передней и задней, вентромедиальной и латеральной областей. Вероятно, это связано с тем, что имеются различные виды агрессивности, направленные на борьбу за самосохранение, лидерство в группе и территорию. Типичный симптомокомплекс этих реакций: яркое проявление отрицательных эмоций (гнев, ярость, страх), резкие вегетативные эрготропные сдвиги, попытки к нападению или бегству. Вместе с тем агрессивное поведение может быть без эмоционального возбуждения («холодная атака») или сопровождаться положительной эмоцией.
Перерезка ствола мозга ниже уровня гипоталамуса ликвидирует агрессивное поведение. При осуществлении агрессивно-оборонительных реакций гипоталамус взаимодействует с центральным серым веществом среднего мозга. В этой структуре Д.Адамс в 1960-х годах обнаружил «нейроны агрессии», которые через гипоталамус запускают реакции агрессии (борьба, драка) и не возбуждаются при других реакциях. При повреждении этих нейронов резко увеличивается порог электрического раздражения гипоталамуса для вызова реакции ярости. Выраженное стимулирующее влияние, вызывающее агрессивное поведение, оказывают андрогены, особенно тестостерон (пороговая величина 1-2 мкг/л).
Перерезка мозгового ствола выше гипоталамуса по данным У.Кеннона показала, что у животных легко возникает агрессивное поведение с реакциями ярости и вегетативными проявлениями симпатического характера. Однако они не направлены на конкретный объект («ложная агрессия и ярость»). Эти данные свидетельствуют о важной роли вышележащих отделов мозга в формировании «осмысленного» агрессивного поведения.
Сон и бодрствование. Изучение больных с поражением гипоталамуса позволило К.Экономо в начале ХХ века сформулировать предположение о том, что «центр сна» расположен в переднем гипоталамусе, а «центр бодрствования» – в заднем. Экспериментальные исследования с повреждением различных участков гипоталамуса проведенные В.Гессом в 1920-1950-е годы, подтвердили эти наблюдения. Электрическое разрушение преоптической области вызывало синхронизацию ЭЭГ и поведенческий сон. В это время активирующая ретикулярная формация ствола реципрокно заторможена. Стимуляция заднего гипоталамуса, напротив, вызывала десинхронизацию ЭЭГ и пробуждение. Пробуждающий эффект заднего гипоталамуса увеличивался при возбуждении активирующей ретикулярной формации ствола мозга.
Роль гипоталамуса не ограничивается только формированием механизмов сна и бодрствования. Выполняя роль внутренних часов, гипоталамус является водителем околосуточного ритма, а важнейшими структурами, обеспечивающими это состояние, являются супрахиазматическое и вентромедиальное ядра, разрушение которых нарушает периодичность многих циркадианных ритмов. Регулируя околосуточные биоритмы, гипоталамус взаимодействует с эпифизом, с которым он имеет выраженные связи.
Поражения функций ядер гипоталамуса. У человека нарушения деятельности гипоталамуса бывают связаны, главным образом, с опухолевыми, травматическими или воспалительными поражениями. Подобные поражения могут быть весьма ограниченными, захватывая передний, промежуточный или задний отдел гипоталамуса. У таких больных наблюдаются сложные функциональные расстройства.
Картина поражения ядер гипоталамуса крайне полиморфна, что находит объяснение в многообразии функций, регулируемых этим отделом мозга. Наиболее закономерно поражение гипоталамуса проявляется нарушением деятельности внутренних органов и сосудистой системы, расстройством терморегуляции, нарушением водного, минерального, жирового и белкового обмена, дисфункцией желез внутренней секреции, нарушением сна и бодрствования. Различная комбинация этих дисфункций определяет конкретный характер их проявлений. Особенно типичны жажда, изменение аппетита (булимия или анорексия), сонливость или бессонница, головная боль, боли в области сердца, сердцебиение, затруднение дыхания.
Одним из наиболее ярких и часто встречающихся поражений является нейроэндокринный синдром. В основе его лежит эндокринная, как правило, плюригландулярная дисфункция, сочетающаяся с вегетативными нарушениями. В эту группу входят такие очерченные клинические формы, как синдром Иценко-Кушинга, адипозо-генитальная дистрофия, несахарный диабет, дисфункция половых желез (ранний климакс, импотенция). Вегето-сосуди-стый синдром включает в себя следующие симптомы: повышенную потливость, высокую сосудистую возбудимость (склонность к сердцебиениям, неустойчивому артериальному давлению), спазмы мозговых, сердечных и периферических сосудов. Наблюдается также неустойчивость деятельности желудочно-кишечного тракта. Для описываемого варианта диэнцефального синдрома типичны периодические вегетососудистые пароксизмы (кризы). Кризы могут быть редкими (раз в несколько месяцев) и очень частыми (несколько раз в день).
Несколько реже встречается нейродистрофический синдром: трофические расстройства кожи (зуд, сухость, нейродермит, язвы, пролежни) и мышц, поражение внутренних органов (язвы и кровотечения по ходу желудочно-кишечного тракта), костей (остеомаляция, то есть их размягчение или, наоборот, склерозирование). Нарушается также солевой обмен, в результате чего иногда имеются оссификация мышц в виде интенсивного откладывания солей в мышцах, а также внутритканевые отеки.
Все эти симптомы укладывается в понятие диэнцефальный синдром, который, кроме прочего, проявляется также нарушением сна (бессонница) и бодрствования (сонливость днем), постоянным небольшим повышением температуры тела – субфебрилитетом, перемежающегося с гипертермическими приступами. Как правило, отмечаются астено-невротические явления, включающие вегетативные, эндокринные и трофические расстройства. Анимальная неврологическая симптоматика при диэнцефальном синдроме, как правило, представлена лишь негрубыми рассеянными признаками.
Диэнцефальный синдром характеризуется вегетососудистой дистонией, которая не значится в списке заболеваний, но приносит страдающим от нее немало проблем. У нее много имен, еще – нейроциркуляторная дистония, психовегетативный синдром, вегетоневроз, синдром вегетативной дисфункции… Ее даже не считают болезнью, но людей, которым «повезло» столкнуться с этим недугом, нельзя назвать здоровыми. Их жизнь в период обострения, похожа на ад, а врачи только разводят руками и просят «смириться». Однако у больного мир уплывает из под ног, сердце начинает бешено стучать, периодически замирая, руки и ноги покрываются холодным потом, давление то падает, то взлетает, в горле появляется ком, а легкие сопротивляются очередному вдоху…
Через 5 мин. такого состояния человека охватывает паника и ощущение, что смерть с косой уже стоит за плечами. И вот тогда взять себя в руки уже практически невозможно. Длится этот ужас от нескольких минут до нескольких часов. И здорово, если рядом с вами окажется человек, который может вам помочь.
Что же происходит при диэнцефальном синдроме? Гипоталамус в обычном состоянии поддерживает на оптимальном уровне артериальное давление, частоту сердечных сокращений, регулирует теплоотдачу, ширину дыхательных путей, отвечает за реакцию зрачков на свет, активность пищеварительной системы, образование мочи и так далее. Но у некоторых особей ядра гипоталамуса могут находиться в состоянии гиперреактивности. Именно, гиперреактивность гипоталамических структур виновна во всех бедах этих людей.
У человека со здоровой вегетативной нервной системой адаптация происходит плавно и незаметно. А у больного дистонией при любом изменении, например, при смене погоды, принятии душа, попадании в душное помещение, появлении нового запаха – вплоть до духов, после чашечки кофе, при плохих или хороших новостях либо резком звуке, организм реагирует так, как если бы ему угрожала смертельная опасность.
Причем сложность ситуации в том, что после такой атаки гипоталамус срочно решает вернуть все на круги своя и также резко отвечает отклонением, но теперь уже – в другую сторону. Таким образом, человека, страдающего диэнцефальным синдромом, постоянно бросает из огня да в полымя. И не удивительно, что после каждого приступа он чувствует себя как «выжатый лимон».
Следует, однако, указать на неоправданную тенденцию к гипердиагностике диэнцефального синдрома: подавляющее число больных с подобным диагнозом на самом деле страдают депрессией или неврозом с выраженными вегетативными расстройствами. Среди последних чаще других встречаются так называемые панические атаки: внезапно возникающее сердцебиение, озноб, иногда нарушение дыхания. Такие пароксизмы сопровождаются чувством страха смерти и обычно завершаются обильным мочеиспусканием, и, иногда, поносом.
Частым симптомом при различных поражениях гипоталамуса является ожирение. Различают два вида – гипоталамическое и эндокринное ожирение.
Гипоталамическое ожирение наблюдается при заболеваниях с поражением гипоталамуса (при опухолях, в исходе травм, инфекций). Для этого вида ожирения характерно быстрое развитие тучности. Отложение жира отмечается преимущественно на животе (в виде фартука), ягодицах, бедрах. Нередко возникают трофические изменения кожи: сухость, белые или розовые полосы растяжения (стрии).
По клиническим симптомам (например, головной боли, расстройстве сна) и данным неврологического обследования обычно удается установить патологию головного мозга. Как проявление гипоталамических расстройств наряду с ожирением наблюдаются различные признаки вегетативной дисфункции – повышение АД, нарушения потоотделения и другое.
Эндокринное ожирение развивается у больных при некоторых заболеваниях эндокринной природы, например, гипотиреозе, болезни Иценко-Кушинга, симптомы которых преобладают в картине заболевания. При осмотре наряду с ожирением, которое обычно характеризуется неравномерным отложением жира на теле, выявляются другие признаки гормональных нарушений (например, маскулинизация или феминизация, увеличение молочных желез – гинекомастия, рост терминальных волос по мужскому типу – гирсутизм), на коже обнаруживаются полосы – стрии.
Особенно яркими являются картины поражения гипофиза, так как нарушения его функций сопровождаются избыточным либо недостаточным образованием гормонов. Причиной их могут быть гиперстимуляция рилизинг-гормонами, сопровождающаяся гиперфункцией соответствующих клеток и их последующей разрастанием – гиперплазией, которая может завершиться формированием железистой опухоли – аденомы, а также развитием первичных опухолей гипофиза.
При поражении гипофиза возникают множество разнообразных синдромов. Так, например, гиперпродукция соматотропина при наличии в гипофизе опухоли – соматотропиномы ведет к развитию акромегалии или гигантизма в детском и юношеском возрасте, а недостаточная его продукция – к карликовости. Гиперпролактинемия функционального или опухолевого происхождения сопровождается развитием галактореи и снижения функций женских половых органов – аменореи и гипогонадизма. Гиперпролактинемия может быть связана с синдромом, так называемого пустого турецкого седла, развивающегося, как правило, при разрушении его спинки. Обычно он наблюдается у тучных женщин, нередко страдающих артериальной гипертензией. При этом отмечаются головные боли, головокружения, сочетающиеся с расстройством менструального цикла, иногда зрения. Первичное нарушение продукции гонадотропинов вызывает расстройства половых функций: раннее половое созревание у детей, а при выпадении гонадотропной функции – гипогонадотропный гипогонадизм. Чревато расстройствами половых функций также нарушение циклической гонадотропной функции гипофиза у женщин. Гиперплазия железистых клеток гипофиза приводит к развитию болезни Иценко – Кушинга, а выпадение кортикотропной функции – к недостаточности надпочечников. Недоразвитие – гипоплазия и атрофия аденогипофиза, а также разрушение его паренхимы патологическим процессом вызывают пангипопитуитаризм, сопровождающийся выпадением функции периферических эндокринных желез, и гипофизарную кахексию (истощение). Разрушение задней доли гипофиза, повреждение его ножки или поражение ядер переднего гипоталамуса ведут к возникновению диабета – несахарного мочеизнурения.
Нарушение функций гипофиза выявляют на основании анализа клинической картины в динамике и данных дополнительных методов исследования – радиоиммунологического (определение уровня гормонов в крови), рентгенологических (краниографии, компьютерной томографии), а также нейроофтальмологических (оценка остроты зрения и полей зрения, зрачковых рефлексов, осмотр глазного дна). Сочетание симптомов эндокринных нарушений с рентгенологическим симптомокомплексом, например увеличением турецкого седла, свидетельствует о возможном развитии опухолевого процесса в гипофизе.
Болезненные проявления опухолей зависит от характера, локализации, направления и темпа роста. На ранней стадии заболевания опухоль растет в полости турецкого седла и нередко проявляется лишь эндокринными расстройствами. В дальнейшем присоединяются нарушения зрения и различные анатомические изменения в области гипоталамуса, выявляемые при рентгенологическом исследовании (изменение размеров и формы турецкого седла, разрушение его спинки, смещение хиазмальных цистерн и прочее). На поздней стадии появляются симптомы поражения головного мозга. При краниофарингеомах выявляются включения солей кальция, как в ткани самой опухоли, так и в стенках ее капсулы. Дифференцировать опухоли гипофиза у женщин необходимо с синдромом пустого турецкого седла, для которого характерны увеличение турецкого седла, артериальная гипертензия, хиазмальный синдром (нарушение зрения), но функция гипофиза при этом обычно не нарушена, хотя и имеется гиперпролактинемия, сопровождающаяся выделениями из молочных желез.
