
ИДЗ2
.docxМИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
Санкт-Петербургский государственный
электротехнический университет
«ЛЭТИ» им. В.И. Ульянова (Ленина)
Кафедра Физической химии
Химия
Индивидуальное домашнее задание № 2
Вариант № 14
Выполнил: студент гр. № 9493 Скотаренко Д.Д.
Проверил: доцент кафедры Рахимова О.В.
Оценка:
Санкт-Петербург
2020
Индивидуальное домашнее задание №2.
Задание №1:
Найти
стандартную энтальпию образования
жидкого бензола
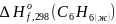 ,
если известно, что при сгорании 3,6 г.
бензола до
,
если известно, что при сгорании 3,6 г.
бензола до
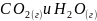 выделяется 140.194 кДж теплоты. Стандартные
энтальпии образования
выделяется 140.194 кДж теплоты. Стандартные
энтальпии образования
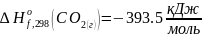 ,
,
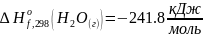 .
.
Запишем
реакцию, энтальпию которой нам надо
найти:
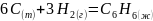 -
-
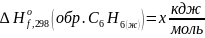 .
.
Запишем имеющиеся у нас данные:
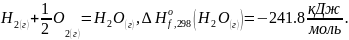
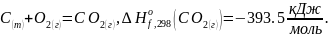
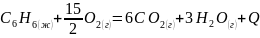
Мы
знаем теплоту сгорания 3,6 г. жидкого
бензола. Нам необходимо найти стандартную
энтальпию сгорания 1 моль жидкого
бензола. Молярная масса бензола:
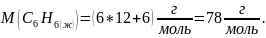 Значит, 1 моль бензола – 78 грамм.
Значит, 1 моль бензола – 78 грамм.
Составим пропорцию:
3,6 г. бензола при сгорании выделяют 140,194 кДж теплоты
78 г. бензола при сгорании
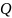 кДж теплоты
кДж теплоты
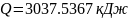 (Данные из справочника: Q=3135,58
кДж)
(Данные из справочника: Q=3135,58
кДж)
Изменение энтальпии, так как реакция
экзотермическая, будет
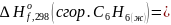
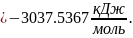
(Данные
из справочника: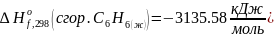
Теперь запишем соотношение для реакции горения:
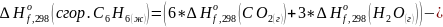
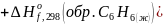
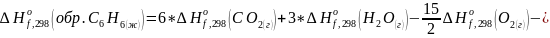
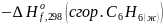
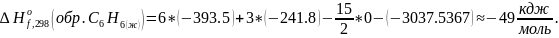
Либо, если взять данные из справочника:
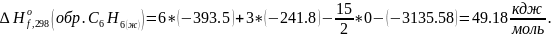
С этими данными получается, как в справочнике. Мне кажется, что, либо в задании ошибка, либо так специально и задумано, но, на всякий случай, приведу оба варианта. Ответ: -49 кДж/моль (по заданию), 49.18 кДж/моль (по справочным данным).
2. Пользуясь справочными данными, определить, в каком направлении пойдёт процесс:
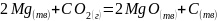
При
T=500K и
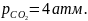
Определим
стандартное изменение свободной энергии
Гиббса
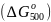 .
Запишем формулу:
.
Запишем формулу:
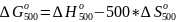
Подставим выражения для изменения энтальпии образования и изменения значения энтропии реакции при 500К:
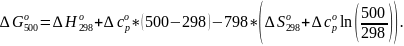
Определим
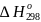 ,
,
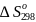 ,
,
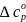 :
:
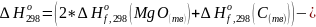
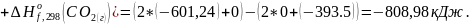
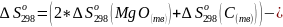
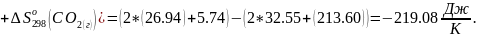
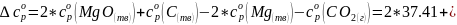
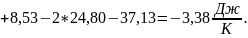
Получим изменение свободной энергии Гиббса:
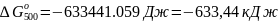
Так
как
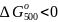 ,
то реакция пойдёт в прямом направлении.
,
то реакция пойдёт в прямом направлении.
3. При 1000К катализатор понижает энергию активации на 30000 кДж/моль. Во сколько раз возрастает скорость реакции?
Воспользуемся уравнением Аррениуса:
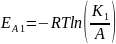
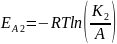
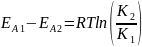
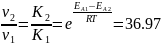
Следовательно, скорость химической реакции увеличилась в 36,97 раз.
4. Как изменится скорость реакции 2А+3В=C+D, если в смеси концентрацию вещества А уменьшили в 3 раза и снизили температуру с 410 до 370 К? Энергия активации 180000 Дж/моль.
Воспользуемся соотношениями для скоростей реакции и уравнениями Аррениуса:
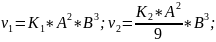
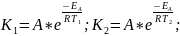
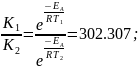
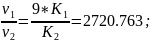
Следовательно, скорость реакции уменьшилась в 2720.63 раз.
