
4_Lektsia_Mobilizatsia_lipidov_iz_zhirovoy_tkani
.pdf
МЕТАБОЛИЗМ ЖИРНЫХ КИСЛОТ
β-Окисление жирных кислот
β-окисление – это аэробный процесс катаболизма жирных кислот,
протекающий в матриксе митохондрий путём последовательного отщепления двууглеродных фрагментов в виде ацетил-SКоА.
Окислению жирных кислот в митохондриях предшествует: 1. Активация ВЖК в цитоплазме.
2.Транспорт её через мембрану в матрикс митохондрий.
Активация жирных кислот
Активации подвергаются свободные жирные кислоты, поступающие в цитозоль из двух источников:
1.В неэтерифицированной форме (НЭЖК) в комплексе с альбумином доставляются кровью;
2.Другим источником ВЖК служат цитозольные ТАГ, расщепляющиеся под действием цитозольной ТАГ-липазы.
НЭЖК+ |
Цитозольные |
|
альбумины |
ТАГ |
ЛП |
|
липаза |
Ацетил- |
|
|
|
Свободные жирные |
SKoA |
|
|
||
кислоты |
|
|
Формирование пула свободных жирных кислот клеток
В активации принимают участие:
1.АТФ;
2.Коэнзим А (HSKoA);
3.Фермент – ацил-КоА-синтетаза (тиокиназа).
Реакция протекает в области наружной мембраны митохондрии.
Существует несколько изоформ фермента ацил-SKoA-синтетазы: одни катализируют активацию жирных кислот, содержащих 2-3 атома углерода,
другие – от 4 до 12 атомов, третьи – от 12 и более атомов углерода.

Активация высших жирных кислот
В результате активации ВЖК образуется:
1.Ацил–SКoA (общее название активированной формы жирной кислоты) с
высокоэнергетической тиоэфирной связью;
2.АМФ;
3.ФФн (пирофосфат).
На последней ступени процесс легко обратим, так как изменение свободной энергии очень мало (ΔG = 0,2 ккал/моль). Однако, присутствующая в среде пирофосфатаза расщепляет макроэргическую связь пирофосфата и обеспечивает необратимость реакции активации жирной кислоты.
Транспорт ацил-KoA в матрикс митохондрий
Переносчиком ацильных групп (ацил-KoA) из цитоплазмы в матрикс митохондрий является карнитин. Карнитин – синтезируется из лизина и метионина с участием витамина С. Он имеет заряд, что помогает карнитину двигаться между заряженными структурами мембран.
R - CO - S - KoA +(CH3)3N+ - CH2 –CH (OH) - CH2 –CO OH ↔ HSKoA +
Структура ацилкарнитина

В митохондриальную ацилкарнитин – транспортную систему входят:
1.Транслоказа – белок, который встроен во внутреннюю мембрану митохондрий. Он осуществляет транспорт карнитина через эту мембрану.
2.Два фермента, катализирующие присоединение и отщепление ацильного остатка к карнитину. Это ацилкарнитинтрансфераза I, локализованная в
наружной мембране, и |
ацилкарнитинтрансфераза II, находящаяся |
на |
внутренней поверхности внутренней мембраны митохондрий. |
|
|
Карнитин соединяется |
с ацил-S-KoA с образованием ацил-карнитина (E – |
|
ацилкарнитин-трансфераза |
I) и высвобождением НS-КоА, который уходит в |
|
цитозоль. Ацил-карнитин проходит через межмембранное пространство к наружной стороне внутренней мембраны митохондрии и транспортируется с помощью транслоказы на внутреннюю поверхность внутренней мембраны митохондрий, где фермент – ацил-трансфераза II катализирует перенос ацильного остатка на внутри митохондриальный КоА-SH с образование ацил-S-KoA и
свободного карнитина. Ацил-SKoA включается в реакции β-окисления, а
свободный карнитин возвращается на наружную сторону внутренней мембраны митохондрий той же транслоказой.
Транспорт ацил-КоА через митохондриальную мембрану в матрикс
Активация низших жирных кислот (с количеством углеродных атомов от 4 до
11) и их окисление могут происходить в митохондриях независимо от карнитина.
Длинноцепочечные ВЖК не могут проникать в митохондрии, если не образуют ацилкарнитинпроизводных и они нуждаются в переносчике (карнитин).
β-окисление ЖК
Цикл β-окисления состоит их четырёх реакций.
1. Реакции дегидрирования (фермент –ацил-КоА-дегидрогеназа) происходит
отщепление двух атомов водорода от α- и β-углеродных атомов с образованием
2 транс-еноил-КоА и восстановленный ФАДН2. Его окисление в дыхательной цепи обеспечивает синтез 2-х АТФ. Природные ненасыщенные ЖК образуют
цис-конфигурацию двойной связи.
2. Реакции гидратации (фермент – гидратаза), образуется L-3-гидроксиацил-
КоА. У ненасыщенных жирных кислот образуется D-изомер.
3. Реакции дегидрирования (фермент: 3-гидроксиацил-КоА-дегидрогеназа,
кофермент – НАД+). В ходе реакции образуется 3-кетоацил-КоА. В результате НАД+ переходит в НАДН+Н+. Который в дыхательной цепи обеспечивает синтез
3 АТФ.
4. Тиолитическое расщепление 3-кетоацила-КоА, на ацетил-SКоА и укороченный ацил-SКоА (фермент – тиолаза).
Укороченный ацил-SКоА вступает в следующий цикл, а ацетил-S-КоА используется либо на синтез кетоновых тел, либо сгорает в ЦТК.
Этапы катаболизма ЖК на примере полного окисления С16:0
1 этап. β-окисление – сопряжен с переносом электорнов и протонов по дыхательной цепи от ФАДН2 и НАДН+Н+ к О2.
Ацил-SКоА
ФАДН2 → 2АТФ НАДН+Н+ → 3АТФ
Ацетил-SКоА
1 цикл β-окисления обеспечивает синтез 5 молекул АТФ.

Количество циклов вычисляется по формуле (n/2 – 1), где n = числу атомов углерода в молекуле жирной кислоты.
При распаде С16:0 число циклов = 7:
(16/2 - 1) = 8-1 = 7
7 циклов → 7×5 = 35 АТФ.
2 этап: Цикл трикарбоновых кислот Ацетил-SКоА
ЦТК
ЦПЭ
12 АТФ
3 этап. Окислительное фосфорилирование
1 молекула ацетил-КоА, проходя через ЦТК, сопряженного с дыхательной цепью, обеспечивает синтез 12 АТФ.
Количество молекул ацетил-SКоА вычисляется по формуле n/2, где n - числo
атомов углерода.
При распаде С16:0 образуется: 16/2 = 8 молекул ацетил-КоА. 8 молекул ацетил-КоА дают 8×12 = 96 АТФ.
Итого: 35 АТФ + 96 АТФ – 1 АТФ = 130 АТФ (950 ккал)
β-окисление ОПК на активацию ВЖК
Суммарная реакция β-окисления активированной пальмитиновой кислоты можно представить следующим образом.

O
βα //
R-CH2-CH2-C-SKoA |
|
ацил-SKoA |
Е1 |
ФАД |
1 |
|
|
|
ацил-КоА-дг. |
|
ЦПЭ |
|
|
|
|
ФАДН2 |
2АТФ |
O
βα //
|
R-CH=CH-C-SKoA |
2-трансеноил-SKoA |
Е2 |
Н-ОН (Н2О) |
2 |
гидратаза |
|
|
O
βα //
R-CH - CH2-C-SKoA |
L-3-гидроксиацил-SKoA |
||
׀ |
|
|
|
ОН |
НАД+ |
|
|
Е3 |
|
ЦПЭ |
|
3-гидроксиацил-КоА дг. |
НАДН+Н+ |
3АТФ |
3 |
O
βα //
R-C |
|
CH2-C-SKoA |
3-кетоацил-SKoA |
|
|||
// |
|
|
|
О |
|
|
|
Е4
тиолаза
H-SKoA |
4 |
|
|
О |
|
// |
|
СН3-С-SKоА |
синтез |
( ацетил-SКоА) |
кетоновых тел |
|
ЦТК → АТФ, СО2, Н2О |
O
//
R-C-SKoA
укороченный ацил (кетоацил-SKoA)
Рис. 34. Схема β-окисления ВЖК
Окисление ненасыщенных ВЖК
Окисление ненасыщенных высших жирных кислот идёт идентично этапам β-
окисления насыщенных ЖК, однако имеет некоторые особенности.
1. Если окислению подвергаются мононенасыщенные ЖК, то оборот цикла β-
окисления участка ВЖК, содержащего одну двойную связь, требует участия одного дополнительного фермента – еноил-КоА-изомеразы, который превращает цис-конфигурацию в транс-конфигурацию и одновременно смещает положение двойной связи вправо (или в α-положение). Дальнейшее окисление идёт аналогично окислению насыщенных ВЖК.
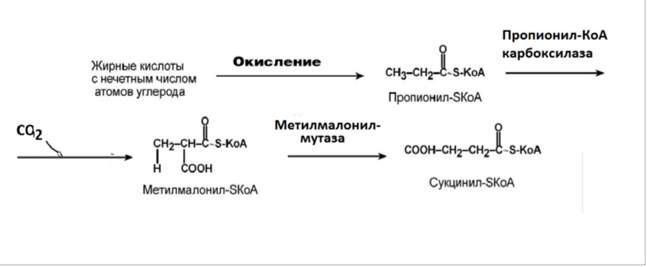
Окисление ВЖК с нечетным числом атомов углерода в молекуле.
1.Если окислению подвергаются полиненасыщенные ВЖК, то первая двойная связь подвергается окислению, аналогичному мононенасыщенным ВЖК.
2.Фрагмент углеродной цепи между двумя двойными связями подвергается дальнейшему окислению по схеме, аналогичной β-окислению
насыщенной ЖК. Каждый следующий фрагмент углеродной цепи,
содержащий двойную связь, находящуюся в цис-конфигурации, сразу подвергается гидратации под действием еноил-КоА-гидратазы. В
результате образуется стереоизомер β-гидроксиацила в D-конфигурации.

Окисление ненасыщенных ВЖК на примере олеиновой кислоты.
Для дальнейшего дегидрирования он изомеризуется в L-стереоизомер под действием второго дополнительного фермента – эпимеразы (еноил-КоА-
эпимераза).
Дальнейшее окисление идёт аналогично окислению насыщенных ВЖК.
α-окисление ВЖК
Этот путь катаболизма ВЖК характерен для ткани мозга и других отделов нервной ткани. Так окисляются ВЖК, содержащие более 20 атомов углерода. При
α- окислении ВЖК от углеводородной цепи отщепляется по одному атому углерода, выделяющемуся в виде СО2. Этот путь окисления не связан с синтезом АТФ. ВЖК с разветвлённой углеводородной цепью, например фитановая кислота
(3,7,11,15-тетраметилгексадекановая кислота), поступающая в организма с растительной пищей подвергаются α-окислению. В фитановой кислоте у каждого третьего атома углерода находится метильная группой, что делает невозможным
β-окисление данной кислоты.

α-окисление ВЖК.
При α-окислении фитановой кислоты удаляется карбоксильная группа в виде СО2, а затем происходит цикл β-окисления.
ω-окисление жирных кислот
Этот тип окисления катализируется микросомальными гидроксилазами при участии цитохрома Р-450.
Ω-окисление жирных кислот активируется в тех случаях, когда активность β-
окисления жирных кислот снижена. Процесс ω-окисления жирных кислот протекает в эндоплазматическом ретикулуме.
Метильная группа в ω-положении превращается в СН2ОН-группу, которая затем окисляется до –COOH, в результате чего образуется дикарбоновая кислота,
которая расщепляется путем β-окисления обычно до адипиновой (С6) (НOOC- (CH2)4-COOН ) и субериновой (С8) (НOOC-(CH2)6 -COOН ) кислот, которые затем удаляются с мочой.
Регуляция β-окисления ВЖК
Регуляция процесса β- окисления ВЖК осуществляется на этапе транспорта жирных кислот через мембрану митохондрии, т.к. здесь действует регуляторный аллостерический фермент – карнитинацилтрансфераза I.
Положительными модуляторами фермента являются АДФ, АМФ, НАД+, а
отрицательными – АТФ, НАДН+Н+ и малонил-КоА - главный аллостерический ингибитор (он является субстратом удлинения цепи в синтезе жирных кислот).
Биологическое значение окисления жирных кислот
1. Процесс β-окисления используется для получения энергии клеткой (в ЦТК).
2. В процессе β-окисления образуется значительное количество ацетил-SКоА,
который может быть использован при достаточном количестве энергии для биосинтеза различных веществ (ХС и его производных, кетоновых тел и т.д.).
БИОСИНТЕЗ ВЖК
Биосинтез ВЖК происходит в период приёма пищи. Субстратом для биосинтеза жирных кислот является ацетил-КоА, который образуется из ПВК в процессе расщепления глюкозы (преимущественно углеводного происхождения)
и в меньшей мере – из глюкогенных аминокислот – аланина, цистеина, серина,
глицина и треонина, которые сначала превращаются в ПВК, а лизин – сразу в ацетил-S-КоА. Синтез ВЖК происходит в цитоплазме. В биосинтезе ВЖК выделяют 3 этапа
1. Транспорт ацетил-KoA из митохондрий в цитозоль.
Ацетил-SKoA транспортируется в цитоплазму с помощью цитратного челночного механизма. В матриксе митохондрий ацетил-S-KoA соединяется с оксалацетатом с образованием цитрата при действии цитратсинтазы.
Цитрат переносится в цитозоль при помощи специальной трикарбоксилат-
транспортной системы при условии достаточно высокой концентрации цитрата,
что возможно лишь при избытке углеводов в клетке.
В цитоплазме цитрат расщепляется при действии цитратлиазы на ОАА
(оксалоацетат) и ацетил-KoA, с затратой 1 молекулы АТФ и KoA-SH.
Цитрат + АТФ + KoA-SH → ацетил-S-KoA + АДФ + Фн + ОАА
Ацетил-КоА далее используется в синтезе ВЖК и ХС.
Образующийся в результате реакции ОАА не может вернуться самостоятельно в матрикс митохондрий, т.к. мембрана митохондрий для него непроницаема. ОАА последовательно окисляется при действии цитозольной НАД+-зависимой дегидрогеназы в малат, который либо самостоятельно попадает в матрикс митохондрий и там при действии митохондриальной НАД+-зависимой малатдегидрогеназы превращается в ОАА; либо в цитозоле подвергается окислительному декарбоксилированию при действии НАДФ+-зависимого малат-
