
- •Классификация и номенклатура неорганических веществ
- •Наука, включающая в себя химию и физику, изучает природу и свойства материи и
- •Вещества, изучаемые химией —
- •Вещества
- •Простые вещества
- •Сложные вещества
- •Оксиды
- •Оксиды (ЭхОy-2)
- •По какому признаку солеобразующие оксиды делят на три вида?
- •Кислотные оксиды
- •Основные оксиды-
- •Амфотерные оксиды
- •Кислоты – это сложные вещества, содержащие атомы водорода, которые могут замещаться атомами металлов.
- •Классификация кислот
- •Кислоты (НхАс)
- •Соответствие кислот и оксидов
- •Классификация оснований (Ме(ОН)x)
- •Соответствие оснований и оксидов
- •Амфотерные гидроксиды
- •Соли
- •Классификация солей
- •Номенклатура неорганических соединений
- •Основания
- •Номенклатура кислот
- •Оксокислоты. Названия некоторых оксокислот и
- •Номенклатура амфотерных гидроксидов
- •Каждому амфотерному гидроксиду можно дать название, как основанию, так и кислоте
- •Соли. Номенклатура.
- •Кислые соли
- •Основные соли
- •Двухкислотное основание образует одну нормальную и одну основную соль с кислотным остатком.
- •Номенклатура
- •Модель решения 1.Средние соли –
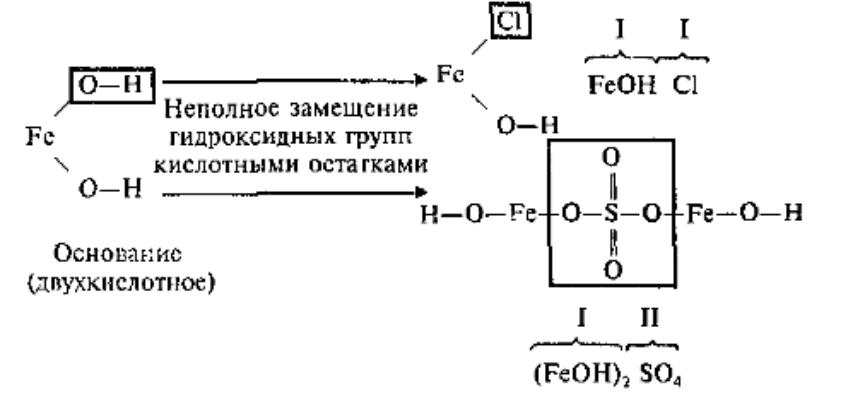
Основные соли
– это продукты неполного замещения гидроксидных групп в молекулах многокислотных оснований кислотными остатками.
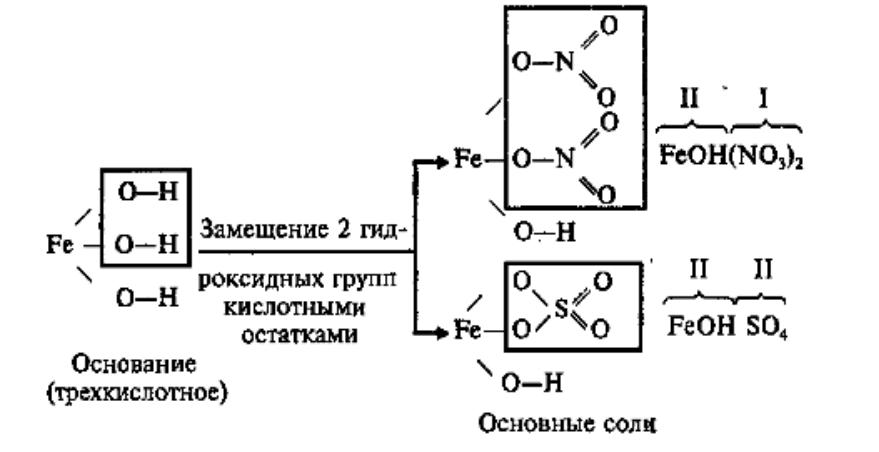
Двухкислотное основание образует одну нормальную и одну основную соль с кислотным остатком.
Трехкислотное основание образует две основные и одну среднюю соль с кислотным остатком.
Номенклатура
Название соли = Название кислотного остатка + притсавка «гидроксо- или дигидроксо- + название металла в родительном падеже + валентность металла ( в скобках, римскими цифрами) Примеры :
CuOHCl – хлорид гидроксомеди (II) Fe(OH)2Br – бромид дигдроксожелеза (III)
[Al(OH)2 ]SO4 – сульфат дигидроксоалюминия.
Алюминий имеет постоянную валентность III, поэтому ее можно не указывать.

Модель решения 1.Средние соли –
а)BaSO4 – сульфат бария б)AlPO4 – фосфат алюминия
2.Кислые соли –
а)Ca(HS)2 – сульфид кальция б)NaH2PO4 – дигидрофосфат натрия
3.Основные соли
а)FeOHCl2 – хлорид гидроксожелеза (III) б)Mn(OH)NO3 – нитрат гидроксомарганца (II) в)(СuOH)2SO4 – cульфат гидроксомеди (II)*
*Примечание: в данном случае значение валентности не обязательно, поскольку Cu(I) основных солей не образует.
