
Коллок
.docx1.Уравнение Шредингера в квантовой механике

Общее уравнение Шредингера справедливо для любой частицы (со спином, равным 0), движущейся со скоростью малой по сравнению со скоростью света. Оно дополняется условиями, накладываемыми на волновую функцию:
волновая функция должна быть конечной, однозначной и непрерывной;
производные должны быть непрерывны;
функция должна быть интегрируема; это условие в простейших случаях сводится к условию нормировки вероятностей.
В тех случаях, когда частица находится в стационарных потенциальных силовых полях (энергия U=U(x,y,z) не зависит от времени), общее уравнение Шредингера можно упростить, исключив зависимость ψ от времени.


2. Потенциальная энергия в атоме водорода
 Из
уравнения движения электрона следует,
что кинетическая энергия равна
потенциальной. Тогда можно записать:
Из
уравнения движения электрона следует,
что кинетическая энергия равна
потенциальной. Тогда можно записать:
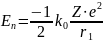
Подставим сюда выражение для радиуса первой орбиты и получим:
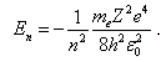
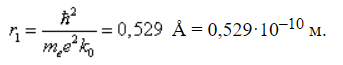
3. Собственное значение энергии электрона в атоме водорода

Полную
информацию о возможных состояниях
внешнего электрона в водородоподобных
атомах можно получить, решив трехмерное
уравнение Шредингера для стационарных
состояний:
![]() где
ψ – собственная волновая функция
стационарного состояния, U – энергия
кулоновского взаимодействия электрона
с атомным ядром, Е – собственное значение
энергии.
где
ψ – собственная волновая функция
стационарного состояния, U – энергия
кулоновского взаимодействия электрона
с атомным ядром, Е – собственное значение
энергии.

4. Волновая функция, отвечающая основному состоянию (1s -состоянию)
Волновая функция ψ, являясь основной характеристикой состояния микрочастицы, позволяет в квантовой механике вычислить средние значения физических величин, характеризующих данный микрообъект. Волновая функция – основной носитель информации о корпускулярных и волновых свойствах микрочастицы.
5. Волновая функция, отвечающая 2s состоянию
6. Первый боровский радиус
Радиус первой орбиты водородного атома называют боровским радиусом.
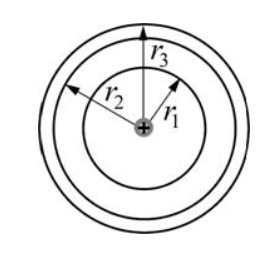
7. Вероятность обнаружить электрон в области, ограниченной элементом объема
Движение квантовой частицы отличается от движения классической частицы. В квантовой механике существует конечная вероятность обнаружить частицу в классически запрещённой области пространства.
Вероятность найти частицу в момент t в конечном объѐме V:
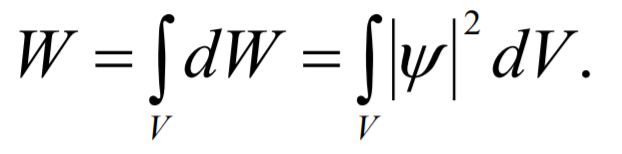

При интегрировании по бесконечному V вероятность обнаружить частицу равна 1. Из этого следует условие нормировки:
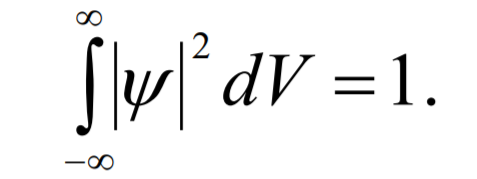
Все положения свободной частицы в пространстве равновероятны, т.к. вероятность обнаружить частицу в любой точке пространства
![]()
8. Состояние электронов в атоме однозначно определяется набором четырех квантовых чисел…
главного n
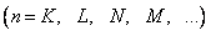 ;
;орбитального l
 ,
обычно эти состояния обозначают 1s,
2d,
3f;
,
обычно эти состояния обозначают 1s,
2d,
3f;магнитного m
 ;
;магнитного спинового

9. Принцип Паули:
в одном и том же атоме не может быть более одного электрона с одинаковым набором четырех квантовых чисел: n, l, m , ms :
![]()
где Z (n, l, m , ms ) - число электронов, находящихся в квантовом состоянии, описываемых набором четырех квантовых чисел: n, l, m , ms . Таким образом, принцип Паули утверждает, что два электрона, связанные в одном и том же атоме различаются значениями, по крайней мере, одного квантового числа.
10. Максимальное число электронов находящихся в состоянии с данным n
Максимальное число электронов, находящихся в состояниях, определяемых значением главного квантового числа n, равно:
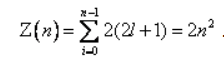
11. Максимальное число электронов находящихся в состоянии с данным l
Максимальное число электронов, находящихся в состояниях, определяемых двумя квантовыми числами n и l:
![]()
12. Орбитальный момент импульса электрона
Момент
импульса электрона в атоме квантуется
![]()

13. Проекция орбитального момента импульса электрона на направление внешнего магнитного поля

14. Магнитный момент импульса электрона
Орбитальный магнитный момент pm, вызванный движением электрона по орбите обозначают Lm
![]()
Вектора Ll и Lm направлены в противоположные стороны.

Lm иногда обозначают μl .
15. Магнетон Бора
Это элементарный магнитный момент.
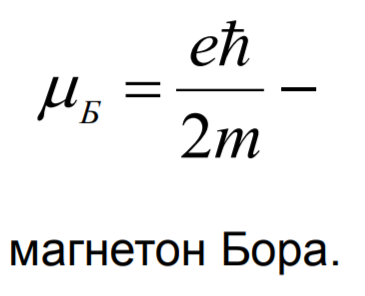
16. Проекция магнитного момента импульса электрона на направление внешнего магнитного поля
Проекция
магнитного момента на направление
внешнего магнитного поля (например, ось
z):
![]() ml
– магнитное квантовое число, определяющее
проекцию момента импульса электрона
на z.
ml
– магнитное квантовое число, определяющее
проекцию момента импульса электрона
на z.
17. Собственный магнитный момент импульса электрона
Помимо собственного механического момента – спина, у электрона есть собсвенный магнитный момент, который связан с механическим соотношением:
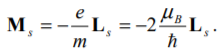
18. Проекция спинового магнитного момента импульса электрона на направление внешнего магнитного поля
Проекция
магнитного момента спина на направление
внешнего магнитного поля (например, ось
z):

Электрон обладает собственным моментом импульса – спином, который не связан с движением электрона в пространстве и имеет только две ориентации относительно внешнего магнитного поля.

