
Лекции / Л13 Химические загрязнения гидросферы
.pdf
Тяжелые металлы
Одним из сильнейших по токсическому действию и очень распространенным химическим загрязнением является загрязнение тяжелыми металлами.
Тяжёлые металлы - это элементы периодической системы химических элементов, с молекулярной массой свыше 50 атомных единиц. Эта группа элементов активно участвует в биологических процессах, входя в состав многих ферментов. Группа «тяжелых металлов» во многом совпадает по составу с группой микроэлементов (необходимых организму химических элементов, но в очень малых концентрациях). С другой стороны, тяжёлые металлы и их соединения оказывают вредное воздействие на организм при превышении ПДК. К ним относятся: свинец, цинк, кадмий, ртуть, молибден, хром, марганец, никель, олово, кобальт, титан, медь, ванадий.
Их опасность и особенность заключается в том, что тяжелые металлы способны накапливаться в организме (кумулятивный эффект) и почти не поддаются выведению (очень устойчивы). Достигая определенной концентрации в организме, они начинают свое губительное воздействие - вызывают отравления, мутации.
Попавшие в воду тяжелые металлы сравнительно быстро распространяются по большому объему. Частично они выпадают в осадок в виде карбонатов, сульфатов или сульфидов, частично адсорбируются на минеральных или органических осадках. Словом, концентрация тяжелых металлов в отложениях постоянно растет. Если водная среда имеет рН меньше 7 (кислая), то осажденные металлы могут перейти в воду. Значения рН уменьшается при попадании кислот в реки и в сильно заросшие водоемы, когда в результате активной деятельности растущих микроорганизмов выделяется особенно много углекислого газа.
1
Для некоторых тяжелых металлов установлена возможность микробиологического алкилирования (реакций с присоединением алкильной группы -СН), таким образом они могут включаться в цикл питания. Реакции метилирования характерны для мышьяка и ртути. Основные реакции ртути в живых организмах:
Hg ® CH3Hg+ ® (CH3)2Hg
|
HgS ® HgSO3 ® HgSO4 |
NADH +H + |
||||
|
¾¾¾¾¾¾®Hg° |
|||||
|
NADH2 - никотинамид-адениндинуклеотид |
|||||
|
|
Hg2+ |
|
|
|
(CH3)2Hg |
|
|
|
|
CH Hg+ |
|
|
|
|
|
|
|||
|
|
|
|
|
3 |
Hgo + CH4 |
|
|
|
|
|
|
|
|
|
аэробные |
анаэробные |
|||
3- |
® AsO3 |
3- условия |
условия |
|||
AsO4 |
¾¾¾¾¾® (CH3)3As ¾¾¾¾¾¾® (CH3)2AsH |
|||||
Соединения |
тяжелых |
металлов |
постепенно концентрируются в |
|||
пищевых цепях и в конце цепи, дойдя до человека, достигают токсичной концентрации. Подобные вещества представляют особую опасность для организма вследствие их устойчивости и липофильности (взаимодействия с жирами), что обеспечивает большой период полувыведения, т.е. время, в течение которого выделяется или разрушается половина усвоенного организмами вещества. Биологический период полувыведения для ртути составляет 70÷80 дней; для кадмия - больше 10 лет. Не приходится удивляться вредным последствиям внедрения кадмия в организм: соответствующая болезнь носит название итаи-итаи, выражается в болезненном скручивании костей, анемии и почечной недостаточности. Токсичность тяжелых металлов связана с образованием хелатов (особо прочных комплексных соединений) и сульфидов с биологически активными веществами, особенно ферментами.
2
В растения тяжелые металлы отлагаются в клеточных стенках с образованием хелатов, и становятся физиологически неактивными, поэтому растения нормально развиваются, при попадании в пищу человека механизм обезвреживания тяжелых металлов прекращается (хелатные комплексы разрушаются) и человек получает большую дозу тяжелых металлов.
Поверхностно-активные вещества (ПАВ), детергенты
ПАВ (поверхностно-активные вещества) - продукты, входящие в состав моющих средств - детергентов. Они выполняют две функции:
1.Уменьшают поверхностное натяжение жидкости, в которой растворены
2.Образуют стабильную эмульсию или суспензию с частицами
удаляемых загрязнений. Снижают жесткость воды с образованием щелочного раствора.
ПАВ подразделяются на три класса: o анионактивные
o катионактивные o неионогенные
Химический состав ПАВ
|
анионактивные |
|
O |
R |
S O Na |
|
O |
R=C12- C18 алкилбензолсульфонат (АБС)
катионактивные
R' |
|
R N R'' X |
|
R''' |
R, R' и R''- УВ радикалы; |
|
3
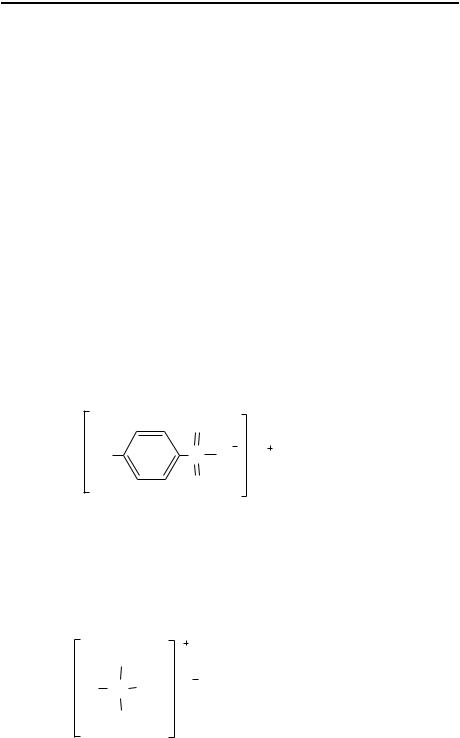
R'''- ароматический УВ; X - галоген или кислотная группа
неионогенные
CH3 |
CH2 |
8 |
O CH |
OC2H5 |
|
|
2 |
20 |
Внастоящее время растет производство неионогенных (менее полярных) ПАВ для современных тканей, отличающихся гидрофобностью.
Всостав моющих средств в качестве связующего компонента входят смеси полифосфатов (Na5P3O10- триполифосфат). Для загрязнений особое значение имеют полифосфаты. Фосфорные компоненты гидролизуются с образованием нетоксичных монофосфатов:
Р3О55- + 2Н2О Û 2НР О24- + Н2РО-4 которые являются питательной средой для растений и могут вызвать
интенсивный рост растений, что приведет к загрязнению ранее чистых водоемов. По мере отмирания растений начинается их гниение, а вода обедняется кислородом, что ухудшает условия существования живых организмов в воде.
ПАВ отрицательно влияют на качество подземных питьевых вод, самоочищаемую способность водоемов и организм человека. Благодаря высокой проникающей способности через грунты (до 3 км), ПАВ проходят через очистные сооружения водопроводов и могут попасть в питьевую воду.
В первую очередь поражается нервная и ферментная системы, обменные процессы, увеличивается содержание холестерина в крови, что приводит к атеросклерозу.
ПАВ способствуют растворению обычно нерастворимых в воде канцерогенов, образуя с ними стойкие эмульсии, активизируют действие канцерогенов, а также усиливают канцерогенные свойства других веществ.
Для большинства ПАВ характерен узкий интервал между токсической
и нетоксической концентрацией для водных организмов. ПАВ с
4
концентрацией 50 мг/л губят рыбную молодь, поэтому даже небольшие количества ПАВ в водоемах могут нанести большой урон растительному и животному миру.
Особую опасность представляют ПАВ (0,5 мг/л) в сочетании с другими загрязнителями (пестицидами и другими высокотоксичными веществами). Последние всасываются в кровь быстрее и в бОльших количествах, чем в отсутствии ПАВ (эффект синергизма вредного воздействия).
Присутствие ПАВ уменьшает концентрацию кислорода в воде, поскольку он дополнительно расходуется на окисление ПАВ. Они образуют стойкие пены с эмульгированными в поверхностных пленках нефтепродуктами, что увеличивает их концентрацию в воде. Из-за высокой пенообразующей способности ПАВ затрудняется доступ кислорода в толщу природных вод и ухудшается самоочищение. В пене концентрируются органические загрязнители, болезнетворные микроорганизмы. Наибольшее пенообразование у неионогенных ПАВ.
Характеристика некоторых пестицидов
Хлорпроизводные углеводороды
|
H |
|
Cl |
C |
Cl |
|
CCl3 |
|
|
ДДТ |
|
1,1,1-трихлор-2,2-бис(n-хлорфенил) этан
Против комаров, вредителей хлопка, технических культур, строевого леса.
Фосфорорганические вещества
S |
|
|
|
|
|
|
|
O |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
CH3O P |
|
S |
|
|
|
CH |
|
C |
|
|
OC2H5 |
|||||
|
|
|
|
|
|
|||||||||||
CH3 |
|
O |
|
|
|
|
CH |
|
C |
|
|
OC H |
||||
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
5 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
O
5

Карбофос (мелатион) О,О-диметил-S-1,2-дикарбэтоксиэтинлдитиофосфат
Уничтожение вредителей фруктовых деревьев, овощей, декоративных растений, а также комаров.
Производные карбоматов
O
O C O NHCH3
Севин 1-нафтил-N-метилкарбомат Обработка хлопка, кормовых культур, фруктов, овощей.
Нитраты и нитриты.
Нитраты (NO3-), удобрения: натриевая селитра NaNO3, калийная KNO3, аммонийная NH4NO3. Интенсивное поступление нитратов в растения приводит к тому, что они не полностью включаются в обменные процессы и накапливаются в листьях, стеблях и корнях. Для растений избыток нитратов значительной опасности не представляет, но при попадании в организм теплокровных с пищей они превращаются в более токсичные нитриты (NO2-), вступающих во взаимодействие с аминами (NН2-), и амидами (-СОNН2), с образованием нитрозаминов и нитрозамидами:
R |
NH |
+ HO-NO |
|
|
|
R |
N-N=O + H2O |
R |
|
|
|
R |
|||
|
HNO2 |
|
|
|
|
||
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
O |
R-C-NH |
+ HO-NO |
|
|
|
R-C-NH-N=O + H2O |
||
|
|
|
|||||
|
2 |
|
|
|
|
|
|
HNO2
Накопление в организме человека нитратов приводит к тяжелому нарушению обмена веществ, аллергии, нервным расстройствам. В крови NO3- превращают Fe2+ гемоглобина в Fe3+, что вызывает нарушение переноса О2 от легких к тканям:
Fe2+ + NO3-® Fe3+ + NO2-
6
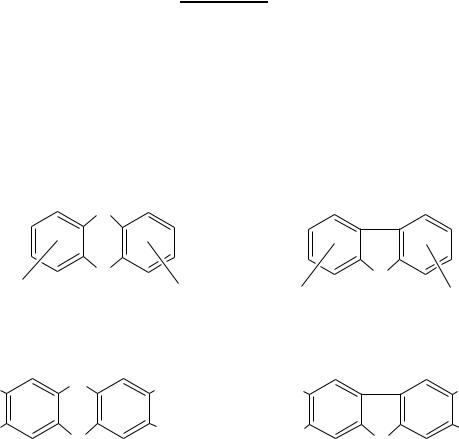
Диоксины
Полихлорированные дибензо-n-диоксины (ПХДД) и дибензофураны (ПХДФ) являются представителями хлорированных циклических ароматических эфиров, в которых два бензольных кольца с различной степенью хлорирования связаны между собой двумя атомами кислорода в о- положении (ПХДД) или одним атомом кислорода и связью С-С (ПХДФ).
|
|
9 |
10 |
1 |
|
|
9 |
|
1 |
|
|
8 |
O |
|
8 |
|
|
||||
|
|
2 |
|
2 |
||||||
|
|
|
|
|
|
|
||||
|
7 |
6 |
O |
4 |
3 |
7 |
|
O |
4 |
3 |
|
Cly |
Clx |
Cly |
6 |
Clx |
|||||
|
|
5 |
|
5 |
|
|||||
|
дибензо-n-диоксин |
|
x=1-4 |
дибензофуран |
|
|||||
|
|
ПХДД |
|
|
y=0-4 |
|
ПХДФ |
|
|
|
Cl |
|
O |
|
Cl |
|
Cl |
|
|
|
Cl |
Cl |
|
O |
|
Cl |
|
Cl |
|
O |
|
Cl |
|
|
|
|
|
|
|
|
|
||
2,3,7,8-тетрахлордибензо-р-диоксин 2,3,7,8-тетрахлордибензо-р-фуран
Дибензо-1,4-диоксин |
ПХДФ |
ПХДД |
|
Рис.14. Химическая структура полихлорированных дибензо-n- диоксинов (ПХДД) и дибензофуранов (ПХДФ).
Таким образом, для замещения атомами хлора остаются 8 мест (1,2,3,4 и 6,7,8,9). Всего имеется 75 изомеров среди гомологов ПХДД и 135 изомеров гомологов ПХДФ; последних оказалось несколько больше, т.к. у молекул ПХДФ отсутствует плоскость симметрии. Наряду с этими чисто полихлорированными изомерами существует также чисто полибромированные дибензо-n-диоксины и дибензофураны (ПБДД и ПБДФ), а также смешанные хлорированные и бромированные изомеры. Бромированные диоксины и фураны являются продуктами термических
7
превращений бромсодержащих веществ, повышающих огнестойкость материалов, и применяются в пластмассах и других горючих материалах.
Из-за наличия смешанных галогенированных соединений число возможных изомеров на основе диоксинов и фуранов далеко превышает тысячу.
Диоксины образуются в качестве побочных продуктов при целом ряде химических процессов в ходе сжигания отходов в мусоросжигательных печах и пожарах.
Чтобы остановить эти процессы, т.е. ингибировать образование диоксинов при сжигании мусора, в топочные газы при 400°С (выше оптимума образования диоксинов 300°С) распыляют триэтаноламин и триэтиламин, что снижает выход ПХДД/Ф более чем на 95%.
Эмиссии мусоросжигательных печей близки по составу к дыму обычных каминов с горящими дровами, но только в том случае, если в мусоре нет хлорфенолов, полихлорированных дифенилов и дифениловых эфиров, при термолизе которых образуются диоксины и фураны в больших концентрациях.
Хранение отходов, содержащих ПХДД и ПХДФ, на свалках также вызывает загрязнение окружающей среды. Хотя эти вещества плохо вымываются водой, они могут экстрагироваться органическими растворителями, имеющимися на свалках, в виде "просачивающегося масла".
Другим рассеянным источником эмиссии диоксинов и фуранов являются выхлопные газы грузовых автомобилей. Для снижения отложений свинца внутри двигателя в моторное топливо, содержащее алкилсвинец (0,15 г Pb в 1 л бензина), добавляют дихлорэтан в качестве "мусорщика" (scavenger). Автомобили, работающие на таком топливе, выделяют на каждый километр пути до 12 пг 2,3,7,8-ТХДД. В выхлопных газах грузовых автомобилей, снабженных катализаторами и работающих на неэтилированном бензине и соответствующего "мусорщика", ПХДД и ПХДФ
не обнаружено.
8
В окружающей среде вследствие их низкой растворимости в воде (~0,2 мкг/л) диоксины малоподвижны и поэтому прочно связываются с осадками в водных системах и проявляют очень низкую вертикальную подвижность в почвах. Горизонтальная подвижность связана в основном с процессами эрозии (например, выветриванием). Несмотря на низкую летучесть, эти соединения могут переходить в газовую фазу при испарении, что снижает их концентрацию в загрязненных местах. 2,3,7,8-ТХДД достаточно быстро разрушается под действием УФ-излучения (> 290 нм).
Диоксины накапливаются преимущественно в печени и жировых тканях. Животные, находящиеся в длительном контакте с загрязненной почвой, не накапливают эти вещества в концентрациях, превышающей почвенную, в то время как у организмов, обитающих в воде (дафнии, змеи, рыбы), отмечены коэффициенты биоаккумуляции от 2 до 6×103. Примерно такого же порядка аккумуляция наблюдается в водорослях, ряске и пр., в то время как в наземных растениях (пшеница, соя, морковь, картофель) можно обнаружить лишь 0,1% от содержания 2,3,7,8-ТХДД в почве.
У человека отравление ПХДД и ПХДФ дают следующую картину симптомов болезни: хлороакне (гнойная сыпь на коже, вызванная воздействием хлорированных соединений), тошнота, рвота, головные и мышечные боли, усталость, психические изменения, повышение содержания липидов в крови, озноб.
Промышленные процессы, связанные с применением хлора, могут привести к образованию ПХДД (в порядке убывания интенсивности образования диоксинов):
¨процессы получения хлорфенолов и продуктов на их основе;
¨процессы получения замещенных хлорбензолов;
¨синтез алифатических хлорпроизводных;
¨процессы с хлорсодержащими промежуточными продуктами;
9
¨процессы в неорганической хлорной промышленности;
¨процессы с применением хлорированных катализаторов и растворителей.
Однако основным путем образования диоксинов являются процессы горения в широком смысле слова. При протекании термолитических процессов преимущественно в средней области температур (300-600°С) создаются условия для осуществления многочисленных радикальных реакций, механизм которых еще недостаточно выяснен. В ходе этих реакций, особенно в присутствии доноров хлора, наряду с хлорированными фенолами и ароматическими соединениями образуются также ПХДД и ПХДФ.
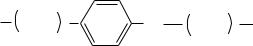
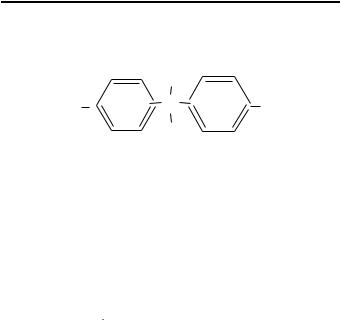
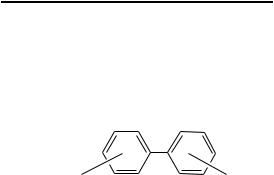
Полихлорированные бифенилы
Токсичность полихлорированных бифенилов заметно возрастает с увеличением содержания в них хлора. При содержании хлора 42% ПДКм.р. равна 1 мг/м3, при содержании хлора 54% ПДКм.р. равна 0,5 мг/м3.
Clx |
Cly |
Полихлорированные
бифенилы
Отравление полихлорированными бифенилами вызывает хлороз – хлоракне, которое выражается в трудно излечимом поражении кожи, после чего остаются шрамы. Кроме того, изменяется состав крови, отравление сказывается на печени и состоянии нервной системы. Их концентрация в жировых тканях человека составляет от 0,1 до 10 млн-1. Имеются предположения, что эти вещества обладают и канцерогенным действием. На открытом воздухе период полураспада составляет от 10 до 100 лет, т.е. значительно больше, чем для ДДТ. Эти чрезвычайно устойчивые соединения находят применение в холодильных установках, как пластификаторы в
10
