
- •Холестерин
- •Роль липопротеинов плазмы крови в транспорте холестерина и патогенезе атеросклероза.
- •Участие липопротеинов низкой плотности (лпнп) в синтезе стероидных гормонов
- •Слайд 12 Нерациональное питание
- •Генетический фактор.
- •Эндокринные нарушения.
- •Курение
- •Недостаточная физическая активность.
- •Стрессорные ситуации
СЛАЙДЫ 1 – 8
Метаболизм липидов (Обмен липидов в организме. Резорбция, переваривание, трансформация и транспорт липидов).
Жиры могут расщепляться и всасываться в тонком кишечнике только при условии их обязательной эмульгации, то есть в результате образования частиц (капелек) жира размером 0,5 мкм. Эмульгация жира происходит под влиянием желчных кислот. Расщепление жира идет до моноглицеридов и жирных кислот под влиянием панкреатической липазы и фосфолипазы, а также – липазы кишечного сока. Капли эмульсии (мицеллы), состоящие из моноглицеридов и жирных кислот, поступают в энтероцит, где моноглицериды и жирные кислоты ресинтезируются в триглицериды и, объединившись с холестерином и фосфолипидами, образуют глобулы – капли, покрытые с поверхности -липопротеином (липопротеином низкой плотности – ЛПНП). Глобулы экскретируются в межклеточное пространство и, далее, поступают в лимфу в виде так называемых хиломикронов – частиц малой плотности (0,96), содержащих до 1% белка и 99% липидов (триглицериды, фосфолипиды, холестерин).
Через грудной лимфатический проток хиломикроны поступают в кровеносную систему и достигают легких, печени, миокарда, селезенки, жировой ткани. Далее под воздействием липопротеиновой липазы триглицериды хиломикронов расщепляются до образования свободных жирных кислот (СЖК). Значительная часть этого процесса проходит интраваскулярно. Две трети образовавшихся СЖК адсорбируется на альбумине сыворотки, а одна треть - на -липопротеинах (липопротеинах высокой плотности – ЛПВП) и транспортируется в органы и ткани, где частично ресинтезируется в триглицериды, а частично используется как донатор энергии.
В жировой ткани продукты липидного обмена хранятся в основном в виде триглицеридов и по мере необходимости поступают в кровь в виде СЖК.
В печени значительная часть СЖК ресинтезируется в триглицериды, а оставшиеся СЖК используются для образования фосфолипидов и холестерина. В печени же происходит синтез липопротеинов низкой плотности (-липопротеинов), в составе которых до 20% белка (апопротеины), триглицериды, фосфолипиды, эфиры холестерина и свободный холестерин. В дальнейшем на уровне капилляров органов и тканей триглицериды, входящие в состав -липопротеинов, гидролизуются липопротеинлипазой до СЖК, частично идущих на энергетические нужды, а частично депонирующиеся в жировой ткани в виде ресинтезированных триглицеридов. В печени, отдавая холестерин, -липопротеины превращаются в -липопротеины (липопротеины высокой плотности – ЛПВП).
СЛАЙД 9
Место атеросклероза в патологии сосудистой стенки
Прежде всего, необходимо определить место атеросклероза среди других патологических процессов, поражающих сосудистую стенку.
Термин атеросклероз происходит от двух греческих слов: athere – кашица (в данном случае – жиро-белковый детрит) и sclerosis – затвердение, и означает разрастание соединительной ткани в стенке сосуда, являющееся реакцией на эту “кашицу”.
Разрастание соединительной ткани в стенке артерии может быть следствием самых различных заболеваний. Существует патологический процесс, который носит название болезни Менненберга, или атерокальциноза. Он заключается в том, что в средней оболочке сосуда начинают откладываться соли кальция, вокруг которых развивается реактивное воспаление, и окружающая ткань склерозируется.
В основе развития склеротических процессов в сосудистой стенке может лежать гиалиноз, который является следствием ее пропитывания плазматическими белками.
Если в стенке артерии развился воспалительный процесс, то он тоже может завершиться склерозированием ткани. Например, при сифилитическом мезоаортите (сифилитическом воспалении средней оболочке аорты) в ней развивается склероз - разрастается соединительная ткань, и интима аорты становится морщинистой, приобретает вид “шагреневой кожи”.
Склероз сосудистой стенки может возникать и при аллергических васкулитах, когда она поражается антителами, и в очагах этого поражения начинается склеротический процесс.
Таким образом, атеросклероз является одной из разновидностей артериосклероза, той его разновидностью, когда соединительная ткань разрастается в ответ на образование в стенке сосуда жиро-белкового детрита.
Однако разбирая этиологию и патогенез атеросклероза, следует подчеркнуть, что, хотя атеросклероз и находит свое выражение в поражении сосудистой стенки, тем не менее он представляет собой заболевание организма в целом. Это положение можно проиллюстрировать одним ярким примером. Хирург Кристиан Барнард пересадил Филиппу Блайбергу – человеку пожилого возраста, сердце от молодого донора, погибшего в результате кровоизлияния в мозг. Когда через восемнадцать месяцев Блайберг скончался, на секции было обнаружено, что коронарные сосуды пересаженного органа сильно изменены атеросклерозом; состояние венечных артерий этого, полтора года назад молодого, сердца было таким же, как и остальных сосудов пожилого реципиента. Следовательно, дело заключается не столько в местных изменениях сосудистой стенки, сколько в общем нарушении обмена веществ организма.
Холестерин
Согласно химической номенклатуре правильное название холестерина – холестерол, так как он является ненасыщенным спиртом, и относится к группе стеринов.
Холестерин – вещество жизненно важное для организма, так как он входит в состав биомембран клеток, участвует в синтезе желчных кислот, стероидных (половых и кортикоидных) гормонов. Под влиянием ультрафиолетовых лучей холестерин преобразуется в витамин Д3 и, таким образом, защищает организм от рахита. Определенное количество холестерина «запасается» клетками, в протоплазме которых он в виде эфиров с жирными кислотами образует вакуоли (капли), Механизм синтеза стероидных гормонов из холестерина демонстрирует приводимая ниже схема.
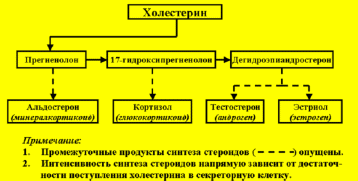
Около 1/3 холестерина организм получает с пищей, а 2/3 его синтезируется клетками органов и тканей, в основном – клетками печени. В зависимости от рациона питания в организм ежесуточно поступает 300 – 500 мг холестерина, остальной холестерин (суточная потребность – до 1,2 – 1,4 г), как уже было сказано, синтезируется клетками организма.
Сам по себе холестерин какой-либо «атерогенностью» не обладает. Его участие в патогенезе атеросклероза проявляется только тогда, когда этому способствуют разнообразные атерогенные факторы. Однако, для диагностики атеросклероза важно знать нормальную концентрацию холестерина в крови (общий холестерин сыворотки крови) и его содержание в липопротеинах низкой плотности (ЛПНП) и липопротеинах высокой плотности (ЛПВП), так как при развитии атеросклероза эти показатели могут существенно изменяться. Более подробно механизмы патогенеза атеросклероза будут рассмотрены далее.
Итак, норма общего холестерина сыворотки крови – до 200 мг/%
(5,2 ммоль/л); умеренная гиперхолестеринемия - 200 – 250 мг/%
(5,2 – 6,5 ммоль/л); выраженная гиперхолестеринемия – более 250 мг/% (более 6,5 ммоль/л). Нормальный уровень холестерина ЛПНП – 2,6 – 4,1 ммоль/л; норма холестерина ЛПВП – менее 0,9 ммоль/л.
Роль липопротеинов плазмы крови в транспорте холестерина и патогенезе атеросклероза.
По современным представлениям основной причиной возникновения атеросклероза являются нарушения в транспорте и утилизации холестерина клетками организма, в том числе – и клетками эндотелия сосудов.
Холестерин в организме может транспортироваться только в виде сложных по своему строению высокомолекулярных соединений (комплексов), отличительной особенностью которых является их водорастворимость. К таким соединениям относятся хиломикроны и липопротеины. Последние играют основную роль в доставке холестерина к клеткам эндотелия сосудов, к клеткам печени и других органов и тканей организма.
Липопротеины синтезируются и секретируются клетками печени и эпителиальными клетками тонкого кишечника. Все виды липопротеинов имеют мицеллярную структуру и, независимо от их величины и плотности, построены по одному и тому же принципу. В центре мицеллы находится жировая капля (ядро), состоящее из неполярных липидов (триглицеридов и эфиров холестерина). Оболочка мицеллы образована фосфолипидным монослоем, в который встроены молекулы белков (апопротеинов) и свободного холестерина.
Мицеллы липопротеинов имеют различные размеры и плотность и содержат различное количество белков (апопротеинов), холестерина и триглицеридов. Выделено три основные вида липопротеинов: липопротеины очень низкой плотности (ЛПОНП, пре--липопротеины), липопротеины низкой плотности (ЛПНП, -липопротеины) и липопротеины высокой плотности (ЛПВП, -липопротеины). Первые два вида липопротеинов переносятся кровотоком в соединении с -глобулинами, ЛПВП – в соединении с -глобулинами плазмы крови.
Основным переносчиком холестерина (его в мицелле этого вида липопротеинов содержится более 50%) являются ЛПНП. В ЛПОНП холестерина содержится несколько меньше. Этот вид липопротеинов в основном является переносчиком триглицеридов. ЛПВП содержат очень мало холестерина и много белка и фосфолипидов.
ЛПНП доставляют холестерин к клеткам организма, в том числе – и к клеткам эндотелия сосудов. ЛПВП, наоборот, переносят холестерин от клеток различных органов и тканей к клеткам печени, где он и метаболизируется. Следует иметь в виду, что холестерин может проникнуть в клетку только благодаря рецепторам ЛПНП. При соединении ЛПНП с соответствующими рецепторами (рецепторы ЛПНП), холестерин выделяется из мицеллы, переносится в протоплазму клетки и там используется для ее нужд. С другой стороны, при переносе холестерина из клеток организма (в том числе – и из клеток сосудистого эндотелия) к клеткам печени с помощью ЛПВП он может проникнуть в гепатоциты только благодаря рецепторам ЛПВП, находящимся на мембране гепатоцитов. Таким образом, как усвоение холестерина клетками эндотелия сосудов, так и перенос излишков холестерина от клеток эндотелия сосудов к гепатоцитам и усвоение ими холестерина зависит от состояния и плотности соответствующих рецепторов на мембране клеток. В норме клетки способны увеличивать или уменьшать количество рецепторов как ЛПНП, так и ЛПВП. Однако в значительной степени эта их особенность генетически детерминирована.
Весьма серьезную роль в контактах липопротеинов с рецепторным аппаратом клеток играют апопротеины, которые, как мы помним, встроены в липидный монослой мембраны липопротеиновой мицеллы. Именно молекулы апопротеинов мицеллы липопротеинов являются лигандами, связывающими соответствующий липопротеин с его рецептором. Они же в ряде случаев играют и роль кофакторов для соответствующих ферментов. В настоящее время выделено четыре вида апопротеинов.
Апо-А – обеспечивает связь ЛПВП с соответствующим рецепторным аппаратом.
Апо-В – обеспечивает связь ЛПНП с рецепторным аппаратом клеток печени и периферических тканей;
Апо-С-II – кофактор для липопротеиновой липазы, благодаря которой триглицериды удаляются из хиломикронов и ЛПОНП;
Апо-Е – обеспечивает связь липротеинов с рецепторным аппаратом гепатоцитов.
Описан и еще один вид апопротеинов – так называемый апопротеин (а), которому приписывают наибольшую атерогенность и входящий в состав ЛПНП. Атерогенность этого апопротеина объясняют несколькими его свойствами. Во-первых, он легко окисляется и поглощается макрофагами. Во-вторых, печеночные клетки имеют наименьшее количество рецепторов к ЛПНП, содержащим липопротеин (а). И, наконец, в-третьих, имеются данные о том, что ЛПНП, содержащие липопротеин (а), обладают повышенными антитромболитическими свойствами.
Учитывая особенности транспорта холестерина липопротеинами (от печени к клеткам других органов и тканей и от клеток органов и тканей к клеткам печени) одни из них (ЛПОНП и, особенно, ЛПНП) получили название «атерогенных липопротеинов», а другие (ЛПВП) – «антиатерогенных липопротеинов». Однако, говорить о том, что патогенез атеросклероза определяется только уровнем концентраций в плазме крови атерогенных и антиатерогенных липопротеинов, конечно, нельзя. Нужно не забывать о достаточности (недостаточности) соответствующего рецепторного аппарата, а также о полноценной (или неполноценной) функции апопротеинов, входящих в состав мицеллы липротеинов. Кроме того, значительную роль в провокации атеросклероза играют и, так называемые, «модифицированные» липопротеины. Причин модификации (изменения) липопротеинов достаточно много, однако основной из них является их перекисное окисление. В результате перекисного окисления «нормальные» липопротеины приобретают мощные атерогенные свойства, которые объясняются двумя причинами.
Во-первых, модифицированные липопротеины могут без каких-либо ограничений накапливаться в макрофагах, что заставляет их превращаться в «пенистые клетки» - один из основных факторов морфогенеза атеросклероза. Известно, что макрофаги в норме поглощают избыток ЛПНП и, метаболизируя их, предотвращают перегрузку клеток эндотелия сосудов холестерином. Этот процесс регулируется по принципу обратной связи: при заполнении макрофага достаточным количеством ЛПНП чувствительность рецепторного аппарата макрофага к ЛПНП резко падает и он перестает их поглощать. Модифицированные ЛПНП нарушают эту регуляционную связь, и макрофаги поглощают эти липотротеины без каких-либо ограничений, вплоть до их полной перегрузки и превращения в пенистые клетки.
Во-вторых, белки, входящие в состав модифицированных липопротеинов приобретают антигенные свойства, благодаря чему к ним начинается выработка аутоантител, повреждающих, в том числе, и клетки эндотелия сосудов и тромбоциты. Так запускается еще один патологический цикл, лежащий в основе развития атеросклероза.
Таким образом, об «атерогенности» и «антиатерогенности» тех или иных липопротеинов, если мы имеем в виду нормальный организм, говорить не приходится. «Атерогенность», например, ЛПНП проявляется только тогда, когда в действие вступают другие факторы патогенеза атеросклероза.
