
- •Экзаменационный билет №1
- •Предмет цитологии. Основные методы исследования клетки.
- •Транспорт через плазматическую мембрану макромолекул и частиц. Механизмы пино- и фагоцитоза.
- •Экзаменационный билет №2
- •История развития и основные положения клеточной теории.
- •Строение и функции постоянных межклеточных контактов.
- •Экзаменационный билет №3
- •Общий план строения про- и эукариотических клеток: общие черты и отличия.
- •Специальные органоиды движения клетки. Строение ресничек и жгутиков.
- •Экзаменационный билет №4
- •Общие черты и особенности строения животных и растительных клеток.
- •Десмосома как один из вариантов адгезионных межклеточных соединений: строение, функции.
- •Экзаменационный билет №5
- •Строение, функции и разнообразие поверхностного аппарата клеток.
- •Уровни суперспирализации днк в митотической хромосоме.
- •Транспортная функция плазмалеммы. Пассивный и активный транспорт.
- •Экзаменационный билет №7
- •Рецепторная функция плазматический мембраны. Внеклеточные сигнальные молекулы: разнообразие, механизмы действия.
- •Состав и строение рибосом про- и эукариот.
- •Экзаменационный билет №8
- •Биологическое значение и варианты межклеточных взаимодействий.
- •Центриоли: строение, удвоение, функции.
- •Образование веретена деления
- •Образование микротрубочек
- •Формирование ресничек и жгутиков
- •Экзаменационный билет №9
- •Химический состав и свойства плазматической мембраны про- и эукариот. Модели строения плазматической мембраны.
- •Ядерный аппарат про- и эукариот. Общие черты и отличия.
- •Экзаменационный билет №10
- •Основные компоненты клеточного ядра и их функции.
- •Белки плазматической мембраны: разнообразие, расположение в мембране, функции.
- •Экзаменационный билет №11
- •Ядрышко как центр образования р-рнк: ультраструктура, изменение во время клеточного цикла и при различной функциональной нагрузке.
- •Транспорт через мембрану малых молекул. Унипорт и котранспортные системы.
- •Экзаменационный билет №12
- •Строение и функции аппарата Гольджи. Внутриклеточная сортировка белков.
- •Щелевидный контакт как один из вариантов проводящих межклеточных соединений: строение, функции.
- •Экзаменационный билет №13
- •Химический состав и структурная организация хроматина.
- •Микрофиламенты как часть опорно-сократительного аппарата клеток. Химический состав, строение и функции микрофиламентов.
- •Экзаменационный билет №14
- •Ц итоскелет: структура, функции и разнообразие.
- •Ядерная оболочка: структура, функции. Ядерная ламина, поры.
- •Экзаменационный билет №15
- •Структуры, образующие опорно-сократительный аппарат клетки: микротрубочки, микрофиламенты, промежуточные филаменты. Химический состав, морфологические особенности.
- •Пути восприятия и передачи информации клеткой (способы химической сигнализации).
- •Экзаменационный билет №16
- •Митохондрии: общий план строения, функции, пластичность.
- •Мейоз: основные фазы, события. Биологическое значение мейоза.
- •Экзаменационный билет №17
- •Генетический аппарат митохондрий и пластид. Сравнительная характеристика ядерной и митохондриальной днк.
- •Формы клеточной гибели.
- •Экзаменационный билет №18
- •Ультраструктура пластид. Разнообразие. Онтогенез и функциональные перестройки пластид.
- •Лизосомы: разнообразие, строение и функции. Круговорот мембранных компонентов.
- •Экзаменационный билет №19
- •Строение и функции гранулярного и агранулярного эпр.
- •Интерфаза клеточного цикла: основные события и их значение.
- •Экзаменационный билет №20
- •Понятие о стационарных и обновляющихся клеточных популяциях. Жизненный путь клеток.
- •Относительная автономия хлоропластов и митохондрий. Теории происхождения органоидов энергетического обмена.
- •Экзаменационный билет №21
- •Митоз: основные фазы, события. Биологическое значение митоза.
- •Промежуточные филаменты как часть опорно-сократительного аппарата клеток. Химический состав, строение и функции промежуточных филаментов.
- •Экзаменационный билет №22
- •Вакуолярный аппарат клетки: основные компоненты и их функции. Круговорот мембранных компонентов.
- •Фазы клеточного цикла. Деление клеток.
Экзаменационный билет №1
Предмет цитологии. Основные методы исследования клетки.
Предметом цитологии является клетка как структурная и функциональная единица жизни. В задачи цитологии входит изучение строения и функционирования клеток, их химического состава, функций отдельных клеточных компонентов, приспособления к условиям окружающей среды и тд.
Методы исследования:
Световая микроскопия
Вычислено, что разрешающая способность объектива, т.е. минимальное расстояние между двумя точками, которые видны раздельно, будет равно
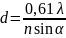 ,
где
- длина волны света, используемого для
освещения объекта; n – коэффициент
преломления среды;
- угол между оптической осью объектива
и наиболее отклоняющимся лучом, попадающим
в объектив.
,
где
- длина волны света, используемого для
освещения объекта; n – коэффициент
преломления среды;
- угол между оптической осью объектива
и наиболее отклоняющимся лучом, попадающим
в объектив.
Разрешение микроскопа зависит от длины волны – чем она меньше, тем меньшего размера деталь мы можем увидеть, и от нумерической апертуры объектива (n sin ) – чем она выше, тем выше разрешение.
Фазово-контрастная микроскопия
Отдельные участки прозрачной в общем клетки хоть мало, но все же отличаются друг от друга по плотности и по светопреломлению. Проходя через них, свет изменяет свою фазу, однако такое изменение фазы световой волны наш глаз не улавливает, так как он чувствителен только к изменению интенсивности света. Последняя зависит от величины амплитуды световой волны. В фазово-контрастном микроскопе в объектив вмонтирована специальная пластинка, проходя через которую луч света испытывает дополнительный сдвиг фазы колебаний
Интерференционный микроскоп
Он устроен так, что пучок параллельных световых лучей от осветителя разделяется на два потока. Один из них проходит через объект и приобретает изменения в фазе колебания, другой идет, минуя объект. В призмах объектива оба потока вновь соединяются и интерферируют между собой. В результате интерференции будет строиться изображение, на котором участки клетки, обладающие разной толщиной или разной плотностью, будут отличаться друг от друга по степени контрастности. В этом приборе, измеряя сдвиги фаз, можно определить концентрацию и массу сухого вещества в объекте.
Поляризационный микроскоп
Изучают объекты, обладающие так называемой изотропией, т.е. упорядоченной ориентацией субмикроскопических частиц (например, волокна веретена деления, миофибриллы и др.). У такого микроскопа перед конденсором помещается поляризатор, который пропускает световые волны с определенной плоскостью поляризации. После препарата и объектива помещается анализатор, который может пропускать свет с этой же плоскостью поляризации. Поляризатор и анализатор – это призмы, сделанные из исландского шпата (призмы Николя). Если вторую призму (анализатор) повернуть затем на 90о по отношению к первой, то свет проходить не будет. В том случае, когда между такими скрещенными призмами будет находиться объект, обладающий двойным лучепреломлением, т.е. способностью поляризовать свет, он будет виден как светящийся на темном поле. С помощью поляризационного микроскопа можно убедиться, например, в ориентированном расположении мицелл в клеточной стенке растений
Витальное (прижизненное) изучение клеток
Для кратковременного наблюдения клетки помещают просто в жидкую среду на предметное стекло; если нужно длительное наблюдение за клетками, то используются специальные камеры.
Метод клеточных структур
Более простой вариант этого метода заключается в том, что в камеру, наполненную питательной средой (смесь плазмы крови с эмбриональным экстрактом или смесь синтетической среды с добавлением плазмы крови), помещают небольшой кусочек живой ткани. Через некоторое время на периферии такого кусочка начинается деление и рост клеток. В другом случае вырезанный кусочек ткани слегка обрабатывают раствором фермента трипсина или хелатона - версена, что приводит к его диссоциации, к полному разобщению клеток друг от друга. Затем такую взвесь отмытых клеток помещают в сосуд с питательной средой, где они опускаются на дно, прикрепляются к стеклу и начинают размножаться, образуя сначала колонии, а затем сплошной клеточный пласт.
Метод микрохирургии
С помощью прибора микроманипулятора клетки разрезают, извлекают из них части, вводят вещества (микроинъекция) и т.д.
Метод флуоресцентной микроскопии
Суть его заключается в том, что целый ряд веществ обладает способностью светиться (флуоресцировать, люминесцировать) при поглощении ими световой энергии. Спектр флуоресценции всегда смещен в сторону больших длин волн по отношению к возбуждающему флуоресценцию излучению. Так, например, выделенный хлорофилл при освещении в ультрафиолетовых лучах светится красным цветом
Конфокальный сканирующий световой микроскоп
С помощью этого прибора получают серии последовательных оптических срезов, взятых с различной глубины и изображения которых накапливаются в компьютере, и по специальной программе реконструируется трехмерное, объемное, изображение объекта. Обычно используются объекты, окрашенные флуорохромами.
Изучение фиксированных клеток
Часто для фиксации используются альдегиды и их смеси с другими веществами. В качестве фиксаторов применяют также спирты, вызывающие необратимую денатурацию белков, осаждение нуклеиновых кислот и полисахаридов.
Метод цитофотометрии
Основу его составляет определение количества химических веществ по поглощению ими света определенной длины волны. Для такого рода исследований используют приборы – микроскопы-цитофотометры; у них за объективом расположен чувствительный фотометр, регистрирующий интенсивность прошедшего через объект светового потока.
Иммунохимические реакции
Его можно использовать для выявления не только белков, но и отдельных последовательностей нуклеотидов в ДНК или для определения мест локализации РНК-ДНК гибридных молекул. Для этого сначала на белок (например, тубулин) получают специфические сыворотки, содержащие антитела. Очищенные антитела химически соединяют с флуорохромами. Такие препараты наливают на объекты и с помощью люминесцентного микроскопа по свечению флуорохрома находят места локализации искомых белков в клетке.
Метод радиоавтографии
Заключается в регистрации веществ, меченных изотопами. Принцип этого метода очень прост, он повторяет метод Беккереля, открывшего радиоактивный распад. При радиоавтографическом исследовании клеткам в среду вводится предшественник одного из макромолекулярных соединений (например, аминокислота или нуклеотид), один из атомов которого замещен радиоактивным изотопом. Например, вместо 12С введен атом 14С, вместо водорода – тритий 3Н и др. В процессе синтеза в биополимер включится и меченая молекула предшественника. Регистрировать ее место в клетке можно с помощью фотоэмульсии.
Метод молекулярной гибридизации
Для этого раствор с меченной нуклеиновой кислотой (например с рибосомной РНК) или с ее фрагментом (например, с сателитной ДНК) наносят на препарат, предварительно обработанный так, чтобы денатурировать ДНК (разорвать водородные связи в нативной ДНК) в составе хромосом или ядер, что достигается щелочной или температурной обработкой образца,. В процессе ренатурации ДНК происходит образование молекулярного гибрида между меченой нуклеиновой кислотой из раствора и комплементарным ему участком ДНК в препарате. Место такой гибридизации определяется радиоавтографически.
Электронная микроскопия
По принципу конструкции электронный микроскоп очень сходен с оптическим: в нем есть источник освещения (катод электронной пушки), конденсорная система (конденсорная магнитная линза), объектив (объективная магнитная линза), окуляр (проекционные магнитные линзы), только вместо сетчатки глаза электроны попадают на люминесцирующий экран или на фотопластинку
Метод высоковольтной микроскопии
Сконструированы приборы с ускоряющим напряжением 1-3 млн. вольт. Это очень дорогие приборы, что сдерживает их широкое применение. Преимущество этого класса электронных микроскопов не в том, что на них можно получить более высокое разрешение (при более короткой длине волны электронов), а в том, что при высокой энергии электронов, которые меньше поглощаются объектом, можно просматривать образцы большой толщины (1-10 мкм). Дополнительное использование стереоскопической съемки позволяет получить информацию о трехмерной организации внутриклеточных структур с высоким их разрешением (около 0,5 нм).
Метод сканирующей электронной микроскопии
Позволяет изучать трехмерную картину поверхности клетки. При сканирующей электронной микроскопии тонкий пучок электронов (зонд) пробегает по поверхности объекта и полученная информация передается на электронно-лучевую трубку. Изображение может быть получено в отраженных или вторичных электронах. При этом методе фиксированный и специальным образом высушенный объект покрывается тонким слоем испаренного металла (чаще всего золота), отражаясь от которого электроны попадают в приемное устройство, передающее сигнал на электронно-лучевую трубку.
Контрастирование корпускулярных объектов
Оттенение металлов
В этом случае в специальных вакуумных установках производится термическое испарение металла. При этом атомы металла разлетаются от места испарения по прямым траекториям. Встречаясь с объектом, они осаждаются на нем в виде слоя; его толщина будет больше в местах, перпендикулярных направлению полета частиц металла. В участках, где объект экранирует пучок частиц, возникнут «тени». Таким образом, напыленная часть объекта обладает большей плотностью, чем напыленная подложка (фон), и поэтому объект будет виден
Негативное контрастирование
При негативном контрастировании объектов растворами солей тяжелых металлов применяют молибденовокислый аммоний, уранилацетат, фосфорно-вольфрамовую кислоту (ФВК). Если водные растворы таких веществ смешать с биологическими объектами, а затем их нанести на пленки-подложки и высушить, то объекты (например, вирусы или белковые комплексы) окажутся как бы погруженными в тонкий слой аморфного вещества высокой плотности. В электронном микроскопе они выглядят как светлые объекты на темном фоне (как фотонегатив). Преимущества метода в том, что растворенные соли могут проникать в глубь объекта и выявлять дополнительные его детали
Ультрамикротомия
Метод замораживания-скалывания
Он заключается в том, что объект сначала быстро замораживают жидким азотом, а затем при той же температуре переносят в специальную вакуумную установку. Там замороженный объект механическим способом скалывается охлажденным ножом. При этом обнажаются внутренние зоны замороженных клеток В вакууме часть воды, перешедшей в стекловидную форму, возгоняется («травление»), а поверхность скола последовательно покрывается тонким слоем испаренного углерода, а затем металла. Таким образом с замороженного и сохраняющего прижизненную структуру материала получают реплику с его скола (рис. 12). Затем уже в условиях комнатной температуры ткань или клетки растворяют в кислотах, но пленка-реплика при этом остается цела, ее изучают в электронном микроскопе.
Фракционирование клеток
Методы клеточной инженерии
