
Программа ИБП
.pdfГудов 1.Адъюванты, понятие. Химический состав, происхождение.
Для усиления иммуногенности вакцин применяют адъюванты (от лат. adjuvant— помощник). Вызывают неспецифичный иммунный ответ.
Вкачестве адъювантов используют минеральные сорбенты (гели гидрата окиси и фосфата аммония), полимерные вещества, сложные химические соединения (ЛПС, белковолипополисахаридные комплексы, мурамилдипептид и его производные и др.); бактерии и компоненты бактерий, например вытяжки БЦЖ (вакцина против туберкулеза), из которых готовят адъювант Фрейнда; инактивированные коклюшные бактерии, липиды и эмульгаторы (ланолин, арлацел); вещества, вызывающие воспалительную реакцию (сапонин, скипидер). Неорганические соединения – фосфат алюминия, гидроксид алюминия, хлорид кальция.
2.Необходимость и области использования адъювантов.
Вмедицине – при производстве вакцин (повышение иммуногенности рекомбинантных
вакцин, уменьшение дозы антигена, активация врожденного иммунитета, изменение времени высвобождения основного антигена).
Влабораторной практике - для усиления выработки антител при иммунизации животных в процессе получения гибридом (гибридная клеточная линия, полученная в результате слияния клеток двух видов: способных к образованию антител B-лимфоцитов, полученных из селезёнки иммунизированного животного (чаще всего мыши), и опухолевых клеток миеломы).
Вс/х - удобрения, помогают прилипать и впитываться.
Механизм: основное свойство большинства адъювантов - способность их депонировать антиген, то есть адсорбировать его на своей поверхности и длительное время сохранять в организме, что увеличивает продолжительность его влияния на иммунную систему.Наиболее сильные адъюванты содержат в своем составе микроорганизмы ослабленных штаммов или какие-либо субстанции, извлеченные из них. Эти компоненты являются стимуляторами клеток врожденного иммунитета, таких как макрофаги и другие антигенпрезентирующие клетки.
3.Классификация и виды адъювантов.
Классификация по происхождению:
Минеральные адъюванты: гели гидрата окиси и фосфата аммония.
Растительные адъюванты: сапонины.
Микробные адъюванты: липиды, углеводы, липополисахаридобелковые комплексы.
Цитокины и пептиды со свойствами цитокинов.
Синтетические вещества: пептиды, мурамилдипептид..
Сложные искусственные адъювантные системы: липосомы.
Неоргнические – алюминивые квасцы, фосфат алюмини, хлорид кальция.
Классификация по механизму действия:
Создание депо антигена в месте введения вакцин (мин.соед., липосомы);
Воспалительная реакция, активирующая иммунокомпетентные клетки (липососмы, масла);
Активация процесса захвата антигенов и его переработки фагоцитами (цитокин, адъювант фрейнда).
Виды адъювантов:
Убитые микроорганизмы (микобактерии, коринебактерии, нокардии и др.)
Органические вещества (бактериальные полисахариды и липополисахариды, лецитин, холестерин, ланолин, агар, глицерин, желатин, крахмал, пектины, протамины и др.)
Неорганические вещества (гидроксид алюминия, фосфат алюминия, хлорид кальция, фосфат кальция, гидроксид железа, аммониево-кальциевые квасцы, минеральные масла и др.)
Синтетические вещества (олигонуклеотиды, CpGОДН, полианионные соединения (полианионные полимеры) и др.).
Кроме простых адъювантов, используют сложные, представляющие собой смеси липидов с минеральными сорбентами, масел с липополисахаридами и эмульгаторами, микроорганизмов с маслами и другими веществами. Из сложных адъювантов наиболе известен адъювант Фрейнда.
Адъюванты:
Неполный адъювант Фрейнда - Представляет собой водно-жировую эмульсию, содержащую вазелиновое масло, ланолин и эмульгатор. Депонирует антиген и усиливает его захват фагоцитами.
Полный адъювант Фрейнда - Включает в себя, кроме вышеперечисленных компонентов, БЦЖ или мурамилдипептид. Это позволяет ему дополнительно активировать макрофаги и костимулировать Т-клетки.
Алюминиевые квасцы - Гидроксид алюминия, который благодаря высокой способности к сорбции выполняет функцию антигенного депо, а также неспецифически усиливает фагоцитоз.
Bordetella pertussis с квасцами - Изготовлен из ослабленного штамма B. pertussis, сорбированного на гидроксиде алюминия. Действие гидроксида алюминия дополняется активацией макрофагов и костимуляцией Т-клеток.
Иммуностимуляторный комплекс (ISCOM) - Представляет собой липидные мицеллы, окружающие белковые (чаще всего вирусные) частицы. Частицы антигена доставляются непосредственно в цитозоль Т-клеток, чем достигается индукция Т- киллеров.
4.Вакцины, классификация.
Вакцины - Препараты, получаемые из живых аттенуированных или убитых штаммов и их антигенов, предназначенные для создания активного иммунного ответа в организме привитых людей и животных.
Классификация:
Живые (аттенуированные) – основу препарата составляют ослабленные м/о (возбудители болезней). Выработка адекватного иммунного ответа (корь, грипп, туберкулез, полиомиелит, нат. и ветр. оспа).
Убитые (инактивированные) – в составе мертвые бактерии или их фрагменты. Инактивируют температурой, радиацией, уф-лучами (физически) и химически (спирт, ацетон, формальдегид). Против гриппа, гепатита а, полиомиелита, холера, герпес, коклюш.
Расщепленные (сплит-вакцины) - содержат разрушенные инактивированные вирионы, при этом сохраняя все белки вируса (против гриппа).
Субъединичные (химические) - состоят из отдельных антигенов, способных обеспечить надежный иммунный ответ у привитого. На белковом носителе – коклюш, гепатит б, полисахаридные - менингококковая, пневмококковая, конъюгированные - менингококковая, пневмококковая.
Анатоксины – инактивированные или убитый токсин бактерий. Вызывается иммунный ответ на действие токсина. Анатоксин адсорбируется на соли алюминия, чтобы увеличить иммунный ответ (столбняк, дифтерия) .
Рекомбинантные - применяют методы генной инженерии, встраивая генетический материал микроорганизма в дрожжевые клетки, продуцирующие антиген (впч, гепатит б).
Комбинированные (поливакцины) - комбинация антигенов в одной и той же инъекции с целью профилактики различных заболеваний или защиты против множественных
штаммов инфекционных агентов, которые вызывают одно и то же заболевание (например, комбинированная вакцина АКДС включает антигены дифтерии, коклюша и столбняка).
Поколения вакцин:
1 – цельновирионные
2 – расщепленные
3 – субъединичные
4 – адъювантные
5.Иммунобиологические препараты на основе специфических антител. Классификация.
Иммунобиологические препараты имеют сложный состав, отличаются по своей природе, способам получения и применения, целевому назначению. Однако, их объединяет то, что они действуют или на иммунную систему, или через иммунную систему, или же механизм их действия основан на иммунологических принципах.
Внастоящее время выделяют 5 групп ИБП:
первая группа — К ним относятся живые и инактивированные корпускулярные вакцины, субклеточные вакцины из микробных продуктов, анатоксины, бактериофаги, пробиотики;
вторая группа — ИБП на основе специфических антител. К ним относятся иммуноглобулины, иммунные сыворотки, иммунотоксины, антитела-ферменты (абзимы), моноклональные антитела.
Антитела - белковые соединения плазмы крови, препятствующие размножению микроорганизмов и нейтрализующие выделяемые ими токсические вещества. В зависимости от природы и свойств антигенов, к которым они образуются, антител могут быть антибактериальными, противовирусными, антитоксическими, противоопухолевыми, антилимфоцитарными, трансплантационными, цитотоксическими, рецепторными и тд.
третья группа — иммуномодуляторы для иммунокоррекции, лечения и профилактики инфекционных и неинфекционных болезней, иммунодефицитов. Сюда относятся экзогенные иммуномодуляторы (адъюванты, некоторые антибиотики, антиметаболиты, гормоны) и эндогенные иммуномодуляторы (интерфероны, миелопептиды и др.);
четвертая группа — адаптогены — сложные химические вещества растительного, животного или иного происхождения, обладающие широким спектром биологической активности, в том числе действием на иммунную систему. Экстракты женьшеня, элеутерококка, различные бады (липиды, полисахариды, витамины);
пятая группа — диагностические препараты и системы для специфической и неспецифической диагностики инфекционных и неинфекционных болезней, с помощью которых можно обнаруживать антигены, антитела, ферменты, продукты метаболизма, биологически активные пептиды, чужеродные клетки и т. д.
6.Иммунные сыворотки. Основные понятия. Классификация.
Иммунные сыворотки получают путем гипериммунизации (т. е. многократной интенсивной иммунизации) животных (чаще всего лошади, ослы, иногда кролики) специфическим антигеном (анатоксином, бактериальными или вирусными культурами и их антигенами) с последующим, в период максимального антителообразования, кровопусканием и выделением из крови иммунной сыворотки. Иммунные сыворотки, полученные от животных, называют гетерогенными, так как они содержат чужеродные для человека сывороточные белки. Для получения гомологичных нечужеродных иммунных сывороток используют сыворотки переболевших людей (коревая, паротитная, оспенная сыворотки) или специально иммунизированных людей-доноров (противостолбнячная, противоботулиническая и другие сыворотки) либо сыворотки из плацентарной, а также абортной крови, содержащие антитела к ряду возбудителей инфекционных болезней вследствие вакцинации или перенесенного заболевания.
Из сывороток выделают иммуноглобуилны. Их очищают и концентрируют: осаждением спиртом или ацетоном нахолоде, обработка ферментами, аффинная хроматография, ультрафильтрация.
1.Антитоксические - сыворотки против дифтерии, столбняка, ботулизма, газовой гангрены, т.е. сыворотки, содержащие в качестве антител антитоксины, которые нейтрализуют специфические токсины.
2.Антибактериальные - сыворотки, содержащие агглютинины, преципитины, комплементсвязывающие антитела к возбудителям брюшного тифа, дизентерии, чумы, коклюша.
3.Противовирусныесыворотки (коревая, гриппозная, антирабическая) содержат вируснейтрализующие, комплементсвязывающие противовирусные антитела.
7.Моноклональные антитела. Получение. Преимущества и недостатки.
Моноклональные антитела — антитела, вырабатываемые иммунными клетками, принадлежащими к одному клеточному клону, то есть произошедшими из одной плазматической клетки-предшественницы.
Получаются в процессе получения гибридом (гибридная клеточная линия, полученная в результате слияния клеток двух видов: способных к образованию антител B-лимфоцитов, полученных из селезёнки иммунизированного животного (чаще всего мыши), и опухолевых клеток миеломы). Получаемые при этом гибридные линии клеток наследуют родительские свойства — способность к опухолевому росту и образованию специфических антител.
Плюсы: узкая специфичность, молекулярная однородность, получения больших количеств при низкой себестоимости, долгосрочное хранение гибридом.
Минусы: риск введения генетического материала миеломных клеток.
8.Календарь прививок. Способы введения вакцин.
Календарь прививок – документ(?), который регламентирует обоснованное проведение во все возрастные периоды человека вакцинаций определенных инф. болезней. В календаре указывается, какими вакцинами и по какой временной схеме должен быть привит каждый человек в детском возрасте и во взрослом периоде. В детском возрасте (до 10 лет) каждый человек должен быть привит против туберкулеза, кори, полиомиелита, коклюша, дифтерии, столбняка, гепатита В, а в эндемичных районах — по особо опасным заболеваниям и против этих инфекций. Фз «о вакцинопрофилактике инф.заб человека».
Способы введения:
Пероральный (через рот) - вводятся живые вакцины, защищающие от кишечных инфекций (полиомиелит, брюшной тиф).
Внутрикожный и накожный – бцж, нат. оспа, вводятся живые бактериальные вакцины, распространение микробов из которых по всему организму крайне нежелательно.
Аэрозольный, интраназальный - подобный путь введения вакцин улучшает иммунитет во
входных воротах воздушно-капельных инфекций (корь, грипп, краснуха) за счет создания иммунологического барьера на слизистых оболочках.
Безыгольный - введении вакцин с помощью безыгольных инъекторов пистолетного типа, в которых, благодаря высокому давлению, создаваемому в приборе с помощью гидравлики или инертного газа, формируется струя жидкой вакцины проникающая в необходимой объемной дозе через кожу на заданную глубину (накожно, подкожно, внутримышечно).
9.Врожденный иммунитет, функции, рецепторы врожденного иммунитета.
Врожденный иммунитет – способность организма обезвреживать чужеродный и
потенциально опасный биоматериал (микроорганизмы, трансплантат, токсины, опухолевые клетки, клетки, инфицированные вирусом), существующая изначально, до первого попадания этого биоматериала в организм. Наиболее ранний защитный механизм как в плане эволюции, так и по времени ответа; Развивается быстро в течение нескольких часов, задолго до развития адаптивной иммунной реакции; Играет важную роль в реакции на повреждение собственных клеток - асептического воспаления;
Функции:
Удаление апоптических и некротических клеток;
Элиминация бактерий из организма;
Воспаление;
Распознавание РАМР (Pathogen-Associated Molecular Pattern) микробов – молекулярные структуры м/о.
Рецепторы:
Мембранные рецепторы. Эти рецепторы расположены как на наружных, так и на внутренних мембранных структурах клеток.
TLR (Toll-Like Receptor - Toll-подобный рецептор; т.е. сходный с Toll-рецептором дрозофилы). Одни из них непосредственно связывают продукты патогенов (рецепторы для маннозы макрофагов, TLR дендритных и других клеток), другие работают совместно с иными рецепторами.

Цитоплазматические рецепторы:
NLR (NOD-подобные) рецепторы включают в себя 22 человеческих и 34 мышиных белка с функциями АТФаз, подразделяющаяся на подгруппы на основании характеристик их эффекторного N-концевого домена. Эффекторные домены NOD подобных рецепторов реагируют с аналогичными доменами киназ или каспаз и передают активационные сигналы. Сходная черта для всех рецепторов наличие в их структуре центрального домена NACHT (NOD – Nucleotidebinding Oligomerization Domain) – нуклеотидсвязывающий домен олигомеризации. С-концевой лиганд LRR – домен обеспечивает специфичность распознавания лигандов.
- RIG-подобные рецепторы (RLR, RIG-Like Receptors): RIG-I (Retinoic acid-Inducible Gene I), MDA5 (Melanoma Differentiation-associated Antigen 5) и LGP2 (Laboratory of Genetics and Physiology 2). Все три рецептора, кодируемые этими генами, имеют сходную химическую структуру и локализуются в цитозоле. Рецепторы RIG-I и MDA5 распознают вирусную РНК. Роль белка LGP2 пока неясна; возможно, он выполняет роль хеликазы, связываясь с двуцепочечной вирусной РНК, модифицирует её, что облегчает последующее распознавание с помощью RIG-I. RIG-I распознаёт односпиральную РНК с 5-трифосфатом, а также относительно короткие (<2000 пар оснований) двуспиральные РНК. MDA5 различает длинные (>2000 пар оснований) двуспиральные РНК. Таких структур в цитоплазме эукариотической клетки нет. Вклад RIG-I и MDA5 в распознавание конкретных вирусов зависит от того, образуют ли данные микроорганизмы соответствующие формы РНК.
10. Врожденный и приобретенный иммунитет. Механизмы их взаимодействия.
Взаимосвязь врожденного и адаптивного иммунитета.
• Врожденный иммунитет обеспечивает презентацию антигена b костимуляцию, необходимые для запуска адаптивного иммунитета.
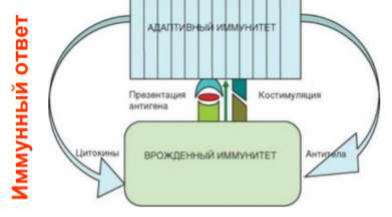
• Адаптивный иммунитет, благодаря выработке антител и цитокинов придает реакциям врожденного иммунитета избирательность действия и повышает их эффективность.
11.Свойства рецепторов врожденного иммунитета, механизм действия.
Свойства:
Уникальность – одинаковые у всех клеток опреленного гистотипа, одинаковы и растворимые рецепторы.
Геномная последовательность – кодируется непосредственными генами «зародышевго генома».
Диапазон распознавания – распознает широкие группы патогенов.
Специфичность – распознает «чужое микробные РАМР», попавшие в организм, а также «сигналы опасности» от поврежденных клеток организма.
Распознаваемые детерминанты – повторяющиеся характерные и консервативные структуры углеводов, липидов, двухцепочечной рнк, неметилированный СpG-мотив бакт. ДНК и некоторые другие маркеры патогенов.
Скорость развития иммуного овтета - после связывания патогена безотлагательно развиваются процессы, направленные на деструкцию (быстрый ответ).
Механизм иммунного реагирования
•Твердые и растворимые антигены эффективно интернализуются фагоцитозом и макропиноцитозом соответственно.
•Интернализованные антигены распознаются Toll-like рецепторами (TLR) на дендритных клетках, что приводит к активации Т-клеток (хелперов).
•CD8 + и CD4 + Т-клетки (хелперы) экспрессируют рецепторы, которые распознают фрагменты антигенов (пептиды), связанные с классом MHC I и II соответственно. Антиген деградирует и пептид связывается с молекулами МНС профессиональной антиген презинтирующей клетки (АПК).
•Для активации Th (Т-helper) клетки требуется 2 сигнала:
1.Т-клеточный рецептор связанный с MHC – II
2.Интерлейкин-1, который экспрессирует АПК.
•Активированные Th-клетки формируют интерлейкин2 и другие цитокины необходимых для активации Вклеток.
•Т-Клетки активируются, когда они контактируют с представленными антигенами, ассоциированными с молекулами МНС класса I.
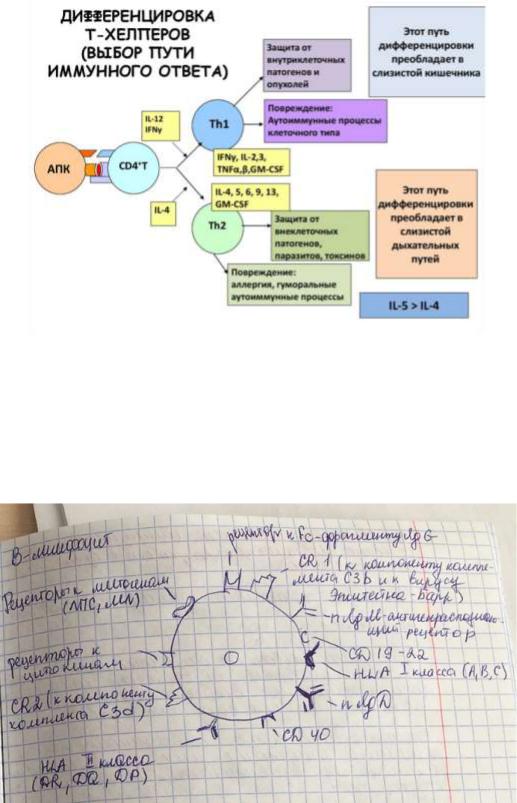
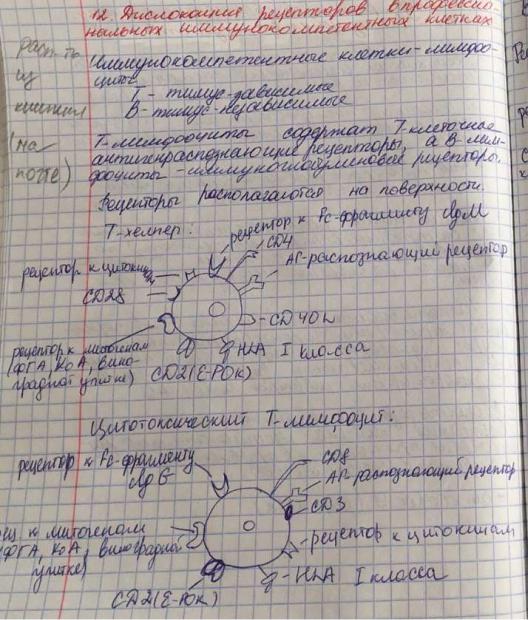
12. Дислокация рецепторов в профессиональных иммунокомпетентных клетках.
13. Свойства идеального иммуноадъюванта. Основные проблемы при разработке адъювантов, побочные эффекты.
Свойства и.и.:
Безопасность
Препарат вызывает сильный иммунный ответ со слабым антигеном, включая конъюгаци полисахарид-белок в более низких дозах антигена и с меньшим количеством инъекций.
Способствовал соотв. иммунному ответу, а именно клеточному или длительному иммунитету в зависимости от требований
Адъювант должен быть стабильным в отношении адъювантности и токсичности, нет взаимодействия с антигеном
Биодеградируемый и иммунологически инертный
Коммерчески доступный
Проблемы при разработке:
Ограниченная адъювантность (пример: соединения алюминия не проявляют адъювантного эффекта при использовании с тифозной вакциной, антигеном гемаглютинина)
Для предварительной оценки адъювантов используются вакцинные антигены, такие как столбнячный анатоксин, дифтерийный токсоид, коклюш токсоид в дозах, которые не являются максимальными для этой модели животных или рекомендуемыми минимальными пороговыми дозами. Дифтерийный токсоид являлся слабым иммуногеном.
Модели животных: нет надежных моделей животных для многих болезни, против которых разрабатываются вакцины.
Проблемы с анализом, особенно в случаях сложных адъювантных форм, когда вместе
несколько адъювантов представляют собой комплекс, который невозможно разделить на составляющие компоненты.
Побочные эффекты:
Токсичность (стимуляция в минимальными побочными эффектами)
Локальные реакции: воспаление4 местная боль и частичная некротизация тканей; появление гранулем и реакции гиперчувствительности.
Системные эффекты: повышение тем-ры; лихорадка и т.д.
14.Механизм действия иммуноадъювантов.
1.Адъюванты помогают миграции антигенов в лимфатические узлы, где они могут быть распознаны Тклетками.
2.Адъюванты обеспечивают физическую защиту антигенов (депонирование), пролонгируя их действие ИС.
3.Адъюванты вызывают локальные реакции в месте инъекции, вызывающие больший выброс сигналов«опасности» хемокинами, продуцируемыми хелперные Т-клетками и тучные клетки ИС.
4.Адъюванты увеличивают реакцию врожденного иммунитета в ответ на антиген путем взаимодействия с Tollподобными рецепторами (TLR) на иммунокомпетентных клетках.
15. Широко распространенные иммуноадъюванты. Алюмосодержащие иммуноадъюванты, сквален.
Алюмосодержащие (фосфат алюминия, гидроксид алюминия), механизм действия:
1.Формирование депо антигена в тканях.
2.Прямое воздействие на АПК - усиление иммунного ответа на ДНК-вакцины, при смешении с адъювантами фосфата алюминия.
3.Прямая активация дендритных клеток.
4.Было обнаружено, что гидроксид алюминия является более мощным адъювантом, чем фосфат алюминия.
5.Гидроксид алюминия показал более высокую адсорбцию столбнячного токсоида и дифтерийного анатоксина, чем фосфат алюминия при комнатной температуре, при рН 6,0. Адсорбционные механизмы: основные механизмы, с помощью которых алюминийсодержащие аъюванты адсорбируют антигены:
электростатическое притяжение - на основе изоэлектрической точки
гидрофобные силы (испытания с этиленгликолем).
обмен лигандами - происходит с фосфорилированными антигенами
Сквалены:
Комбинированные адъюванты на основе сквалена: МF59, AS03. MF59 представляет собой эмульсию. Состав MF59: Tween 80 - водорастворимое поверхностно-активное вещество; Span 85 - масло-растворимое поверхностно-активное вещество; 4,3% скваленого масла; вода для инъекций;10 нМ Na-цитратный буфер.
AS0: сквален, дл-а-токоферол, полисорбат 80. Механизм действия:
Эмульсия действует как система прямой доставки и ответственна за поглощение антигена АПК (антигенпредставляющие клетки).
Прямое влияние на уровни цитокинов in vivo, активирует их синтез.
Недавние исследования подтвердили способность MF59 (AS03) воздействать на иммунные клетки непосредственно, вызывая высвобождение хемокинов и других факторов, ответственных за активацию и созревание иммунных клеток.
16. Адъюванты полученные из микроорганизмов, ISCOM, липосомальные иммуноадъюванты.
М/о:
Компоненты бактерий или грибков являются продуктивным источником веществ неспецифично воздействующих на иммунную систему. Пептидогликаны бактериальной клеточной стенки или липополисахариды усиливают иммунный ответ, как врожденный, так и адаптивный при введении совместно с антигеном.
Основные адъюванты из м/о:
а) мурамилдипептид – в физ.растворе усиливает гуморальный иммунитет, часто в составе липососм.
б) липид а (монофосфорил липид а) – получают из клеточной стенки грамотр бактерй. Липид А в условиях низкой кислотности гидролизуется в монофосфориловый липид а, который сохраняет адъювантную активность липида а, но обладает более низкой системной токсичностью
в) трегалоза димиколат – стимулирует гуморальный и клеточный ответ. Соединение миколовых кислот получаемых из микобактрий.
ISCOM Immune stimulating complexes Иммуностимулирующие комплексы:
ISCOM представляют собой крупные частицы размером 40 нм, состоящие из сапонинов (Quil A), липидов, холестерина и антигена, удерживаемых вместе гидрофобными взаимодействия между тремя компонентами. Холестерин является лигандом, который связывается с сапонином, образующим 12 нм кольца. Эти кольца фиксируются вместе липидами с образованием сферических наночастиц. Гидрофобные антигены могут быть также включены в этот комплекс.
Они представляют собой универсальные и гибкие системы доставки с увеличенной эффективностью представления антигена В-клеткам и поглощения АПК. Вакцины являются мощным индуктором как гуморального, так и клеточного иммунного ответа. •Использование сапонинов в вакцинах на основе ISCOM сохраняет адъювантную активность сапонинового компонента, но токсичность в комплексе снижена. Технология ISCOM также способна индуцировать адаптивный иммунный ответ в присутствии ранее существовавших антител, например у новорожденных, имеющих материнские антитела.
Липосомы:
Липосомы представляют собой синтетические сферы, состоящие из липидных бислоев, которые могут инкапсулировать антигены и действовать как как средство доставки вакцины, так и адъювант.
Эффективность липосом зависит от количества липидных слоев, электрических заряд, состав и способ приготовления. Липосомы создают депо в месте инъекции и эффективное презентируют антигены макрофагам (крупные клетки) и другим АПК. Липосомы способны вызывать, как гуморальный, так и клеточный иммунный ответ. Иммуностимуляторы при инкапсулировании внутри липосомы проявляют повышенную адъювантность с уменьшенными побочными эффектами.
Однако фосфолипидные липосомы имеют определенные ограничения, повышенная чувствительность к фосфолипазам хозяина, нестабильность при хранении, высокая стоимость производства и трудности его масштабирования. Для преодоления этих проблем с ФЛЛ были разработаны нефосфолипидные липосомы. Эти нефосфолипидные липосомные везикулы, состоящие из диоксиэтилен ацетатного эфира, холестерина и олеиновой кислоты, их работу оценивали в составе с человеческими вакцинными антигенами (столбнячные и дифтерийные токсоиды) у кроликов и мышей. Столбнячные и дифтерийные анатоксины, инкапсулированные или смешанные с этими липосомами, вызывают уровень образования антител, подобные тем, которые вызываются антигенами с использованием FCA или при адсорбции антигена на алюминиевых адъювантах.
17. Виросомы, PLG, адъюванты на основе нуклеиновых кислот, CpG-ДНК, неметилированные фрагменты ДНК.
Виросомы – тип липосом, содержащие мембранный гемагглютинин и нейраминидазу, полученные из вируса гриппа. Служат для усиления фузогенной активности (сливаться) и
