
Гидролиз
.docxФедеральное государственное бюджетное образовательное учреждение высшего образования
«ПЕТЕРБУРГСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ ПУТЕЙ СООБЩЕНИЯ Императора Александра I»
Кафедра «ИНЖЕНЕРНАЯ ХИМИЯ И ЕСТЕСТВОЗНАНИЕ»
ОТЧЁТ
ПО ЛАБОРАТОРНОЙ РАБОТЕ №3
«Гидролиз солей»
Выполнил:
студент Григорьев Ф.М.
группы АТ-603
Проверила:
Шредник Н.А
Санкт-Петербург
2016
Цель работы:
Цель работы - изучение реакций гидролиза различных типов солей по изменению рН, а также влияния концентрации растворов этих солей рH, значение которого рассчитывается теоретически, а затем проверяется экспериментально и визуально.
Основные теоретические положения:
Гидролиз – это процесс обменного взаимодействия между ионами раствора соли и водой, в результате которого образуется слабодиссоциирующее соединение и изменяется рН среды.
Гидролизу подвергаются три типа солей:
Соль, образованная сильной кислотой и слабым основанием.
Соль,образованная слабой кислотой и сильным основанием.
Соль, образованная слабой кислотой и слабым основанием.
Соль, образованная сильной кислотой и сильным основанием, гидролизу не подвергается.
Ход работы:
1. Написать уравнение гидролиза соли (если он возможен) в ионном и молекулярном виде.
2. Рассчитать рН растворов соли концентраций М1 и М2,.
3. Сделать вывод о влиянии разбавления раствора на сдвиг равновесия процесса гидролиза и на величину рН раствора.
1. Уравнение гидролиза соли :
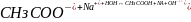
(полное ионное уравнение);
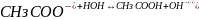
(сокращенное ионное уравнение);
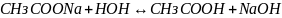
(молекулярное уравнение).
2. Расчет рН растворов соли концентраций М1 и М2.
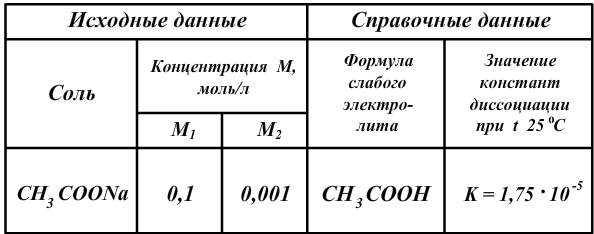
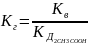 ;
;
Расчет рН соли с концентрацией 0,1 моль:
 =
=
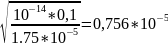 моль/л
моль/л
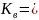
моль/л
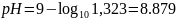
Расчет рН соли с концентрацией 0,001 моль:
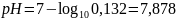

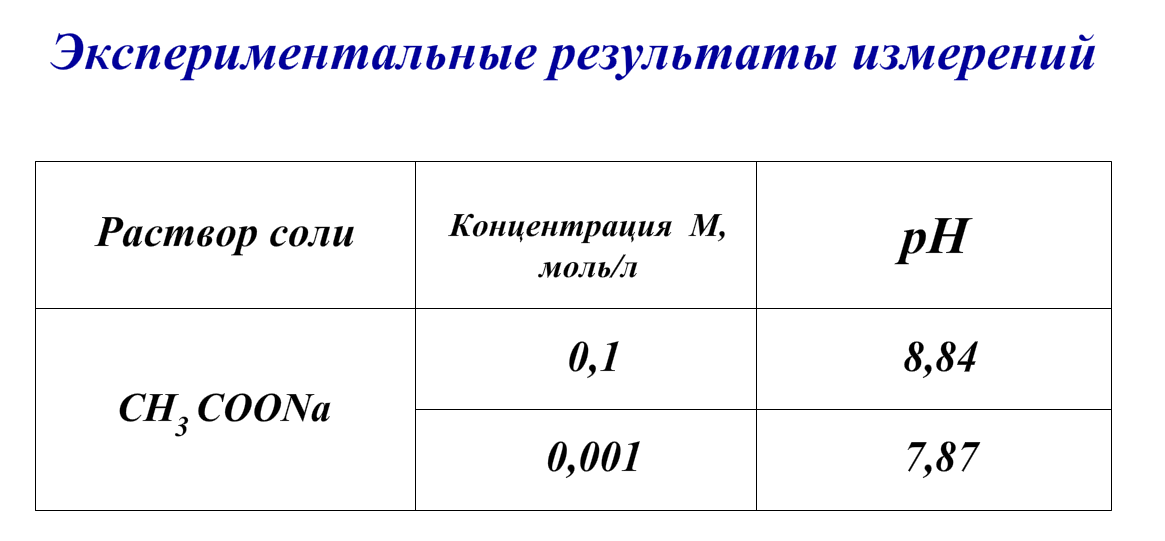
Сравнение результатов:
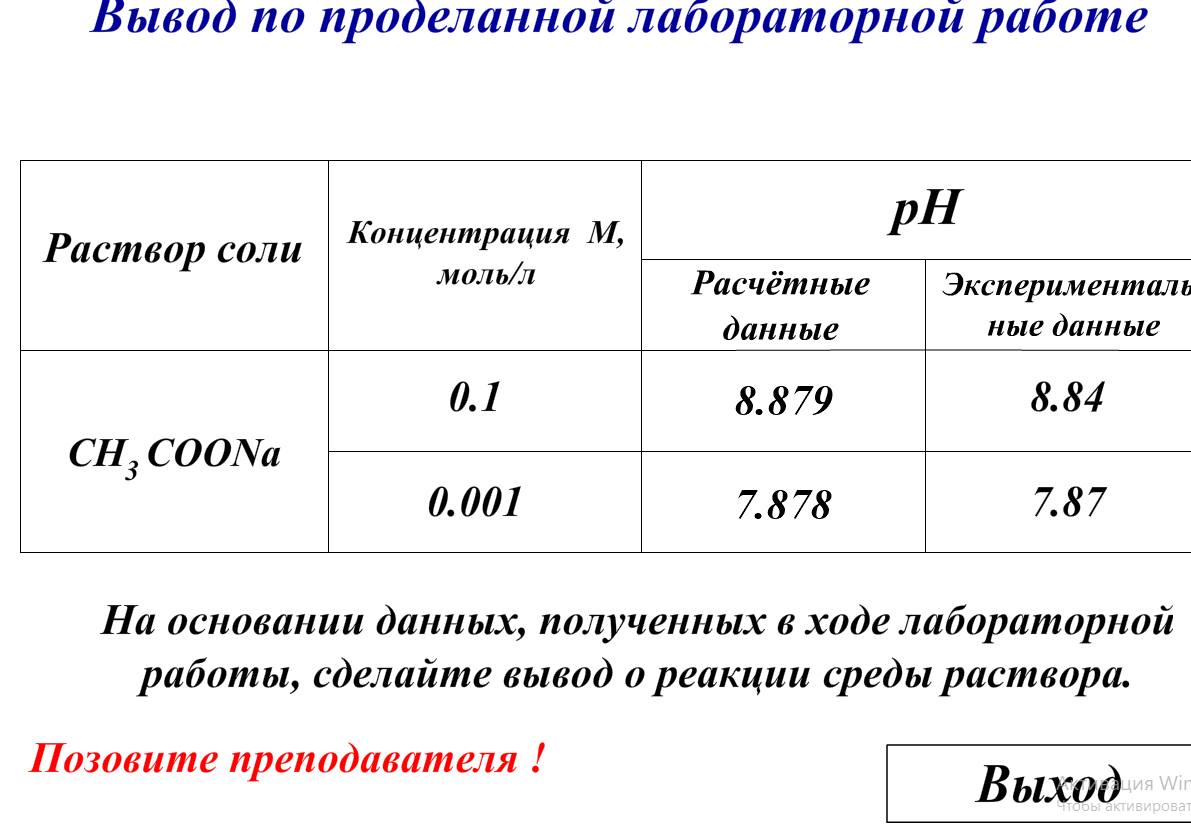
Вывод: был рассмотрен гидролиз соли, произведен расчет рН при разных концентрациях раствора соли и была выявлена зависимость рН от концентрации раствора (чем больше концентрации тем больше рН).
