
- •Лабораторная работа № 1. Строение и свойства аминокислот, пептидов и белков.
- •Контрольные вопросы
- •Лабораторная работа № 2. Строение и свойства углеводов.
- •Контрольные вопросы
- •Лабораторная работа № 3. Нуклеиновые кислоты и их структурные компоненты.
- •Контрольные вопросы
- •Лабораторная работа № 4 Изучение свойств липидов и их структурных компонентов.
- •Контрольные вопросы
Лабораторная работа № 1. Строение и свойства аминокислот, пептидов и белков.
Цель работы: Научиться экспериментально доказывать наличие функциональных групп в аминокислотах, пептидной связи и индивидуальных аминокислот в белках.
Реактивы: 1 %-ный раствор глицина, 1 %-ные растворы яичного белка и желатина; 5 %-ный раствор хлорида железа (III), 5 %-ный раствор сульфата меди (II), 10 %-ный раствор гидроксида натрия, 10 %-ный раствор ацетата свинца (II); концентрированная азотная кислота.
Опыт 1. Реакция аминокислот с хлоридом железа (III).
К 1 мл 5 %-ного раствора глицина добавляют несколько капель 5 %-ного раствора хлорида железа (III). Раствор слегка нагревают до изменения окраски.
Уравнение реакции:
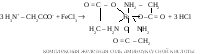
Опыт2. Биуретовая реакция на пептидную связь.
В 2 пробирки помещают по 5 - 6 капель раствора яичного белка и желатина; добавьте равный объем 10 %-ного водного раствора гидроксида натрия и 1 - 2 капли раствора сульфата меди(II). Наблюдается появление красно-фиолетовой окраски.
Опыт 3. Ксантопротеиновая реакция белков.
В 2 пробирки помещают по 10 капель раствора яичного белка и желатина; добавьте 2 - 3 капли концентрированной азотной кислоты, осторожно нагрейте, все время встряхивая. Раствор и осадок окрашиваются в желтый цвет. Охладив пробирку, осторожно добавьте 2 - 3 капли 10 %-ного водного раствора гидроксида натрия до появления ярко-оранжевой окраски.
Опыт 4. Реакция на наличие серусодержащих - аминокислот (реакция Фоля).
В 2 пробирки помещают по 10 капель раствора яичного белка и желатина; добавьте вдвое больший объем 10 %-ного раствора гидроксида натрия; перемешайте, нагрейте до кипения (1 - 2 мин). К полученному щелочному раствору добавьте 5 капель 10 %-ного раствора ацетата свинца (II) и вновь прокипятите. Наблюдается появление серо-черного осадка.
Контрольные вопросы
1. Хорошо ли растворяются аминокислоты в воде? Ответ поясните. Почему водные растворы моноаминокислот имеют практически нейтральную реакцию?
2. Каким образом связаны остатки -аминокислот в белковых молекулах? Можно ли с помощью биуретовой реакции отличить раствор аминокислоты от раствора белка?
3. Напишите схему синтеза трипептида, образованного аланином, глицином и лейцином.
4. О наличии каких аминокислот в белках и полипептидах свидетельствует реакция Фоля? А ксантопротеиновая реакция?
Лабораторная работа № 2. Строение и свойства углеводов.
Цель работы: изучить основные химические свойства моно- и полисахаридов.
Реактивы: 1 %-ные растворы глюкозы, сахарозы, лактозы, фруктозы; 10 %-ные растворы гидроксида натрия и серной кислоты; 2 %-ный раствор сульфата меди (II); реактив Толленса (аммиачный раствор оксида серебра), раствор йода; реактив Селиванова (0,5 % раствор резорцина в 20 %-ном водном растворе НС1); 0,5 %-ный раствор крахмала
Опыт 1. Моно- и дисахариды как восстановители.
Опыт 1.1. В три пробирки помещают по 10 капель 1 %-ного раствора глюкозы, сахарозы и лактозы соответственно; добавьте в каждую пробирку 1 мл 10 %-ного раствора гидроксида натрия и 1 - 2 капли раствора CuSO4. Осторожно нагрейте над пламенем горелки так, чтобы грелась только верхняя часть раствора (не кипятить). Отмечают наблюдаемые изменения.
Уравнение реакции:

Опыт 1.2. В пробирку наливают 3 мл аммиачного раствора оксида серебра (реактива Толленса) и добавляют 1,5 мл 1 %-ного раствора глюкозы. Пробирку нагревают на водяной бане при температуре 70 - 80 °С, наблюдают выделение металлического серебра на стенках пробирки («серебряное зеркало»). Если пробирка была недостаточно чистой или во время нагревания сильно встряхивалась, серебро выпадает в виде черного осадка.
По такой же методике проводят реакцию аммиачного раствора оксида серебра с 1 %-ным раствором фруктозы, наблюдают образование «серебряного зеркала». При нагревании кетоз в щелочной среде происходит их
изомеризация с образованием эпимерных альдоз, легко окисляющихся реактивом Толленса
У равнение
реакции:
равнение
реакции:
Опыт 2
В одну пробирку помещают 10 капель 1 %-ного раствора фруктозы, в другую – столько же 1 %-ного раствора глюкозы, добавляют в обе пробирки по 1 мл реактива Селиванова. Осторожно нагревают над пламенем горелки. В лабораторном журнале отмечают наблюдаемые изменения.
Опыт 3. Качественная реакция на крахмал.
В пробирку помещают 5 капель 0,5 %-ного раствора крахмала и 1 каплю разбавленного раствора йода. Раствор окрашивается в синий цвет. При нагревании раствор обесцвечивается; при охлаждении окраска восстанавливается.
Опыт 4. Кислотный гидролиз крахмала.
В пробирку помещают 0,5 мл 0,5 %-ного раствора крахмала. Добавьте 1 мл 10 %-ного раствора серной кислоты и поместите пробирку в кипящую баню. Мутный раствор крахмала становится прозрачным примерно через 20 мин. Помещают 2 - 3 капли гидролизата в пробирку и добавьте 1 каплю разбавленного раствора йода в йодиде калия. Если проба не дает положительной йодкрахмальной реакции (синего окрашивания), добавляют в пробирку 8 капель 10 %-ного гидроксида натрия для создания щелочной среды. Затем добавьте 1 каплю 2 %-ного раствора сульфата меди (II). Будет ли положительной проба Троммера?
Схема гидролиза крахмала:
Крахмал (С6Н10О5)n амилодекстрины эритродекстрины
ахроодекстрины n/2 С12Н22О11 (мальтоза) n С6Н12О6 (D-глюкоза)
