
Тема Теория химического строения а.М.Бутлерова.
Основные положения теории химического строения А.М.Бутлерова такие:
атомы в молекулах соединяются в соответствии с их валентностью, углерод имеет валентность 4, его атомы обладают свойством соединяться друг с другом в цепи;
свойства веществ зависят не только от того, атомы каких элементов и в каком количестве входят в состав молекул, но и от последовательности соединения атомов в молекулах, от взаимного влияния их друг на друга;
атомы, связанные в молекулу, влияють друг на друга. Наибольшее влияние выявляють атомы, непосредственно соединенные друг с другим.
Способность атомов углерода соединяться друг с другом и с атомами других элементов в определенном порядке и образовывать разные вещества называют изомериею.
Изомеры - это вещества, которые имеють однаковый состав, но разное строение и различные химические свойства.
Гомологи – вещества, отличающиеся друг от друга гомологической разницей [-СН2 -].
Классификация и номенклатура органических соединений.
Тривиальная номенклатура - на основе случайных или исторически возникших названиях.
Рациональная номенклатура – от названий соединений одного из членов соответствующего гомологического ряда.
Межнародная номенклатура (IUPAC) за основу берут углерод - углеродную цепь, которая содержит главную характерную функциональную группу. Все другие группы в цепи расматривають как заместители и перечисляют в названии по алфавиту. Заместители, которые содержат только углеродные атомы, называють радикалами.
Положения заместителей в цепи обозначають числами, а колличество их приставками – греческими числителями: ди-2, три-3, тетра-4, т.д.
Классы органических соединений
Функциональная группа |
Название группы |
Классы соединений |
Общая формула |
Пример |
-ОН |
гидроксил |
спирты, фенолы |
R-OH |
СН3-ОН |
=С=О |
карбонил |
альдегиды, кетоны |
R – C-НО R1 R2 – C=O |
СН3 -СНО СН3-СО-СН3 |
-СООН |
карбоксил |
карбоновые к-ы |
R-NO2 |
СН3 СООН |
-NO2 |
нитро- |
нитросоединения |
R-NО2 |
СН3-NO2 |
- NН2 |
амино- |
амины |
R-NH2 |
СН3-NН2 |
-F, –CI, -Br, -I |
галоген |
галогенпроизводные |
R-HaI |
СН3-СІ |
Основные формулы:
DH2
=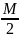 ; DN2=
; DN2=
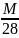 ; DO2=
; DO2=
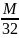 ;
DCO2=
;
DCO2=
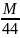 ; DH2O=
; DH2O=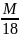 ;
Dвозд
=
;
Dвозд
= ; w =
; w =
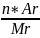 *100% ; n =
*100% ; n =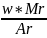 * 100% .
* 100% .
ТемаАлканы
Насыщенные углеводороды (алканы) СпН2п+2 C-C-С
изомерия углеродной цепи С1-С4- газы С5-С15- жидкости С16- твердые вещества
sp3 -гибридизация 4 σ- связи 109028΄ 0,154 нм
Получение алканов
1) C + 2H2 → CH4 2) CO + 3H2→ CH4 + H2O 3) CH3Br + 2Na + BrH3C → CH3- CH3 + 2NaBr (реакция Вюрца)
Химические свойства алканов
1) CH4 + СI2 → CH3CI…→CCI4 2) CH4 +2O2 → CO2 + 2H2O 3) C4H10 → C4H8 + H2 4) C4H10 → H2C=CH2 +CH3- СH3
Применение алканов
Топливо, получение хлорофоса, резины, фреонов, водорода, типографских красок, средство гашения пламени, в медицине как местная анестезия, для производства пластмасс, обезжиривающее средство.
