
- •1.Углеводороды. Алканы. Определение. Реакция свободно – радикального замещения – галогенирование, нитрование.
- •3. Угливодороды. Алкины. Определение. Химические свойства: реакции галогенирования, гидрогалогенирования, гидротации на примере пропана.
- •4.Угливодороды. Алкины. Химические свойства: кислотные свойства, реакции окисления и восстановления на примере ацителена.
- •5.Ароматические углеводороды. Гамологи аренов. Реакции боковой цепи.
- •7. Спирты. Определение. Химические свойства: реакция этерификации, отличие от многоатомных спиртов.
- •8.Фенолы. Определение. Химические свойства одноатомных фенолов – реакция углеводородного радикала.
- •9. Реакция гидролиза ацетилсалициловой кислоты.
- •10. Альдегиды. Определения. Химические свойства: взаимодействие с циановодородной кислотой, с водой.
- •11.Амиды кислот. Определение. Мочевина. Получение. Характеристика свойств: основные свойства.
- •12. Амины. Определение. Химические свойства: основные свойства, реакции алкилирования и ацилирования.
- •13. Соли диазония. Определение. Реакция азосочетания с фенолами и ароматическими аминами.
- •14.Аминокислоты. Определение. Химические свойства: кислотно-основные свойства.Реакция поликонденсации (образование дипептида).
- •15. Пятичленные гетероциклы с одним гетероатомом: пиррол, тиофен, фуран. Структурные формулы . Реакции сульфирования и нитрования для пиррола.
- •16. Одноосновные карбоновые кислоты. Определение. Химические свойства: реакция этерификации, образование галогенангидридов.
- •17. Сложные эфиры. Определение. Химические свойства: кислотный и щелочной гидролиз сложных эфиров на примере этилового эфира уксусной кислоты.
- •18. Триацилглицерины. Жиры. Определение. Химические свойства: гидролиз, гидрогенизация.
- •19. Двухосновные карбоновые кислоты. Определение. Особенности поведения при нагревании (специфические свойства)щавельной и янтарной кислот.
- •20.Гидроксикислоты. Определение. Характеристика специфических свойств (отношение к нагреванию).
- •21. Фенолокислоты. Определение. Химические свойства: реакции по фенольной гидроксильной группе.
- •22. Реакция окисления глюкозы реактивом Фелинга.
- •36. Качественная реакция на Теобромин (Theobrominum)
- •37. Реактив Толленса. Его применение в качестве реактива в органической химии.
- •38. Качественная реакция на глютаминовую кислоту (acidum qlytaminicum)
- •3 9. Качественая реакция на салициловую кислоту (Salicylic acid)
- •40. Качественная реакция на антипирин с нитратом натрия в кислой среде.
- •57. Качественная реакция на первичный ароматический амин на примере анилина.
- •58. Как отличить салициловую кислоту от ацетилсалициловой с помощью качественной реакции.
- •61. Качественная реакция на бензойную кислоту, условия проведения реакции.
- •66. Реакция гидролиза этилового эфира уксусной кислоты. Условия реакции.
- •67.Специфические свойства β – гидроксикислот (отношение к нагревании)
- •68.Качественная реакция на уксусную кислоту – реакция этерификации
- •73Вопрос
- •74Вопрос
- •75 Вопрос
- •97. Применение растительных масел в медицине. Напишите общую формулу триацилглицерина.
- •98. Уксусная кислота. Латинское название. Применение в медицине салицилового эфира уксусной кислоты (ацетилсалициловой кислоты)
- •99. Глюкоза. Структурная формула, латинское название, применение в медицине.
- •100. Глютаминовая кислота. Структурная формула, латинское название, применение в медицине.
- •101. Аминоуксусная кислота (глицин). Структурная формула, латинское название, применение в медицине.
- •102. Кальция глюконат. Структурная формула, латинское название, применение в медицине.
22. Реакция окисления глюкозы реактивом Фелинга.
O O O O O +продолж.
C + C – CH – CH – C Cu2O + C – CH – CH – C окисл. +H2O
 H
KO
ONa оранж.
KO
ONa
H
KO
ONa оранж.
KO
ONa
Д-глюк. O O (кирп.кр) OH OH
Cu
23. .реакция окисления глюкозы реактивом Толенса.
O
C
H
+ [ Ag (NH3)3] OH Ag + NH3 + H2O + продолжается окисления
Д-глюк. Диамин серебра
Амингидроксид или реактив Толенса
25. определение конденсированных систем. Формула ксантина. Амфотерные свойства ксантина.
конденсированных систем – назыв. орган соединения состоящие из двух и более конденсированных цифр ароматичного или кридиального характера.
Формула ксантина:
 OH+NaOH
OH+NaOH
 N
N
– H
N
N
– H
HO
N N
31.Альдегиды. Определение. Реакции окисления.
Альдегидами
называются органические соединения,которые
содержат в себе альдегидную формулу,связанную
с одним радикалом и одним атомом водорода.
Общая формула:

Реакции окисления.
С реактивом Толленса(р-ция «серебряное зеркало»)


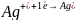 2-ОКИС-ЛЬ
2-ОКИС-ЛЬ
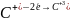 1-восс-ль
1-восс-ль
Окисление с гидроксидом меди.


С реактивом Несслера.

С реактивом Фелинга.

32.Простые эфиры. Определение. Химические свойства: взаимодействие с концентрированной йодированной кислотой в мягких и жестких условиях.
Простые эфиры- это производные спиртов фенолов, у которых атом водорода гидроксильной группы замещен на углеводородный радикал.
R-O-R
Взаимодействие с концентрированной йодированной кислотой в мягких условиях:

Взаимодействие с концентрированной йодированной кислотой в жестких условиях: при нагревании избытки галогеноводорода получается 2 галогеноводорода.

33.Соли диазония. Определение. Реакции с выделением азота.
Соли диазония- это вещества,обладающие очень высокой реакционной способностью,благодаря чему можно получать ряд соединений.
Реакции с выделением азота
Реакции азосочетания с ароматичными аминами(среда нейтральная или слабо-кислая)
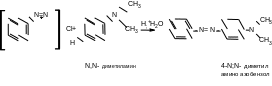
Азосочетания с фенолами.

34.Специфические свойства для α-аминокислот (отношение к нагреванию).
Специфические реакции аминокислот
Реакции с одновременным участием карбоксильной и аминогрупп идут, как правило, с образованием продуктов, содержащих термодинамически устойчивые 5-ти- и 6-тичленные гетероциклы.
Комплексообразование
a -Аминокислоты образуют прочные хелатные комплексы с ионами переходных металлов (Cu, Ni, Co, Cr и др.).
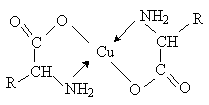
Отношение аминокислот к нагреванию
Превращения аминокислот при нагревании зависят от взаимного расположения карбоксильной и аминогруппы и определяются возможностью образования термодинамически стабильных 5-ти- 6-тичленных циклов
a -Аминокислоты вступают в реакцию межмолекулярного самоацилирования. При этом образуются циклические амиды – дикетопиперазины.
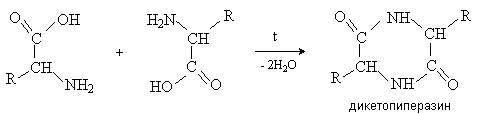
35.Качественная реакция на теофилин.
Реакции солеобразования используются в качественном анализе метилированных ксантинов. Теофиллин и теобромин в щелочной среде образуют с хлоридом кобальта (11) нерастворимые соли соответственно серо – голубого или розоватого цвета.

