
- •1.Углеводороды. Алканы. Определение. Реакция свободно – радикального замещения – галогенирование, нитрование.
- •3. Угливодороды. Алкины. Определение. Химические свойства: реакции галогенирования, гидрогалогенирования, гидротации на примере пропана.
- •4.Угливодороды. Алкины. Химические свойства: кислотные свойства, реакции окисления и восстановления на примере ацителена.
- •5.Ароматические углеводороды. Гамологи аренов. Реакции боковой цепи.
- •7. Спирты. Определение. Химические свойства: реакция этерификации, отличие от многоатомных спиртов.
- •8.Фенолы. Определение. Химические свойства одноатомных фенолов – реакция углеводородного радикала.
- •9. Реакция гидролиза ацетилсалициловой кислоты.
- •10. Альдегиды. Определения. Химические свойства: взаимодействие с циановодородной кислотой, с водой.
- •11.Амиды кислот. Определение. Мочевина. Получение. Характеристика свойств: основные свойства.
- •12. Амины. Определение. Химические свойства: основные свойства, реакции алкилирования и ацилирования.
- •13. Соли диазония. Определение. Реакция азосочетания с фенолами и ароматическими аминами.
- •14.Аминокислоты. Определение. Химические свойства: кислотно-основные свойства.Реакция поликонденсации (образование дипептида).
- •15. Пятичленные гетероциклы с одним гетероатомом: пиррол, тиофен, фуран. Структурные формулы . Реакции сульфирования и нитрования для пиррола.
- •16. Одноосновные карбоновые кислоты. Определение. Химические свойства: реакция этерификации, образование галогенангидридов.
- •17. Сложные эфиры. Определение. Химические свойства: кислотный и щелочной гидролиз сложных эфиров на примере этилового эфира уксусной кислоты.
- •18. Триацилглицерины. Жиры. Определение. Химические свойства: гидролиз, гидрогенизация.
- •19. Двухосновные карбоновые кислоты. Определение. Особенности поведения при нагревании (специфические свойства)щавельной и янтарной кислот.
- •20.Гидроксикислоты. Определение. Характеристика специфических свойств (отношение к нагреванию).
- •21. Фенолокислоты. Определение. Химические свойства: реакции по фенольной гидроксильной группе.
- •22. Реакция окисления глюкозы реактивом Фелинга.
- •36. Качественная реакция на Теобромин (Theobrominum)
- •37. Реактив Толленса. Его применение в качестве реактива в органической химии.
- •38. Качественная реакция на глютаминовую кислоту (acidum qlytaminicum)
- •3 9. Качественая реакция на салициловую кислоту (Salicylic acid)
- •40. Качественная реакция на антипирин с нитратом натрия в кислой среде.
- •57. Качественная реакция на первичный ароматический амин на примере анилина.
- •58. Как отличить салициловую кислоту от ацетилсалициловой с помощью качественной реакции.
- •61. Качественная реакция на бензойную кислоту, условия проведения реакции.
- •66. Реакция гидролиза этилового эфира уксусной кислоты. Условия реакции.
- •67.Специфические свойства β – гидроксикислот (отношение к нагревании)
- •68.Качественная реакция на уксусную кислоту – реакция этерификации
- •73Вопрос
- •74Вопрос
- •75 Вопрос
- •97. Применение растительных масел в медицине. Напишите общую формулу триацилглицерина.
- •98. Уксусная кислота. Латинское название. Применение в медицине салицилового эфира уксусной кислоты (ацетилсалициловой кислоты)
- •99. Глюкоза. Структурная формула, латинское название, применение в медицине.
- •100. Глютаминовая кислота. Структурная формула, латинское название, применение в медицине.
- •101. Аминоуксусная кислота (глицин). Структурная формула, латинское название, применение в медицине.
- •102. Кальция глюконат. Структурная формула, латинское название, применение в медицине.
66. Реакция гидролиза этилового эфира уксусной кислоты. Условия реакции.
O O
// //
СH3 - C + H2O ============ С2H5OH + CH3 - C
\ \
O- C2H5 OH
Реакция в данных условиях обратима, обратной будет реакция гидролиза полученного этилацетата (сложного эфира уксусной кислоты и этанола)
67.Специфические свойства β – гидроксикислот (отношение к нагревании)
Присоединением воды к α,β-ненасыщенным кислотам получают β-гидроксикислоты:
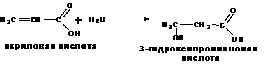
Общим способом получения β-гидроксикислот является реакция Реформатского:

При нагревании β--гидрокислот происходит отщепление одной молекулы воды от одной молекулы гидроксикислоты с образованием α,β-ненасыщенной карбоновой кислоты:
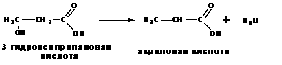
68.Качественная реакция на уксусную кислоту – реакция этерификации
Сложные эфиры могут быть получены при непосредственном взаимодействии кислоты и спирта, например:
CH3—C—OH + HO—CH2—CH3 <=> CH3—C—O—CH2—CH3 + H2O
II укс. к-та II этиловый эфир
О О уксусной кислоты
Как уже было указано, такую реакцию называют реакцией этерификации. Для органических кислот она протекает очень медленно, причем, скорость образования эфира зависит от строения исходных кислот и спирта. Скорость этерификации увеличивается при нагревании и, особенно, в присутствии минеральных кислот благодаря каталитическому действию ионов водорода. Особенно в качестве катализатора применяют серную кислоту (В.В. Марковников, 1873г.)
Реакция этерификации обратима. Это объясняется тем, что получаемый сложный эфир гидролизуется одновременно образующейся при реакции водой, и поэтому процесс идет в обратном направлении с разложением эфира на кислоту и спирт. При этом, чем больше накапливается воды, тем больше скорость обратной реакции, последняя ускоряется и при нагревании, а также под влиянием ионов водорода, вводимых для ускорения прямой реакции. Таким образом, реакция этерификации не доходит до конца, а лишь достигает состояния химического равновесия, применение же катализаторов и повышение температуры только ускоряет достижения равновесия. Соотношение всех реагирующих веществ в момент равновесия зависит от строения кислоты и спирта, а также от склонности сложного эфира к гидролизу.
Чтобы увеличить количество образующегося эфира, т.е. сместить равновесие реакции этерификации вправо одно из реагирующих веществ (то, которое доступнее) берут в избытке (в соответствии с законом действия масс). При избытке спирта в реакцию может вступить практически вся кислота, при избытке кислоты – весь спирт.
Другой способ увеличения выхода сложного эфира заключается в постоянном выведении из реакции одного из образующихся веществ – эфира или воды. Так, применяемая при этерификации в качестве катализатора серная кислота, кроме того, является веществом, связывающим воду, и таким образом способствует смещению равновесия вправо.
69. Хлорэтан. Структурная формула, название по заместительной номенклатуре, латинское название, применение в медицине
C![]() 2H5Cl
2H5Cl
Aethylii chloridum
Применяется в медицине для анестезии методом сильного охлаждения, ранее иногда использовался для ингаляционного наркоза
70.Уксусная кислота. Латинское название. Напишите уравнение реакции щелочного гидролиза этилового эфира уксусной кислоты
acidum aceticum
CH3-C-O-C2H5+H2O->CH3COOH+C2H5OH
||
O
Щелочной гидролиз:
CH3-C-O-C2H5+NaOH->CH3COONa(ацетат натрия)+C2H5OH
||
O
71вопрос
Хлоралгидрат (Chloralum hydratum).
Структурная формула: С2Н3CI3O2
 оH
оH
 Cl3
–
CH
Cl3
–
CH
оH
Название по заместительной номенклатуре 2,2,2-трихлорэтандиол-1,1
Применяют как снотворное, успокаивающее, противосудорожное.
72вопрос
Крахмал используют при приготовление присыпок, паст (густых мазей), а так же при производстве таблеток. В хирургии для приготовления не подвижных повязок.
 Качественная
реакция на крахмал (С6Н10О5)n
+ Т(йод)2
синее
окрашивание
Качественная
реакция на крахмал (С6Н10О5)n
+ Т(йод)2
синее
окрашивание
Образуется соединение включения. Крахмал, в отличие от глюкозы, не дает реакции серебряного зеркала. Подобно сахарозе, не восстанавливает гидроксид меди(II)
