
1 Жауап
1$.Газдың сутегі бойынша тығыздығы 16-ға тең болса, ол газдың молекулалық массасы қанша:
А)32
B)36
C)16
D)9
E)4
F)10
2$.Ауа сутегінен неше есе ауыр:
А)14,5
B)9,6
C)29
D)7,2
E)2
F)11
3$.Авогадро саны:
А)6,02 1023
B)6,02 10-23
C)6,021022
D)6,02 1020
E)6,02 1019
F) 6,02 1013
4$.Атомның салмақтық бірлігі:
А) 12С изотопы массасының 1/12 бөлігі
B) 12С изотопы массасының 0,12 бөлігі
C) 16О изотопы массасының 2,53 бөлігі
D) 39К изотопы массасының 1,24 бөлігі
E) 2Н изотопы массасының 1,56 бөлігі
F) 2Н изотопы массасының 1,51 бөлігі
5$.Қалыпты жағдайдағы бір моль газдың көлемі:
А)22,4
B)44,3
C)56,6
D)11,2
E)20,5
F) 20
6$.Қалыпты жағдайда температура мен қысым:
А)273 и 101,3
B)298 и 113,1
C)100 и 760
D)588 и 100
E)300 и 916,5
F) 300 и 900,5
7$.Гей-Люссак пен Бойль-Мариоттың біріккен заңдары:
А)![]()
B)![]()
C)![]()
D)![]()
E)![]()
F)
![]()
8$.22,4 л газ көлемі сипатталады:
А)2730К ж 101,3 Кпа –де 1 моль газдың көлемі;
B)2730К ж 101,3 Кпа –де газдың молярлық массасы;
C)2730К ж 101,3 Кпа –де 1 моль сутегінің көлемі;
D) 2730К ж 101,3 Кпа –де 1 моль азоттың көлемі
E) 2730К ж 101,3 Кпа –де газдың молярлық массасы;
F) 2730К ж 101,3 Кпа –де газдың массасы;
9.$ Х – затының эквивалентінің молярлық массасы-бұл :
А) Х- затының бір эквивалентінің массасы
B)Х -затының (қ. ж.) 5 литрінің массасы
C) Х- затының 1 молінің массасы
D)Х- затының 2 молінің массасы
E)Х- затының екі эквивалентінің массасы
F) Х- затының 3 эквивалентінің массасы
10. $ Эквиваленттер заңының математикалық өрнегі:
А)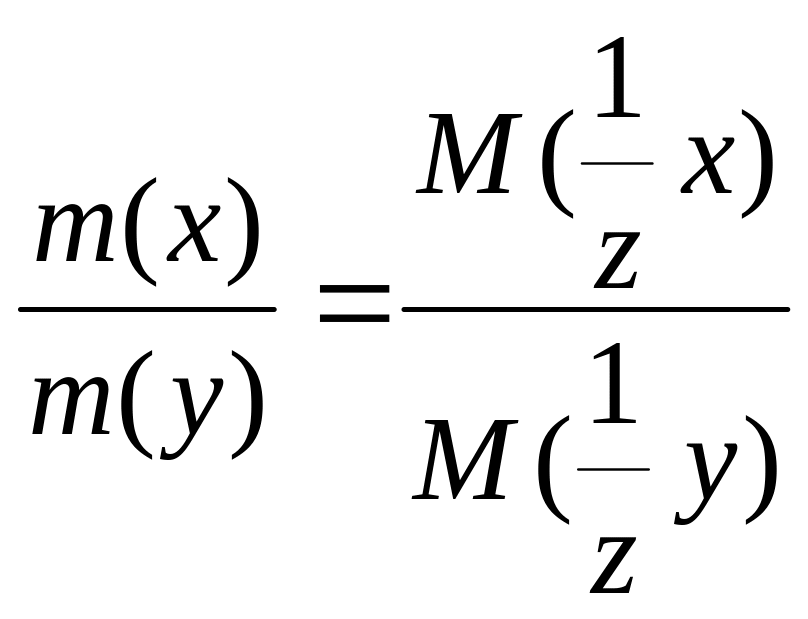
B)m(x)=M![]()
C)V(![]() /V(xy)
/V(xy)
D)V( +V(xy)
E)#
F)
11$.(Қ.ж.) 2 моль N2 құрамында молекула саны:
А)12,041023
B)6,021024
C)6,021023
D)3,011025
E)4,481022
F) 4,491022
12$.(Қ.ж.) 32г О2 құрамында молекула саны:
А)6,021023
B)3,011024
C) 3,011023
DГ)6,041024
E)6,121023
F) 6,121021
13$. 112г газдың зат мөльшері(моль):
А)30,11023
B)3,011024
C) 3,011023
DГ)6,041024
E)6,121023
F) 6,121013
14$. 112 л газдың зат мөлшері (моль):
А)5
B)9
C)15,5
D)2,4
E)44,8
F)44
15$. 6,021023 молекула газдың (қ.ж.)көлемі:
А) 22,4
B) 2,24
C) 4,48
D) 67,2
E) 53,2
F)11
16$.Сутегі эквивалентінің молярлық көлемі:
А) 11,2
B) 22,4
C)2,24
D) 1,12
E) 67,2
F)18,1
17$.Оттегі эквивалентінің молярлық көлемі:
А) 5,6
B) 22,4
C) 2,24
D) 11,2
E) 67,2
F)61,1
18$.Н2SO4 эквивалентінің молярлық массасы:
А) 49
B) 98
C) 64
D) 12
E) 56
F)81
19$.КОН эквивалентінің молярлық массасы:
А) 56
B) 11,2
C) 44,8
D) 22,4
E) 24
F)21
20$.Н3РО4 : эквиваленттік фактоp
А) 1/3
B) 1
C)4
D)2/3
E)2
F)4,1
21$.Al2(SO4)3-тің эквиваленттік факторы:
А)1/6
B) 0,6
C) 1/3
D)0.5
E)6.3
F)6
22$.Эквиваленттік фактор-бұл қышқылдық-негіздік (алмасу) реакциясында заттың бөлшегінің эквиваленттік үлесінде бір сутегі катионын анықтайтын сан:
A) электрон
B) протон
C) нейтрон
D) позитрон
E) анион
F)-,+
23$. 4NH3 + 5O2 = 4NO + 6H2O химиялық реакциясында заттың химиялық формуласы мен эквиваленттік фактор арасындағы сәйкестікті анықтаңдар
A)
![]()
B)
![]()
C)
![]()
D)
![]()
E)
![]()
F)
![]()
24$. 2H2S + 3O2 = 2SO2 + 2H2O химиялық реакциясында (қ.ж) 1 моль күкіртсутектің эквивалентінің көлемі:
A)11,2 л
B)22,4 л
C)7,47 л
D)5,6 л
E)4,48 л
F)3,73 л
G)2,8 л
F) 2,88 л
25$.Хлор атомының 3р орбиталіндегі электрондар саны :
А)5
B)3
C)2
D)6
E)7
F) 4
26$.Теріс зарядты атомның құрам бөлігі:
А)электрон
B)протон
C)позитрон
D)нейтрон
E) нуклон
F) нуклон,нейтрон
27$.4-периодта s-, p-, d- f- элементтер саны:
А) 2, 6, 10, 0
B) 4, 1, 14, 4
C) 1, 4, 14, 5
D) 2, 4, 6 8
E) 1, 3, 5, 10
F) 2,10,4,8
28$. Атомдағы электронның күйін сипаттайды:
А) 4 квант сандар жиынтығымен;
B) тотығу процесінің көмегімен;
C) Больцман тұрақтысының мәнімен;
D) Клечковский және Паули ережесімен;
E) Термодинамикалық функциялар жиынтығымен.
F) Термодинамикалық функциялары
29$.Электрон табиғаты:
А) Бөлшектік және толқындық қасиеттері;
B) тотықтырғыштық қасиеттері;
C) тотықсыздындырғыштық қасиеттері;
D) диэлектрлік өткізгіштігі;
E) парамагнитті қасиеттері.
F) парамагнитті
30$. Күкірт атомындағы протондар мен нейтрондардың қосындысы:
A) 32
B) 15
C) 6
D) 8
E) 44
F)17
31$.Бір кванттық ұяшықтағы электрондар санын анықтайтын принцип:
A) Паули
B) Гунда
C) Клечковского
D) Менделеева
E) Оствальда
F) Аррениус
32$.Атомдық орбитальдардың әртүрлі деңгейшелерде электрондармен толтыру ретін анықтайтын ереже:
A) Клечковского
B) Ле-Шателье
C) Вант-Гоффа
D) Паули
E) Гунда
F) Аррениус
33$.Бір деңгейше шегінде атомдық орбитальдар электрондардың орналасуын анықайтын ереже:
A) Гунд
B) Вант-Гофф
C) Аррениус
D) Ле-Шателье
E) Паули
F) Клечковского
34$. 4s - деңгейшеден кейін толтырылатын деңгейше:
A) 3d
B) 2d
C) 2p
D) 4p
E) 4d
F) 5d
35$. 6s – деңгейшеден кейін толтырылатын деңгейше:
A) 4f
B) 5d
C) 6p
D) 5f
E) 3d
F) 4d
36$. 1s2 2 s2 2p6 3 s2 3p6 3d54s1 электрондық формуласы мына элемент атомына сәйкес келеді:
A) хром
B) азот
C) көміртек
D) күкірт
E) оттегі
F) хлор
37$.Орбиталді квант саны сипаттайды:
A) атомдық орбиталь пішінін (формасын);
B) электронның өз осі бойынша айналуын;
C) Атомның электрондар беруін;
D) Атомның электрондар қосып алуын;
E) Деңгейдегі электрон энергиясын;
F) деңгейдегі электрон санын;
38$.Спин квант саны сипаттайды:
A) Электронның өз осі бойын айналуын;
B) атомның орбиталь пішінін;
C) деңгейшедегі электрон энергиясын;
D) атомның электрондар беру қабілетін.
E) деңгейдегі электрон энергиясын;
F) деңгейдегі электрон санын;
39$.Бас квант саны сипаттайды:
A) деңгейдегі электрон санын;
B) Атомдық орбитальдің бағытын;
C) электронның өз осінен айналуын;
D) Атомдық орбиталь пішінін;
E) Атомның электрон беру қабілетін.
F) Атомның беру қабілетін.
40$.Орбиталь квант саны мына мәндерді қабылдайды :
A) 0 … (n-1)
B) 0, …
C) +1/2, -1/2
D) -l, 0, + l
E) 0, ½, 1
F)
![]()
41$.Бас квант саны мына мәндерді қабылдайды:
A) 1,2. …
B) 0 … (n-1)
C) +1/2, -1/2
D) -l, 0, + l
E) 0, ½, 1
F) ) -1, ½, 1
42$.Магнит квант саны мына мәндерді қабылдайды:
A) -l, 0, + l
B) 1,2. …
C) 0 … (n-1)
D) +1/2, -1/2
E) 0, ½, 1
F) -1, ½, 1
43$.Иондану энергиясы-бұл:
A) бейтарап атомнан электронды үзуге қажет энергия мөлшері;
B) диссоциациялану үрдісіне қышқыл,негіз,тұз молекуласының қабілеттілігі;
C) Атомның электрон қосып алуында бөлінген энергия мөлшерін ;
D) Атомның электрон беру қабілеттілігі;
E) Атомның электрон қабылдау қабілеттілігі.
F) Атомның қабылдау қабілеттілігі.
21$.Кванттық энергия туралы болжамды алғаш айтқан ғалым:
A) М.Планк
B) Лу де Бройль
C) С.Аррениус
D) Д.И.Менделеев
E) Паули
F) Гунд
G) Клечковский
F) Клечковский, Паули
22$.Луи Де Бройль:
A) микробөлшектің қозғалысы-толқындық үрдіс
B) диссоциация – қайтымды үрдіс
C) квант энергиясы сәулелену жиілігіне тәуелді
D) анықталмағыштық принципін ұсынды
E) атомның ядролық моделін құрды
F) электролизді сандық сипаттады
G) заттың ең басты қасиеті- массасының болуы
F) заттың қасиеті- массасының болуы
23$.Масса- энергия сақталу заңының өрнектелуі:
A)![]()
B)![]()
C)![]()
D)![]()
E)![]()
F)
![]()
24$.М.Планк теңдеуінің өрнектелуі:
A)
B)
C)
D)
E)
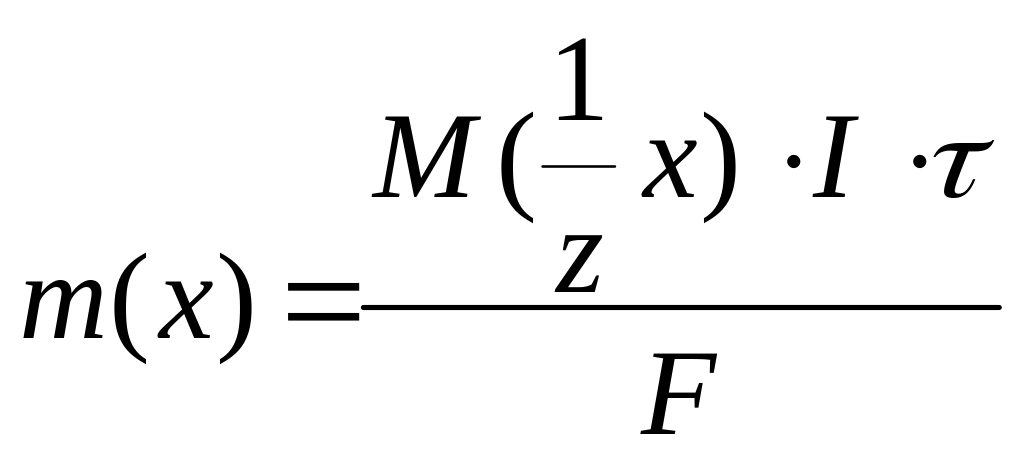
F)![]()
25$.Луи Де Бройль теңдеуінің өрнектелуі:
A)
B)
C)
D)
![]()
E)
F)
26$.В.Гейзенбергтің анықталмағыштық принципі:
A) бір уақытта микробөлшектің орны мен оның қозғалу санын дәл анықтау мүмкін емес
B) атомда барлық квант сандарының жиынтығы бірдей екі электрон бола алмайды
C) кванттық энергия сәулелену жиілігіне тәуелді
D) частице массой m, движущейся со скоростью ν, соответствует волна длиной λ
E) волновая функция называется орбиталью
F) орбиталь можно однозначно описать набором квантовых чисел
27$.Шредингердің толқындық теңдеуі сипатталады:
A) атомның және оның энергиясының берілген орында электронның табылу мүмкіндігі
B) реакция жылдамдығының әрекеттесуші массалар концентрациясына тәуелділігі
C) энергетикалық деңгейдегі электрондар саны
D) бөлшектердің парамагнитті қасиеті
E) атомдық орбитальдардың кеңістіктік бағыты
F) электрондық тығыздықтың радиальді таралуы
28$.К электрондық қабаттың қабаттың максимальді сиымдылығы:
A) 2
B) 16
C) 8
D) 10
E) 24
F)
29$.Максимальная емкость электронного слоя М:
A) 8
B) 18
C) 32
D) 14
E) 10
F) 2
30$.Максимальная емкость электронного слоя L:
A) 18
B) 2
C) 14
D) 10
E) 28
F) 34
31$.Максимальная емкость электронного N:
A) 32
B) 18
C) 8
D) 2
E) 10
F) 3
32$.n = 3, l = 0, m = 0 квант сандарымен сипатталатын орбитальдің пішіні:
A) шар
B) гантель
C) квадрат
D) 4 лепестка
E) шар + гантель
F) квадрат+шар
33$.Үлкен периодтарда d және f элементтердің атомдары радиустарының баяу төмендеуі мынаған байланысты:
A) d- және f- сығылумен
B) сыртқы электрон қабатының толуымен
C) электрон қозғалысының толқындық сипатымен
D) элементтің валенттік күйімен
E) аяқталған қабаттан электронның жойылуымен
F) аяқталған қабаттан жойылуымен
34$.Кіші периодтарда элементтердің атом радиустарының кішіреюі мынаған байланысты :
A) сыртқы электрондық қабаттың толуымен
B) d- және f-сығылуымен
C) электрон қозғалысының толқындық сипатымен
D) элементтің валенттік күйімен
E) аяқталған қабаттан электронның жойылуымен
F) аяқталған қабаттан жойылуымен
35$.Периодтарда атомдық және иондық радиустардың ядро зарядтарының артуы бойынша:
A) төмендейді
B) өседі
C) өзгермейді
D) секірмелі өзгереді
E) бірден өзгереді
F) секіреді
36$.Периодтарда атом радиустарының ең төмендеуі байқалады:
A) кіші периодтар элементтерінде
B) үлкен период элементтерінде
C) d-элементтерінде
D) f-элементтерінде
E) s- , р-, d- және f-элементтерінде бірдей дәрежеде
F) барлық d-элементтер
37$.Электронға ең жақын қасиетке ие:
A) VII топтың р-элементтері
B) II топтың s-элементтері
C) VI топтың f-элементтері
D) d-элементтер
E) III тобының р-элементтері
F) барлық d-элементтер
38$.Иондану энергиясы ең төмен мәнде болатын:
A) I топтың s-элементтері
B) II топтың s-элементтері
C) IV топтың р-элементтері
D) барлық d-элементтер
E) VII топтың р-элементтер
F) VII топтың р/ d элементтер
39$. Электронның өзіне тән электрон қозғалыс мөлшерінің меншікті моменті мына мәндермен анықталады:
A) спин квант сандар
B ) бас квант сандар
С) қосымша квант сандар
D) магнитті квант сандар
E) орбитальді квант сандар
F) орбитальді сандар
40$. l орбитальді квант саны мына мәндерді қабылдауы мүмкін:
A) 0-ден (n - 1) дейін
B) 0-ден шексіздікке дейін
C) 1-ден n дейін
D) 1-ден (n - 1) дейін
E) 1-ден шексіздікке дейін
F) 0-ден n дейін
41$. m магнитті квант саны мына мәндерді қабылдауы мүмкін:
A) -l-ден +l-дейін
B) 0-ден шексіздікке дейін
C) 1-ден n
D) 1-ден (n - 1)-дейін
E) 1-ден шексіздікке дейін
F) 0-ден n дейін
42$.Бас квант саны 6-ға тең электрон қабатындағы электрондардың максималь санын анықтаңдар:
A) 72
B) 36
C) 18
D) 14
E) 10
F) 6
43$.Қосымша квант саны l = 4 болатын электрондық қабаттағы электрондардың максималь саны:
A) 18
B) 32
C) 14
D) 8
E) 10
F) 31
44$. n, l,m квант сандары мына теңдеуді шешу нәтижесінде алынады:
A) Шредингер
B) Гейзенберг
C) Де-Бройль
D) Дирак
E) Ридберг
F) Ридберг/ Дирак
45$. Кестеде n, l, ml және ms электрондардың квант сандары келтірілген
-
Электрон
первый
второй
третий
n
5
5
5
L
2
2
2
ml
0
+1
-1
ms
+1/2
+1/2
+1/2
электрондар күйін анықтаңдар:
A) 5d3
B) 5f3
C) 5p3
D) 2p3
E) 3p3
F) 3p2
46$. 5f, 4s, 7d электрондары мен осы электрондардың 2 бас квант саны мәндерінің арасында сәйкестікті анықтаңдар:
A) 5, 4, 7
B) 4,5, 8
C) 7, 2, 0
D) 3, 4, 7
E) 2, 5, 6
F) 2, 4, 6
47$.Берілген бас квант санды электрондардың максималь саны мен деңгейдегі орбитальдар саны мына формулаға сәйкес анықталады:
A) 2n2 және n-1
B) 2n+1 және 2n2
C) n2 және 2n2
D) n-1 және n2
E) 2n2 және n2
F) 2n2 және n
48$. Қосымша квант саны l = 2 болатын,электрондық қабаттағы электрондардың максималь саны мынаған тең:
A) 10
B) 4
C) 14
D) 6
E) 2
F)3
49$. Ni, Cr, Br, Bа атомдарының қалыпты күйінде жұптаспаған электрондар саны:
A) 2610
B) 3432
C) 5512
D) 6250
1. 4d |
2. 4f |
3. 5p |
4. 6p |
F) 2341
50$.Энергияның арту реті бойынша орналасу реттілігі:
A) 1324
B) 4123
C) 1432
D) 3241
E) 2314
F) 2341
51$. Қосымша квант саны l мәндері мен d, f, p, s электрондық орбитальдардың мәндері арасындағы сәйкестікті анықтаңдар:
A) 2310
B) 1320
C) 3201
D) 0321
E) 2130
F) 2301
52$. Металл атомдарының иондану энергиясының арту ретін анықтаңдар
1- Be, 2- B, 3- Na, 4- Mg:
A) 3412
B) 3214
C) 2134
D) 4123
E) 1234
F) 2341
53$. 1-Be, 2- F, 3- Ca, 4- N элементтері атомдарының электртерістілігінің өсу ретін анықтаңдар:
A) 3142
B) 3214
C) 2134
D) 4123
E) 1234
F) 2341
54$. 1- Азот, 2- Оттегі, 3- Кремний, 4- Фосфор химиялық элементтерін олардың атомдарының электронға жақын қасиетінің төмендеу реті бойынша орналастырыңдар :
A) 2143
B) 3214
C) 2134
D) 4123
E) 1234
F) 2341
55$. Қосылыстарында валенттігі топ нөмірінен артатын химиялық элементтер:
A) мыс,күміс,алтын
B) мырыш,күкірт,сынап
C) мыс,ксенон,осьмий
D) күкірт,платина,темір
E) ксенон, платина, темір
F) платина, темір
56$.Азот молекуласында жұп электрондардың жұп электрондардың жалпы саны:
А) 3
B)2
C)1
D)5
E)4
F) 5,1
57$.Ковалентті полюссіз молекулалар:
А) N2 , O2
B) CO2, SO2
C) CaO, Na2O
D) H2O, NH3
E) CuOH, KOH
F) CuOH, K
58$. s-электрон бұлттарының кеңістіктегі пішіні:
А) шар
B) гантель
C) сызықтық
D) квадрат
E) ромб
F) ромб/кв
59$.р-электрон бұлттарының кеңістіктегі пішіні :
A) гантель
B) шар
C) сызықтық
D) квадрат
E) ромб
F) ромб/кв
60$.Молекуласында бір σ-және екі π-байланысы бар:
A) N2
B) O2
C) H2
D) S2
E) Cl2
61$.Молекуласында төрт σ-байланысы бар:
A) CH4
B) SO3
C) H2O
D) C2H4
E) C2H6
62$.Электртерістілігі ең жоғары элемент:
A) F
B) O
C) N
D) C
E) B
63$. H2SO3 молекуласында байланыстар саны:
A) 6
B) 3
C) 2
D) 4
E) 1
64$.Элемент-хлор байланысының иондану дәрежесі мына қатарда артады:
A) CCl4- BCl3- BeCl2- LiCl
B) BCl3- BeCl2- CCl4- LiCl
C) BeCl2- LiCl- CCl4- BCl3
D) LiCl- CCl4- BCl3- BeCl2
E) LiCl- BeCl2- BCl3- CCl4
65$. Элемент-хлор байланысының иондану дәрежесі мына қатарда артады:
A) BeCl2- MgCl2- CaCl2- BaCl2
B) BaCl2- BeCl2- CaCl2- MgCl2
C) BeCl2- CaCl2- MgCl2- BaCl2
D) MgCl2 - CaCl2- BaCl2- BeCl2
E) BaCl2 - CaCl2- MgCl2- BeCl2
66$.Байланыстың полярлану дәрежесі мына қатарда артады:
A) СH4- NH3- H2O - HF
B) HF - СH4- NH3- H2O
C) NH3- H2O – HF- СH4
D) H2O – HF- СH4- NH3
67$. Екіатомды молекулалардың полярлығы мына ретте артады:
-
1.HI
2.HBr
3.HF
4.HCl
5. Cl2
A) 51243
B) 32145
C) 43521
D) 21345
E)41253
68$.Екіатомды молекулаларда байланыстардың иондық сипатының арту реттілігін анықтаңдар 1- CaCl2, 2- MgCl2, 3- Cl2, 4- HCl, 5- KCl:
A) 34215
B) 32514
C) 52134
D) 45123
E) 12345
E) HF - H2O- NH3- СH4
69$.Қатардағы диамагнитті бөлшектер:
A)
![]()
B)
![]()
C)
![]()
D)
![]()
E)
![]()
70$.Қатардағы парамагнитті бөлшектер:
A)![]()
B)
C)
D)
E)
![]()
F)
71$. Ең берік молекулааралық сутектік байланысы бар заттар:
A) HF
B) HCl
C) HBr
D) NH3
E) Н2О
72$.1-С6Н6, 2-С2Н2, 3-С2Н4, 4-С2Н6 көмірсутектерінде көміртек-көміртек байланыстарының ұзындығының артуы реттілігін анықтаңдар:
A) 2314
B) 3214
C) 2134
D) 4123
E) 1234
73$. 1-H2S, 2-H2O, 3-H2Te, 4-H2Se көмірсутектерінде көміртек-көміртек байланыстарының ұзындығының артуы реттілігін анықтаңдар:
A) 3412
B) 3214
C) 2134
D) 4123
E) 1234
74$. А және В атомдары арасында ковалентті полюссіз байланыс атомдардың электртерістілігінің келесі қатысында түзіледі:
A) ЭО(A) = ЭО(В)
B) ЭО(A) < ЭО(В)
C) ЭО(A) > ЭО(В)
D) ЭО(A) << ЭО(В)
E) ЭО(A) >> ЭО(В)
F) атомдардың кез келген электртерістілігі қатынасында
75$. Химиялық донорлы-акцепторлы байланыс келесі нәтижесінде түзіледі:
A) Бір атомның электрон жұптарын басқа атомның бас орбитасына беруі
B) Әртүрлі атомдардың электрондық орбитальдарының бүркесуі
C) бір және сол атомның электрон бұлттарының бүркесуі
D) Атомдардан біреуінен электрон бұлттарының толық және жартылай ығысуы
E) Бір атомның электрондарын басқа атомның бос орбитальдарына беруі
76$. Na3[AlF6] молекуласында донорлы-акцепторлы байланыстар саны:
A) 3
B) 2
C) 5
D) 4
E) 6
77$. H5IO6 молекуласындағы гибридтену типі:
A) sp3d2-гибридтену
B) sd3-гибридтену
C) sp3d2f-гибридтену
D) sp2d-гибридтену
E) sp3d-гибридтену
F) sp2d2-гибридтену
78$. (ВС) байланыс әдісіне сәйкес химиялық элементтің қалыпты (қозбаған күйінде) валенттігі тең:
A) сыртқы қабаттағы электрондар санына
B) топ нөміріне
C) жұптаспаған электрондар санына
D) бос электрондық орбитальдар санына
E) период нөміріне
79$. ZnO-ін KOH-мен балқытқанда түзілген тұздың массасы мынаған тең:
А)175
B)202
C)88
D)64
E)138
80$. 2HgО2Hg+O2
Келтірілген реакцияның типін көрсетіңіз
А)айырылу
B)қопарылу
C)қосылу
D)орынбасу
E)алмасу
81$.Zn + 2HCl = ZnCl2 + H2 келтірілген реакцияның типін көрсетіңіз
А)орынбасу
B)қосылу
C) ыдырау
D)алмасу
E)тізбекті
82$.Келтірілген реакцияның типін көрсетіңіз 2Zn+O22ZnO
А)қосылу
B)айырылу
C)алмасу
D)орынбасу
E)тізбекті
83$.Негіздік оксидтер қатарын көрсетіңіз:
А)CaO, MgO, Na2O
B)SiO2, CO2, P2O5
C)ZnO, Al2O3, BeO
D)Fe2O3, MnO2, N2O5
E)Cr2O3, CO2, ZnO
84$.Қышқылдық оксидтер қатарын көрсет
А)SiO2,Mn2O7,CrO3
B)Na2SO4, CuO, HCl
C)K2O, MgSO4,Cr2O3
D)Al2O3 , Na2O, NaCl
E)ZnO, BeO, Fe2O3
85$.Қышқыл тұзды көрсет:
А)Na HSO3
B)Na2SO4
C)CuCl2
D)AlOHSO4
E)Fe(OH)3
86$.Негіз тұзды көрсет:
А)(MgOH)2 SO4
B)K2HPO4
C)CuO
D)Fe2O3
E)H2S
87$.Суда еритін негізді көрсет:
А)Са(OH)2
B)Al(OH)3
C)Zn(OH)2
D)Cr(OH)3
E)Be(OH)2
88$.Суда еритін оксидті көрсет:
А)Na2O
B)ZnO
C)BeO
D)MnO2
E)Cr2O3
89$. 68,4% хром және 31,6% оттегі құрамды хром оксидін көрсет:
А)Cr2O3
B)CrO3
C)CrO
D)Cr2O4
E)Cr2O7
90$. 20г қышқыл тұз алу үшін NaOH ерітіндісі арқылы өткізуге қажетті SO2 -нің көлемі:
A) 4,3л
B) 2,24л
C) 11,2л
D) 4,48л
E) 67,2л
91$. 25г орта тұз алу үшін, NaOH ерітіндісі арқылы өткізуге қажетті SO2 –нің көлемі:
A) 4,44
B) 2,38
C) 67,2
D) 34,8
E) 10,1
92$. Төменде келтілрілген қосылыстардың ішінде ең күшті негіз :
A) Ba(OH)2
B) Be(OH)2
C) Mg(OH)2
D) Ca(OH)2
93$.Төменде келтірілген қосылыстардың ішінде ең әлсіз қышқыл:
A) H2TeO3
B) H2SO3
C) H2SeO3
D) H2SO4
E) HNO3
94$.Ең берік сутектік қосылыстың химиялық формуласы:
A) NH3
B) AsH3
C) SbH3
D) PH3
E) HNO3
95$.1- Mg(OH)2,
2- Al(OH)3, 3- KOH, 4- Ca(OH)2 қатарында негіз күшінің арту реттілігін анықтаңдар:
A) 2143
B) 3214
C) 2134
D) 4123
E) 1234
96$. Марганец оксидтерінің негіздік қасиетінің арту реттілігін анықтаңдар
1- MnO2, 2- Mn2O7, 3- MnO, 4- MnO3:
A) 2413
B) 3214
C) 2134
D) 4123
E) 1234
97$.1- HClO, 2- HBrO, 3- HIO, 4- HClO2 қышқылдық күшінің арту реттілігін анықтаңдар:
A) 3214
B) 2413
C) 2134
D) 4123
E) 1234
98$. Бір лиганд алатын координациялық орын саны былай аталады:
A)дентанттылық
B)валенттілік
C)координациялық сан
D)координациялық сфера
E) изомерия
99$. Кешеннің геометриялық формасы-сызықтық,гибридтену түрі:
A)sp
B)sp3d2
C)sp2d
D)sp3
E)sp2
100$. Кешеннің геометриялық формасы-октоэдр,гибридтену түрі:
A)sp3d2
B)sp2d
C)sp3
D)sp
E)sp2
