
- •Магсумов тимур ильнурович
- •Зависимости термодинамических функций сольватации неполярных соединений от состава водно-органических смесей
- •Содержание
- •Введение
- •1. Литературный обзор
- •1.1. Термодинамические функции растворения и сольватации
- •1.1.1. Энергия Гиббса растворения и сольватации
- •1.1.2. Энтальпия растворения и сольватации
- •1.2. Соотношения между энергией Гиббса и энтальпией сольватации. Сольвофобные эффекты
- •1.3. Литературные данные по энергиям Гиббса растворения/сольватации в водно-органических смесях
- •1.4. Литературные данные по энтальпиям растворения в водно-органических смесях
- •1.5. Методы расчета термодинамических функций растворения в смешанных растворителях
- •1.5.1. Методы расчета термодинамических функций сольватации в водно-органических смесях
- •1.5.2. Расчет термодинамических функций сольватации методами компьютерного моделирования
- •Постановка задачи
- •2. Экспериментальная часть
- •2.1 Реактивы
- •2.2. Измерение коэффициентов активности при предельном разбавлении
- •2.3. Измерение энтальпий растворения
- •3. Результаты и обсуждение
- •3.2. Сольватация бензола в водно-органических смесях
- •3.3. Молекулярно-динамическое моделирование сольватации в водно-органических смесях
- •Основные результаты и выводы
- •Список использованной литературы
1.4. Литературные данные по энтальпиям растворения в водно-органических смесях
Изучение энтальпий растворения в водно-органических смесях велось достаточно интенсивно. Исследование зависимости энтальпии растворения от состава смеси, как правило, проводилось для полярных соединений, таких как спирты, фенол [34], ацетонитрил [35], аминокислоты [36], дипептиды [37], краун-эфиры [38], анилин [39, 40].
 Калориметрические
исследования растворения неполярных
и малополярных веществ практически не
проводились из-за их низкой растворимости
в смесях с большим содержанием воды. В
работах Батова и сотр. определены
энтальпии растворения бензола в смесях
воды с апротонными растворителями –
диметилсульфоксидом, ацетоном,
1,4-диоксаном [41]. Авторами отмечено
наличие эндотермического максимума
при содержании органического сорастворителя
около 10-20% по молям (рис. 4), который они
связывают со “структурной стабилизацией”
раствора. Высота и положение максимума
определяются природой органического
сорастворителя. При увеличении в его
молекуле числа гидрофобных групп, таких
как CH3 и CH2,
как правило, увеличивается высота
максимума и происходит его смещение в
область с большим содержанием воды.
Калориметрические
исследования растворения неполярных
и малополярных веществ практически не
проводились из-за их низкой растворимости
в смесях с большим содержанием воды. В
работах Батова и сотр. определены
энтальпии растворения бензола в смесях
воды с апротонными растворителями –
диметилсульфоксидом, ацетоном,
1,4-диоксаном [41]. Авторами отмечено
наличие эндотермического максимума
при содержании органического сорастворителя
около 10-20% по молям (рис. 4), который они
связывают со “структурной стабилизацией”
раствора. Высота и положение максимума
определяются природой органического
сорастворителя. При увеличении в его
молекуле числа гидрофобных групп, таких
как CH3 и CH2,
как правило, увеличивается высота
максимума и происходит его смещение в
область с большим содержанием воды.
В работах [42, 43] получены значения энтальпий растворения н-алканов в смесях апротонный растворитель–вода с минимальной мольной долей органического сорастворителя в растворе 0.4, что не позволяет делать обоснованных выводов. Расчеты, проведенные Батовым [44], предсказывают наличие максимума при мольной доле органического сорастворителя 0.2-0.3.
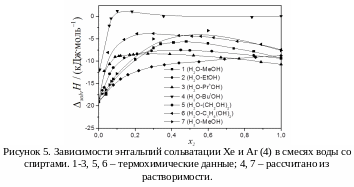 В
работах [45–47] изучались энтальпии
растворения алканов, а также благородных
газов (как прямым калориметрическим
методом, так и по зависимости растворимости
от температуры) в смесях воды с различными
спиртами. Для ксенона и аргона в смесях
воды с метанолом, этанолом, пропанолом,
пропиленгликолем и трет-бутанолом
наблюдается максимум в диапазоне
концентраций спирта от 0.1 до 0.6 мольных
долей (рис. 5). При растворении ксенона
в смеси воды с этиленгликолем максимума
не наблюдается, а происходит плавное
нелинейное уменьшение энтальпии
сольватации при увеличении доли воды
в смеси. Для алканов данные по энтальпиям
растворения в тех областях концентраций
органического сорастворителя, где мог
бы находится максимум по аналогии с
инертными газами, отсутствуют.
В
работах [45–47] изучались энтальпии
растворения алканов, а также благородных
газов (как прямым калориметрическим
методом, так и по зависимости растворимости
от температуры) в смесях воды с различными
спиртами. Для ксенона и аргона в смесях
воды с метанолом, этанолом, пропанолом,
пропиленгликолем и трет-бутанолом
наблюдается максимум в диапазоне
концентраций спирта от 0.1 до 0.6 мольных
долей (рис. 5). При растворении ксенона
в смеси воды с этиленгликолем максимума
не наблюдается, а происходит плавное
нелинейное уменьшение энтальпии
сольватации при увеличении доли воды
в смеси. Для алканов данные по энтальпиям
растворения в тех областях концентраций
органического сорастворителя, где мог
бы находится максимум по аналогии с
инертными газами, отсутствуют.
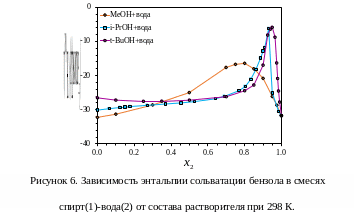 В
работах [48–50] получены данные калориметрии
растворения бензола в смесях воды с
метанолом, изопропанолом и трет-бутанолом.
С увеличением длины гидрофобного
углеводородного радикала максимум
зависимости энтальпии от состава смеси
смещается в область более низких
концентраций органического сорастворителя,
а максимальное значение энтальпии
растет (рис. 6).
В
работах [48–50] получены данные калориметрии
растворения бензола в смесях воды с
метанолом, изопропанолом и трет-бутанолом.
С увеличением длины гидрофобного
углеводородного радикала максимум
зависимости энтальпии от состава смеси
смещается в область более низких
концентраций органического сорастворителя,
а максимальное значение энтальпии
растет (рис. 6).
Энтальпия растворения в водно-органических смесях некоторых лекарственных веществ определена по температурной зависимости растворимости [27, 51–55]. Недостатком метода является низкая точность, что нужно учитывать при интерпретации результатов. Вид зависимости энтальпии растворения от состава смеси зависит от количества гидрофобных и гидрофильных групп, а также от структуры молекулы органического сорастворителя. Для некоторых полярных соединений также наблюдается максимум в смесях, обогащенных водой [27, 52–54, 56, 57] (рис. 7).
