
- •1. Химическая технология
- •Вторичные;
- •Энергетические;
- •2. Физико-химические основы химико-технологических процессов
- •2.1. Стехиометрия химических превращений
- •2.2. Термодинамика химических превращений
- •2.3. Кинетика химических превращений
- •3. Химический процесс
- •3.1. Гетерогенный химический процесс
- •3.2. Каталитический процесс
- •4. Химический реактор
- •4.1. Общие положения
- •4.2. Математическая модель процесса в реакторе
- •4.3. Процесс в реакторе
- •4.4. Выбор реактора
- •6. Химические производства
- •6.1. Производство серной кислоты
- •6.2. Производство аммиака
- •6.3. Производство азотной кислоты
2.3. Кинетика химических превращений
2.3.1. Что такое скорость химического превращения?
-
изменение концентрации во времени;
-
изменение количества вещества во времени;
-
изменение во времени количества вещества в единице объема;
-
соотношение количества образовавшихся продуктов и количества исходных веществ.
2.3.2. Различаются ли понятия "скорость химической реакции" и "скорость химического превращения вещества" и почему"?
-
нет, так как оба понятия определяют одно и то же – как быстро протекает превращение;
-
нет, так как скоростью превращения вещества измеряют скорость реакции;
-
да, так как значения скорости превращения вещества различны для разных участников реакции, а скорость реакции не может быть многозначной.
2.3.3. Сопоставьте тип реакции и вид зависимости ее скорости от температуры:
A)
простая обратимая экзотермическая
реакция;
Б)
простая необратимая экзотермическая
реакция;
В)
простая обратимая эндотермическая
реакция.


1

2
 3
3
ОТВЕТ: 1-Б, 2-В, 3-А
2.3.4. Каким уравнением характеризуют зависимость константы скорости реакции k от температуры T?
1)
 ;
2)
;
2)
 ;
3)
;
3)
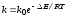 ;
4)
;
4)

2.3.5. Какая существует зависимость скорости необратимой реакции от температуры?
-
прямая зависимость;
-
обратная зависимость;
-
экспоненциальная зависимость;
-
экстремальная зависимость.
2.3.6. На графике приведены зависимости скорости простых необратимых реакций от температуры с разными энергиями активации Е1 и Е2. Какое соотношение между Е1 и Е2?
Е1
> Е2; Е1
< Е2; Е1
Е2.

ОТВЕТ: 1
2.3.7. Сопоставьте порядок простой необратимой реакции n и вид зависимости ее скорости от концентрации c:


А) n = 0;
Б) n = 1;
В) n > 1;
Г) n < 1.
1

2
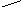
3

4
ОТВЕТ: 1-В, 2-Б, 3-А, 4-Г
2.3.8. Сопоставьте порядок простой необратимой реакции n и вид зависимости ее скорости r от степени превращения х исходного вещества
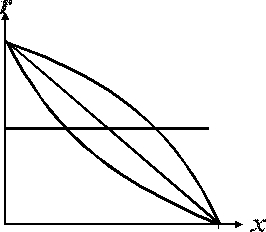

А) n = 0;
Б) n = 1;
В) n > 1;
Г) n < 1.
1

2

3

4
2.3.9.
Сопоставьте
вид сложной реакции и вид зависимости
дифференциальной избирательности от
степени превращения исходного вещества
(глубины протекания реакции)

А) последовательная реакция;
Б) параллельная реакция, n1 > n2 (n1, n2 – порядки целевой и побочной реакций);
В) параллельная реакция, n1 < n2;
Г) параллельная реакция, n1 = n2.
1

2

3

4
 2.3.10.
Как меняется дифференциальная
селективность SR
для параллель-
n1
R
2.3.10.
Как меняется дифференциальная
селективность SR
для параллель-
n1
R
 ной
реакции А
с
увеличением концентрации исходного
вещества А,
n2
S
ной
реакции А
с
увеличением концентрации исходного
вещества А,
n2
S
если n1 > n2?
-
увеличивается;
-
уменьшается;
-
не меняется.
 2.3.11.
Как меняется дифференциальная
селективность SR
для параллель-
n1
R
2.3.11.
Как меняется дифференциальная
селективность SR
для параллель-
n1
R
 ной
реакции А
с
увеличением степени превращения
исходного
n2
S
ной
реакции А
с
увеличением степени превращения
исходного
n2
S
вещества А, если n1 > n2?
-
увеличивается;
-
уменьшается;
-
не меняется.
3. Химический процесс
3.1. Гетерогенный химический процесс
3.1.1. Какие факторы действуют на положение равновесия гетерогенных процессов "газ – твердое"?
-
температура;
-
радиус пор;
-
давление;
-
размер зерна;
-
концентрация реагентов.
3.1.2. Какие из предложенных графиков характеризуют распределение концентрации газообразного реагента A вокруг и внутри твердой частицы для гетерогенного процесса "газ – твердое", протекающего в кинетической области? 4

3.1.3. Какие из представленных графиков отображают распределение концентрации газообразного реагента A вокруг и внутри твердой частицы для гетерогенного процесса "газ – твердое", протекающего во внутридиффузионной области? 2
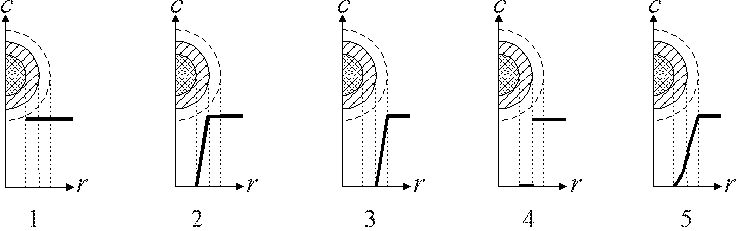
3.1.4. Каким будет распределение концентрации газообразного реагента в ходе реакции, если лимитирующей стадией является внешняя диффузия? 1

3.1.5. Какие из предложенных зависимостей используются как математическое описание гетерогенного процесса "газ – твердое", протекающего во внешнедиффузионной области?
1)
 ;
2)
;
2)
 ;
3)
;
3)
 ;
;
4)
 ;
5)
;
5)
 ;
6)
;
6)
 .
.
3.1.6. Укажите, в чем практический смысл определения лимитирующей стадии гетерогенного процесса?
1) знание лимитирующей стадии позволяет ранжировать технологические мероприятия по степени их воздействия на процесс;
2) практического смысла не имеет, так как для эффективной реализации неисследованного процесса достаточно осуществить предварительное дробление твердых частиц, установить максимальный расход газа и предельно допустимую (по технологическим соображениям) температуру;
3) если известен основной фактор торможения процесса, возможно, оценить экономическую целесообразность его устранения за счет изменения регламента на предыдущих стадиях технологического цикла;
4) практического смысла не имеет, т.к. экономически не целесообразно;
5) определение лимитирующей стадии позволяет оптимизировать энергетические затраты на эффективное проведение гетерогенного процесса.
3.1.7. Какие технологические параметры являются определяющими при интенсификации гетерогенного процесса окисления сульфида цинка?
-
температура, если процесс протекает во внешнедиффузионной области;
-
температура, если процесс протекает в кинетической области;
-
температура при любой области протекания процесса;
-
концентрация кислорода только для кинетической области;
-
концентрация кислорода для любой области;
-
уменьшение размера частиц для любой области;
-
уменьшение размера только для внешнедиффузионной области;
-
увеличение скорости газового потока для кинетической области;
-
увеличение скорости газового потока для внешнедиффузионной области.
3.1.8. Какая стадия гетерогенного процесса может быть лимитирующей при обжиге сульфида цинка?
-
проникновение газового реагента через пограничную газовую пленку, если процесс ускоряется при повышении скорости газового потока;
-
то же, если процесс ускоряется с ростом температуры;
-
то же, если скорость процесса слабо зависит от температуры;
-
химическая реакция, если скорость процесса резко увеличивается с ростом температуры;
-
химическая реакция, если скорость процесса увеличивается при повышении скорости газового потока;
-
проникновение газового реагента внутрь зерна, если скорость процесса резко увеличивается при измельчении твердых частиц;
-
проникновение газового реагента внутрь зерна, если скорость процесса увеличивается при повышении температуры.
3.1.9. В какой области осуществляется гетерогенный процесс, если повышение температуры приводит к значительному возрастанию скорости процесса?
-
в переходной;
-
во внутридиффузионной;
-
во внешнедиффузионной;
-
в кинетической;
-
влияние температуры на скорость процесса не характеризует область его протекания.
3.1.10.
По результатам эксперимента получена
линейная зависимость в координатах

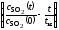 .
Можно ли сказать, в какой области
протекает процесс?
.
Можно ли сказать, в какой области
протекает процесс?
-
да – кинетическая область;
-
да – внешнедиффузионная область;
-
да – внутридиффузионная область;
-
да – переходная область.
-
нельзя сказать по полученной зависимости, какая область лимитирует;
3.1.11. Получена линейная зависимость хтв(t/tк). Можно ли судить по ней об области протекания процесса?
-
нельзя судить об области протекания процесса;
-
процесс идет во внешнедиффузионной области;
-
процесс идет во внутридиффузионной области;
-
процесс идет в кинетической области;
-
линейная зависимость не может иметь место.
3.1.12. Зависит ли скорость окисления ZnS от скорости подачи газового потока?
-
да, если процесс протекает в кинетической области;
-
нет, если процесс протекает в кинетической области;
-
да, если процесс протекает во внешнедиффузионной области;
-
нет, если процесс протекает во внешнедиффузионной области;
-
да, если процесс протекает во внутридиффузионной области.
3.1.13. Влияет ли повышение скорости газового потока на изменение концентрации газового реагента у поверхности частицы?
-
да, если лимитирующая стадия является стадией химического превращения;
-
да, если процесс идет в области внутренней диффузии;
-
да, если твердая частица имеет высокую пористость;
-
да, если при этом процесс переходит из внешнедиффузионной области во внутридиффузионную;
-
нет, если температура процесса высокая.
3.1.14. Какие преимущества имеет аппарат кипящего слоя при проведении гетерогенного процесса "газ-твердое"?
-
снимает внутридиффузионное торможение;
-
увеличивает скорость внешней диффузии;
-
увеличивает поверхность контакта фаз;
-
дает возможность повысить давление;
-
позволяет получать более чистый продукт;
-
позволяет снизить температуру процесса.
Выбрать сочетание правильных ответов:
1) 1, 2, 3; 2) 2, 3, 4, 6; 3) 2, 3; 4) 1, 3; 5) 3, 5; 6) 2, 4, 6;
3.1.15. Какое экспертное суждение справедливо для аппаратов кипящего слоя?
1) аппарат реализует режим идеального смешения твердой фазы и режим идеального вытеснения в газовой фазе;
2) имеет существенный недостаток: усиленное истирание твердых частиц, что требует дополнительных затрат на пылеочистку;
3) имеет существенное достоинство: усиленное истирание твердых частиц способствует увеличению скорости гетерогенного процесса;
4) режим кипящего слоя обладает гидродинамической неустойчивостью, что сужает область его применения;
5) аппарат кипящего слоя обеспечивает развитую поверхность межфазового взаимодействия.
3.1.16. Назовите способы ускорения окисления сульфида цинка при высоких температурах?
-
повышение концентрации исходных веществ;
-
увеличение температуры;
-
снижение давления;
-
увеличение расхода воздуха;
-
дробление твердых частиц.
3.1.17. Какие из приведенных положений справедливы для окисления сульфида цинка, если процесс лимитируется внешней диффузией?
-
повышение скорости газового потока не влияет на скорость процесса;
-
повышение скорости газового потока значительно ускоряет скорость процесса;
-
повышение температуры интенсифицирует процесс;
-
измельчение твердого реагента незначительно интенсифицирует процесс;
-
повышение температуры не влияет на скорость процесса;
-
повышение концентрации газового реагента ускоряет процесс;
-
изменение концентрации газового реагента не влияет на скорость процесса.
3.1.18. Окисление ZnS протекает в кинетической области. Изменением каких параметров можно интенсифицировать процесс?
-
уменьшением радиуса частиц;
-
снижением концентрации кислорода;
-
увеличением концентрации кислорода;
-
повышением температуры;
-
увеличением скорости газового потока.
3.1.19. Какие факторы могут влиять (в общем случае) на скорость окисления сульфида цинка?
-
давление;
-
скорость подачи реагентов;
-
поверхность контакта фаз;
-
движущая сила процесса;
-
применение катализатора;
-
температура;
-
концентрация кислорода в газе.
Выбрать сочетание правильных ответов:
1) 1, 3, 4, 7; 2) 3, 6, 7; 3) 1, 2, 3, 4, 6, 7; 4) 2, 4, 5, 6; 5) 1, 3, 4, 7.
3.1.20. Какой фактор интенсификации является наиболее эффективным при протекании гетерогенного процесса "газ-твердое" во внутридиффузионной области?
-
использование катализатора;
-
уменьшение пористости твердой частицы;
-
турбулизация газового потока;
-
измельчение твердой фазы;
-
увеличение температуры процесса;
-
повышение давления;
-
изменение соотношения концентраций реагирующих компонентов.
3.1.21. Перечислите факторы, влияющие на скорость гетерогенного процесса "газ-твердое", протекающего в кинетической области?
-
увеличение температуры;
-
уменьшение размера частиц;
-
увеличение концентрации газообразного потока;
-
увеличение скорости газообразного потока;
-
применение катализатора.
3.1.22. Какой способ интенсификации гетерогенного процесса "газ-твердое" является наиболее характерным для внешнедиффузионной области его протекания?
-
снижение температуры;
-
уменьшение размера частиц;
-
увеличение поверхности реагирующих компонентов;
-
увеличение концентрации компонента в газовой фазе;
-
увеличение скорости газового потока;
-
механическое перемешивание твердой фазы.
3.1.23. Назовите способы интенсификации гетерогенного процесса "газ-твердое", протекающего во внутридиффузионной области?
-
увеличение концентрации реагента в газовой фазе;
-
увеличение пористости частиц твердой фазы;
-
измельчение частиц твердой фазы;
-
уменьшение скорости газового потока;
-
снижение температуры процесса;
-
увеличение температуры процесса.
3.1.24. Установите область протекания процесса, если частицы сульфида цинка диаметром 4 мм выгорают полностью за 1200 с, а частицы диаметром 2 мм – за 300 с.
-
кинетическая;
-
внутридиффузионная;
-
внешнедиффузионная;
-
переходная от кинетической к внутридиффузионной.
3.1.25. Расположите в ряд режимы по возрастанию влияния степени измельчения твердой фазы на уменьшение времени полного превращения:
-
внутридиффузионный кинетический внешнедиффузионный;
-
внутридиффузионный внешнедиффузионный кинетический;
-
кинетический внутридиффузионный внешнедиффузионный;
-
внешнедиффузионный кинетический внутридиффузионный;
-
кинетический и внешнедиффузионный (влияние измельчения примерно равноценно) внутридиффузионный.
-
влияние измельчения примерно равноценно для всех рижимов протекания процесса.
3.1.26. Какие аппараты обеспечивают наибольшую интенсивность при проведении гетерогенного процесса "газ-твердое", протекающего во внутридиффузионной области?
-
полочные;
-
трубчатые;
-
кипящего слоя;
-
пылевидного обжига;
-
с движущимся слоем.
Выбрать сочетание правильных ответов:
1) 1, 2, 4; 2) 1, 3, 5; 3) 3, 4; 4) 1, 3; 5) 4, 5.
3.1.27. Для интенсификации стадии внутренней диффузии в процессе обжига серного колчедана его частицы надо:
-
измельчить;
-
укрупнить;
-
раздробить;
-
агломерировать.
3.1.28. По какой формуле рассчитывается коэффициент массообмена между газом и жидкостью (г, ж – коэффициенты массообмена со стороны газа и жидкости, соответственно)?
1) = г + ж; 2) = (1/г + 1/ж)1;
3) = (Кабс/г + 1/ж)1 3) = г/Кабс + ж;
3.1.29. Гетерогенный процесс Aг + Вж = Rж протекает в кинетической области. Чему равна концентрация компонента А в жидкости?
-
близка к нулю;
-
концентрации компонента А в газовой фазе;
-
концентрации насыщения жидкости компонентом А;
-
концентрации компонентов А и В в жидкости отвечает стехиометрии реакции.
3.1.30. Гетерогенный процесс Aг + Вж = Rж протекает в диффузионной области. Чему равна концентрация компонента А в жидкости?
-
близка к нулю;
-
концентрации А в газовой фазе;
-
концентрации насыщения жидкости компонентом А;
-
концентрации компонентов А и В в жидкости отвечает стехиометрии реакции.
3.1.31. Какие способы интенсификации гетерогенного процесса "газ-жидкость" можно предложить?
-
в барботажный слой вводить газ мелкими пузырьками;
-
увеличить высоту барботажного слоя;
-
перейти от барботажного аппарата к насадочному;
-
использовать насадочный аппарат с самыми мелкими элементами.
3.1.32. Расположите указанные типы реакторов для процесса "газ-жидкость" в порядке возрастания интенсивности процесса в них:
-
барботажный реактор;
-
реактор с орошаемой насадкой и противоточным движением фаз;
-
реактор с распылом жидкости через эжектор.
-
трубчатый реактор со скоростным прямоточным движением фаз. 1 2 4 3
