
- •2. Механизм действия тиреоидных гормонов.
- •2. Гормоны кальциевого обмена
- •Кальцитриол
- •Регуляция синтеза и секреции
- •Механизм действия
- •1. Ферменты
- •5. Регуляция действия ферментов
- •Ингибиторы ферментов
- •Гипервитаминоз
- •Гиповитаминоз
- •Гипервитаминоз
- •Вит.К(филлохинон)
- •Переизбыток
- •Вит. F( арахидоновая, линолевая, линоленовая к-ты)
- •Окислительное декарбоксилирование пировиноградной кислоты
- •Цитратный цикл
- •14 Разобщители тканевого дыхания (динитроортокрезол)
- •Всасывание углеводов
- •Нарушение переваривания и всасывания углеводов
- •18. Биологическая роль, синтез и распад гликогена. Особенности распада гликогена в печени и скелетных мышцах.
- •31. Мобилизация липидов из жировых депо
- •37. Синтез и использование кетоновых тел. Понятие и причины кетонемии и кетонурии.
- •38. Липопротеины сыворотки крови: биологическая роль, особенности состава и разновидности. Понятие атерогенных и антиатерогенных липопротеинов.
- •39. Нарушения липидного обмена:
- •Симптомы заболевания
- •40. Понятие и разновидности азотистого баланса.
- •41. Особенности переваривания белков. Нормальные и патологические компоненты желудочного сока.
- •42. Гниение белков в толстом кишечнике.
- •43. Реакции дезаминирования аминокислот и их биологическая роль.
- •44. Трансаминирование аминокислот: биологическая роль реакций, использование в диагностике.Глюкозо-аланиновый цикл.
- •45. Декарбоксилирование аминокислот. Образование и биологическая роль биогенных аминов: гамма-аминомасляной кислоты (гамк), гистамина, серотонина, дофамина. Инактивация биогенных аминов.
- •46. Использование безазотистых остатков аминокислот: понятие, биологическая роль и примерыгликогенных и кетогенных аминокислот.
- •47. Источники образования аммиака в организме. Причины токсичности аммиака. Понятие гипераммониемии.
- •Причины токсичности аммиака
- •48. Пути обезвреживания аммиака и их особенности в почках, печени, нервной ткани.
- •51. Биологическая роль и биосинтез креатина.
- •52. Энзимопатии аминокислотного обмена (метаболические блоки и клинические проявления) :
- •II. Синтез пуриновых нуклеотидов
- •56. Синтез пиримидиновых нуклеотидов dе novo его регуляция
- •58. Ингибиторы синтеза тимидиловых нуклеотидов
- •Секреция
- •Механизм
- •77. Медицинские показания и правило проведения теста «сахарной нагрузки» (теста толерантности к глюкозе).
- •78. Адреналин - гормон мозгового вещества надпочечников: схема синтеза и названия ферментов. Механизм действия адреналина и его влияние на обмен веществ.
- •Аденилатциклазный механизм
- •Кальций-фосфолипидный механизм
- •79. Гормоны коры надпочечников: классификация по химической структуре, схема основных этапов синтеза из холестерола, механизм действия.
- •1. Биосинтез йодтиронинов
- •2. Регуляция синтеза и секреции йодтиронинов
- •3. Механизм действия и биологические
- •4. Заболевания щитовидной железы
- •85. Биохимические характеристики гипо- и гиперфункции щитовидной железы.
- •86. Паратгормон: структура, механизм действия и роль в метаболизме кальция и фосфатов.
- •87. Кальцитонин: структура, механизм действия и роль в метаболизме кальция и фосфатов.
- •88. Кальцитриол: структура, этапы синтеза, механизм действия и роль в метаболизме кальция и фосфатов. Рахит.
- •90. Эйкозаноиды:классификация, этапы бисинтеза, примеры соединений. Биологические эффекты эйкозаноидов. Механизм действия нестероидных противовоспалительных препаратов на примере аспирина.
- •94. Ферменты сыворотки крови: их происхождение и значение для диагностики заболеваний.
- •95. Буферные системы крови. Нарушения кислотно-щелочного равновесия крови.
- •109. Изменения в соединительной ткани при старении, коллагенозах, мукополисахаридозах. Роль соединительной ткани в заживлении ран
- •Ситуационные задачи по биохимии для студентов лечебного факультета
- •Эталон ответа
- •Эталон ответа
- •Эталон ответа
- •Задача №42
- •Эталон ответа
- •Задача №43
- •Эталон ответа
- •Задача №44
- •Эталон ответа
- •Задача №45
- •Эталон ответа
- •Ситуационные задачи по биохимии для студентов лечебного факультета
- •Эталон ответа
- •Эталон ответа
- •Эталон ответа
- •Задача №42
- •Эталон ответа
- •Задача №43
- •Эталон ответа
- •Задача №44
- •Эталон ответа
- •Задача №45
- •Эталон ответа
48. Пути обезвреживания аммиака и их особенности в почках, печени, нервной ткани.
В
тканях аммиак находится преимущественно
в виде иона аммония NН![]() в
равновесии с небольшой концентрацией
неионизированного аммиака.
в
равновесии с небольшой концентрацией
неионизированного аммиака.
1. Восстановительное аминирование.
Одним из путей связывания и обезвреживания аммиака в организме, в частности в мозге, сетчатке, почках, печени и мышцах - это биосинтез амидов глутаминовой и аспарагиновой кислот (глутамина или аспарагина):
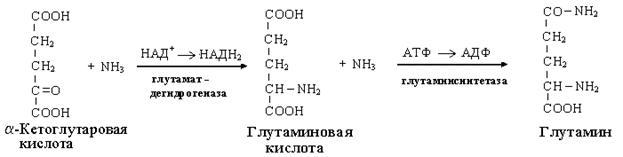
Эта реакция протекает во многих тканях, но наиболее важна для нервной, особенно чувствительной к токсическому действию аммиака. Первая реакция представляет собой обращение глутаматдегидрогеназной реакции (обратная окислительному дезаминированию ГЛУ).
Обезвреживание аммиака путем синтеза глутамина имеет и анаболическое значение, поскольку глутамин используется для синтеза ряда соединений. Прежде всего нужно отметить, что глутамин — одна из 20 аминокислот, входящих в белки. Кроме того, амидная группа глутамина используется для синтеза аспарагина, глюкозамина и других аминосахаров, пуриновых и пиримидиновых нуклеотидов. Таким образом, в этих реакциях азот аммиака включается в разнообразные структурно-функциональные компоненты клетки.
Глутамин затем может поступать во все ткани, где осуществляется его гидролиз при участии глутаминазы:
![]()
Подобным образом происходит образование аспарагина (через ЩУК).
2. Образование аммонийных солей.
Экскреция аммиака с мочой в норме невелика — около 0,5 г в сутки. Но она в несколько раз повышается при ацидозе, т. е. при увеличении содержания кислот в организме. Аммиак в почках образуется главным образом за счет амидной группы глутамина. Глутамин гидролизуется активируемой фосфатом глутаминазой, имеющейся в клетках эпителия канальцев почки. Часть аммиака (примерно 30%) образуется другим путем — в результате непрямого дезаминирования аминокислот.
Образующийся аммиак нейтрализует кислоты: NH3 + Н+ → NH4+. Неионизированные аммиак и кислоты в клетках находятся в равновесии с их ионизированными формами. Через клеточные мембраны проникают преимущественно неионизированные аммиак и кислоты, и в просвете почечного канальца (т. е. уже в моче) аммиак акцептирует протон кислоты, образуя аммонийную соль, которая выводится из организма. Экскреция аммиака почками служит для выведения именно кислот, а не азота, на что указывает значительная скорость экскреции при ацидозе, малая — при нормальной кислотности межклеточной жидкости и крови, и отсутствие экскреции аммиака при алкалозе. Одновременно этот процесс обеспечивает сохранение организмом ионов Na+, которые в отсутствие ионов аммония выводились бы с анионами кислот. Потеря таких количеств Na+, которые необходимы для выведения кислот при ацидозе, могла бы вызвать снижение осмотического давления межклеточной жидкости и крови, а вследствие этого уменьшение объема межклеточной жидкости, т. е. обезвоживание тканей.
3. Основным механизмом связывания аммиака в организме является синтез мочевины. Мочевина выводится из организма с мочой в качестве главного конечного продукта белкового, соответственно аминокислотного обмена. На долю мочевины приходится до 80-85 % от всего выводимого из организма азота. Количество выделяемой мочевины зависит от количества белков, поступающих с пищей. Если суточный рацион включает 80–100 г белка, то за сутки образуется и выводится 25–30 г мочевины.
Основным местом синтеза мочевины является печень. Синтез мочевины является циклическим метаболическим процессом и носит название орнитинового цикла мочевинообразования Кребса (цикл мочевины Кребса - Хензеляйта).
На первом этапе из NН3 и СО2 при участии АТФ синтезируется макроэргическое соединение карбамоилфосфат:

На
втором этапе цикла мочевинообразования
происходит конденсация карбомоилфосфата
и орнитина с образованиемцитруллина.
На следующей стадии вначале происходит
связывание одной молекулы NН3 путем
восстановительного аминирования с
образованием (с затратой молекулы АТФ)
аспарагиновой кислоты. Затем цитруллин
и аспарагиновая кислота взаимодействуют
с образованием аргининосукцината,
который распадается на аргинин и фумарат при
участии аргининосукцинатлиазы. Аргинин
расщепляется под действием фермента
аргиназы на орнитин и мочевину ![]() .
.
Образовавшийся орнитин может вступать в следующий цикл мочевинообразования. Хотя аргинин есть во всех клетках организма человека, образование мочевины происходит исключительно в клетках печени - единственном органе, где локализован фермент аргиназа. Мочевина из клеток печени поступает в кровь и выводится из организма через почки.
Для синтеза одной молекулы мочевины требуется две молекулы NН3, одна молекула СО2 и три молекулы АТФ.
Т.о., исходя из фактических данных о механизмах обезвреживания аммиака в организме часть аммиака используется на биосинтез аминокислот путем восстановительного аминирования a-кетокислот по механизму реакции трансаминирования. Аммиак связывается при биосинтезе глутамина и аспарагина. Некоторое количество аммиака выводится с мочой в виде аммонийных солей. В форме креатинина, который образуется из креатина и креатинфосфата, выделяется из организма значительная часть азота аминокислот. Наибольшее количество аммиак расходуется на синтез мочевины, которая выводится с мочой в качестве главного конечного продукта белкового обмена в организме человека и животных.
50,60
ОБМЕН СЕРИНА И ГЛИЦИНА.
РОЛЬ ФОЛИЕВОЙ КИСЛОТЫ
1. Серин- заменимая аминокислота, синтезируется из промежуточного продукта гликолиза - 3-фосфоглицерата в последовательности реакций дегидрирования, трансаминирования и гидролиза под действием фосфатазы
(рис. 9.17).
В организме серин используется для синтеза:
• фосфолипидов (фосфатидилсерины, сфингомиелины);
• аминокислот (глицина, цистеина).
Основной путь катаболизма серина его дезаминирование с образованием пирувата
2.Глицин образуется из серина под действием сериноксиметилтрансферазы.Коферментом этого фермента является тетрагидрофолиевая кислота (Н4-фолат), которая присоединяет β-углеродный атом серина, образуя метилен - Н4-фолат
(рис. 9.18):
Глицин является предшественником:
• порфиринов (гема),
• пуриновых оснований,
• коферментов,
• глутатиона и др.
Катаболизм глицинапроисходит
также сучастием Н4-фолата,который связывает а-СН2-группу глицина (см. рис.).
3.Н4-фолатобразуется в печени из фолиевой кислоты (фолата) с участием ферментов фолатредуктазы и дигидрофолатредуктазы ( см.рис.). Коферментом этих редуктаз является NADPH.
Метиленовая группа -СН2-в молекуле метилен-Н4-фолата может превращаться в другие одноуглеродные группы:
Н4-фолат способен передавать эти группы на другие соединения и играет роль промежуточного переносчика одноуглеродных групп. Одноуглеродные фрагменты используются для синтеза нуклеотидов и ряда соединений.
4. Фолиевая кислота является витамином для человека и большинства млекопитающих (витамин ВС или В9). Она широко распространена в пищевых продуктах и синтезируется бактериями кишечника. Гиповитаминоз у человека возникает достаточно редко. Причинами его могут послужить:
• неправильное питание - недостаточное потребление овощей, фруктов и мясных продуктов;
• нарушение всасывания фолиевой кислоты в кишечнике;
• гепатит, цирроз и другие поражения печени, вызывающие снижение активности фолатредуктазы.
Гиповитаминоз фолиевой кислоты приводит к нарушению синтеза нуклеиновых кислот в организме, что сказывается прежде всего на быстро делящихся клетках крови, и развитию мегалобластной анемии.
ОБМЕН МЕТИОНИНА.
1. Метионин - незаменимая аминокислота, необходимая для синтеза белков. Мет-тРНКмет участвует в инициации процесса трансляции каждого белка. Как и многие другие аминокислоты, метионин подвергается транс- и дезаминированию. Особая роль метионина заключается в том, что метильная группа этой аминокислоты используется для синтеза целого ряда соединений в реакциях трансметилирования. Основным донором метильной группы является S-аденозилметионин (SAM) - активная форма метионина, который присутствует во всех типах клеток и синтезируется из метионина и АТФ под действием фермента метионин-аденозилтрансферазы: Структура -S+-CH3 в SAM является нестабильной, метильная группа легко отщепляется, что определяет высокую способность ее к переносу на другие соединения в реакциях трансметилирования
В реакциях трансметилирования SAM превращается в S-аденозилгомо- цистеин (SAr), который гидролитически расщепляется с образованием аденозина и гомоцистеина. Последний может снова превращаться в метионин с участием метил-Н4-фолата и витамина В12. Регенерация метионина тесно связана с обменом серина и глицина и взаимопревращениями производных Н4-фолата
2. Метионин и серин необходимы для синтеза условно заменимой аминокислоты цистеина, причем в этом процессе метионин является донором атома серы. Цистеин образуется непосредственно из гомоцистеина в ходе двух реакций, которые происходят с участием пиридоксальфосфата . Генетический дефект этих ферментов приводит к нарушению использования гомоцистеина в организме и превращению его в гомоцистин.
Гомоцистин может накапливаться в крови и тканях, выделяться с мочой, вызывая гомоцистинурию. Заболевание сопровождается эктопией (смещением) хрусталика глаза, катарактой, остеопорозом, умственной отсталостью (-50% больных). Причиной заболевания могут служить как наследственные нарушения обмена гомоцистеина, так и гиповитаминоз фолиевой кислоты или витаминов В12 и
SАМ как донор метильной группы участвует в синтезе многих веществ (лецитина, адреналина, карнитина, ацетилхолина, креатина и др.), а также в инактивации нормальных метаболитов и обезвреживании токсических веществ в печени.
ОБМЕН ФЕНИЛАЛАНИНА, ТИРОЗИНА
1. Фенилаланин - незаменимая аминокислота, так как в клетках животных не синтезируется ароматическое кольцо. Основная часть поступающего с пищей фенилаланина используется в синтезе тканевых белков, превращение остальной части начинается с его гидроксилирования, в результате чего образуется тирозин. Реакция эта катализируется специфической монооксигеназой - фенилаланингидроксилазой, коферментом которой является тетрагидробиоптерин (Н4-БП)
1. Реакцию катализирует фенилаланингидроксилаза (1), коферментом которой является Н4БП. Кофактором являются ионы Fe2+. Н4БП в результате реакции окисляется в дигидробиоптерин (Н2БП).
2. Регенерация дигидробиоптерина (2) происходит при участии дигидробиоптеринредуктазы с использованием NADPH.
2. Тирозин - условно заменимая аминокислота. Синтезируется только из фенилаланина.
Катаболизм Фен и Тир происходит в печени. В результате ряда реакций образуется фумарат и ацетоацетат (рис. 9.23, А). Фумарат используется для синтеза глюкозы (глюконеогенез) или окисляется до СО2 и Н2О. Ацетоацетат - кетоновое тело, которое окисляется в тканях с выделением энергии. Таким образом, Фен и Тир относятся к смешанным (гликокетогенным) аминокислотам по использованию безазотистого остатка.
Превращение промежуточного продукта катаболизма Тир - гомогентизиновой кислоты - в фумарилацетоацетат сопровождается расщеплением ароматического кольца.
Процессы расщепления ароматических колец в биологических системах катализируются ферментами диоксигеназами. Для катализа диоксигеназам необходимыкофакторы - Fe2+ или гем (для некоторых - Сu+), а также - витамин С.
3. В мозговом веществе надпочечников и нервной ткани из тирозина синтезируются катехоламины (дофамин, норадреналин, адреналин)
Тирозин под действием специфической монооксигеназы - тирозингидроксилазы превращается в ДОФА. Для протекания реакции необходимы Н4БП, О2 и Fe2+ (реакция аналогична гидроксилированию фенилаланина,.Тирозингидроксилаза найдена только в надпочечниках и катехоламинэргических нейронах (преимущественно в их нервных окончаниях). Этот фермент является регуляторным и определяет скорость синтеза катехоламинов. Одна из функций последних - регуляция деятельности сердечнососудистой системы.
Активность тирозингидроксилазы значительно изменяется в результате:
• аллостерической регуляции по принципу ретроингибирования норадреналином;
• фосфорилирования с участием цАМР - зависимой протеинкиназы, при этом снижается Км для кофермента Н4БП и сродство фермента к норадреналину, в результате чего происходит активация тирозингидроксилазы;
• индукции синтеза фермента кортизолом.
Катехоламины выполняют очень важные функции в организме. Дофамин является медиатором среднего отдела мозга.Норадреналин - тормозный медиатор синаптической нервной системы и разных отделов головного мозга, но может выполнять функцию возбуждающего медиатора в гипоталамусе. Адреналин - гормон интенсивной физической работы, который синтезируется при стрессе и регулирует основной обмен, а также усиливает сокращение сердечной мышцы.
В щитовидной железе тирозин используется для синтеза гормонов иодтиронинов (тироксина и трииодтиронина)..
В меланоцитах - пигментных клетках кожи, сетчатки глаз тирозин является предшественником пигментов меланинов
Репликация ДНК
Реплика́ция (от лат. replicatio — возобновление) — процесс синтеза дочерней молекулыдезоксирибонуклеиновой кислоты на матрице родительской молекулы ДНК. В ходе последующего деления материнской клетки каждая дочерняя клетка получает по одной копии молекулы ДНК, которая является идентичной ДНК исходной материнской клетки. Этот процесс обеспечивает точную передачу генетической информации из поколения в поколение. Репликацию ДНК осуществляет сложный ферментный комплекс, состоящий из 15—20 различных белков, называемый реплисомой
Репликация проходит в три этапа:
-
инициация репликации
-
элонгация
-
терминация репликации.
Инициация - это самая начальная фаза репликации (удвоения) молекул ДНК, т.е. зарождение двух новых дочерних нитей ДНК на матрице старой двойной родительской молекулы.
2. Элонгация (удлинение цепи).
Комплекс ферментов репликации, называемый реплисомой, движется вдоль молекулы ДНК-матрицы, расплетая ее и наращивая комплементарные цепи ДНК.
3. Терминация (окончание репликации).
В ДНК имеются сайты терминации репликации, содержащие специфические последовательности, с которыми связываются терминаторные белки, препятствующие дальнейшему продвижению репликативной вилки. Синтез ДНК заканчивается.
ДНК-реплицирующий комплекс включает в себя около 20 компонентов. Отметим главные из них.
Геликаза (хеликаза) расплетает ДНК на две отдельные цепи. Образуется репликативная вилка. По-видимому, при этом данный участок расплетённой ДНК отделяется от хромосомных белков. На разъединение комплементарной связи в каждой паре нуклеотидов тратится энергия 2-х молекул АТФ.
Молекула ДНК жестко закреплена в некоторых учакстках на ядерном матриксе и поэтому не может свободно вращаться при расплетании. Это блокирует продвижение геликазы по цепи.
Топоизомераза надрывает одну из двух нитей ДНК, и она раскручивается вокруг целой нити. Так снимается структурное напряжение при раскручивании спирали. Затем разорванные концы сращиваются обратно тем же ферментом. У бактерий другой вид топоизомеразы (гираза) разрывает сразу обе цепи ДНК, а после раскручивания спирали соединяет их вновь.
