
- •2. Механизм действия тиреоидных гормонов.
- •2. Гормоны кальциевого обмена
- •Кальцитриол
- •Регуляция синтеза и секреции
- •Механизм действия
- •1. Ферменты
- •5. Регуляция действия ферментов
- •Ингибиторы ферментов
- •Гипервитаминоз
- •Гиповитаминоз
- •Гипервитаминоз
- •Вит.К(филлохинон)
- •Переизбыток
- •Вит. F( арахидоновая, линолевая, линоленовая к-ты)
- •Окислительное декарбоксилирование пировиноградной кислоты
- •Цитратный цикл
- •14 Разобщители тканевого дыхания (динитроортокрезол)
- •Всасывание углеводов
- •Нарушение переваривания и всасывания углеводов
- •18. Биологическая роль, синтез и распад гликогена. Особенности распада гликогена в печени и скелетных мышцах.
- •31. Мобилизация липидов из жировых депо
- •37. Синтез и использование кетоновых тел. Понятие и причины кетонемии и кетонурии.
- •38. Липопротеины сыворотки крови: биологическая роль, особенности состава и разновидности. Понятие атерогенных и антиатерогенных липопротеинов.
- •39. Нарушения липидного обмена:
- •Симптомы заболевания
- •40. Понятие и разновидности азотистого баланса.
- •41. Особенности переваривания белков. Нормальные и патологические компоненты желудочного сока.
- •42. Гниение белков в толстом кишечнике.
- •43. Реакции дезаминирования аминокислот и их биологическая роль.
- •44. Трансаминирование аминокислот: биологическая роль реакций, использование в диагностике.Глюкозо-аланиновый цикл.
- •45. Декарбоксилирование аминокислот. Образование и биологическая роль биогенных аминов: гамма-аминомасляной кислоты (гамк), гистамина, серотонина, дофамина. Инактивация биогенных аминов.
- •46. Использование безазотистых остатков аминокислот: понятие, биологическая роль и примерыгликогенных и кетогенных аминокислот.
- •47. Источники образования аммиака в организме. Причины токсичности аммиака. Понятие гипераммониемии.
- •Причины токсичности аммиака
- •48. Пути обезвреживания аммиака и их особенности в почках, печени, нервной ткани.
- •51. Биологическая роль и биосинтез креатина.
- •52. Энзимопатии аминокислотного обмена (метаболические блоки и клинические проявления) :
- •II. Синтез пуриновых нуклеотидов
- •56. Синтез пиримидиновых нуклеотидов dе novo его регуляция
- •58. Ингибиторы синтеза тимидиловых нуклеотидов
- •Секреция
- •Механизм
- •77. Медицинские показания и правило проведения теста «сахарной нагрузки» (теста толерантности к глюкозе).
- •78. Адреналин - гормон мозгового вещества надпочечников: схема синтеза и названия ферментов. Механизм действия адреналина и его влияние на обмен веществ.
- •Аденилатциклазный механизм
- •Кальций-фосфолипидный механизм
- •79. Гормоны коры надпочечников: классификация по химической структуре, схема основных этапов синтеза из холестерола, механизм действия.
- •1. Биосинтез йодтиронинов
- •2. Регуляция синтеза и секреции йодтиронинов
- •3. Механизм действия и биологические
- •4. Заболевания щитовидной железы
- •85. Биохимические характеристики гипо- и гиперфункции щитовидной железы.
- •86. Паратгормон: структура, механизм действия и роль в метаболизме кальция и фосфатов.
- •87. Кальцитонин: структура, механизм действия и роль в метаболизме кальция и фосфатов.
- •88. Кальцитриол: структура, этапы синтеза, механизм действия и роль в метаболизме кальция и фосфатов. Рахит.
- •90. Эйкозаноиды:классификация, этапы бисинтеза, примеры соединений. Биологические эффекты эйкозаноидов. Механизм действия нестероидных противовоспалительных препаратов на примере аспирина.
- •94. Ферменты сыворотки крови: их происхождение и значение для диагностики заболеваний.
- •95. Буферные системы крови. Нарушения кислотно-щелочного равновесия крови.
- •109. Изменения в соединительной ткани при старении, коллагенозах, мукополисахаридозах. Роль соединительной ткани в заживлении ран
- •Ситуационные задачи по биохимии для студентов лечебного факультета
- •Эталон ответа
- •Эталон ответа
- •Эталон ответа
- •Задача №42
- •Эталон ответа
- •Задача №43
- •Эталон ответа
- •Задача №44
- •Эталон ответа
- •Задача №45
- •Эталон ответа
- •Ситуационные задачи по биохимии для студентов лечебного факультета
- •Эталон ответа
- •Эталон ответа
- •Эталон ответа
- •Задача №42
- •Эталон ответа
- •Задача №43
- •Эталон ответа
- •Задача №44
- •Эталон ответа
- •Задача №45
- •Эталон ответа
2. Гормоны кальциевого обмена
За обмен кальция и фосфатов в организме отвечают три гормона – кальцитриол, кальцитонин и паратиреоидный гормон.
Кальцитриол
|
Строение кальцитриола |
Представляет собой производное витамина D и относится к стероидам.
Синтез
Образующийся в коже под действием ультрафиолета и поступающие с пищей холекальциферол (витамин D3) и эргокальциферол (витамин D2) гидроксилируются в гепатоцитах по С25 и в эпителии проксимальных канальцев почек по С1. В результате формируется 1,25-диоксихолекальциферол (кальцитриол).
Регуляция синтеза и секреции
Активируют: Гипокальциемия повышает гидроксилирование витамина D по С1 в почках через увеличение секреции паратгормона, стимулирующего этот процесс.
Уменьшают: Избыток кальцитриола подавляет гидроксилирование по С1 в почках.
Механизм действия
Цитозольный.
Костная ткань
-
при высоком уровне гормона активируются остеокласты и происходит деструкция костной ткани,
-
при низких концентрациях активируется перестройка кости и остеогенез.
Почки
-
увеличивается реабсорбция кальция и магния,
-
уменьшается реабсорбция фосфатов, аминокислот, карбонатов, натрия, хлоридов, сульфатов.
-
также гормон стимулирует образование кальцитриола (гидроксилирование по С1).
Кишечник
-
при участии кальцитриола усиливается всасывание кальция и фосфатов
26. 1. Биохимические функции печени: 1) регуляторно-гомеостатическая; 2) мочевинообразовательная; 3) желчеобразовательная; 4экскреторная; 5обезвреживающая.
регуляторно-гомеостатическаяфункция реализуется через участие в обмене питательных веществ
а. углеводный обмен.печень обеспечивает постоянство уровня глюкозы в кровипри повышении глюкозы кровинапримерпосле приема пищиактивируется глюкокиназаобразуется глюкозо-6-фосфаткоторый активно используется в гликолизепфцв синтезе гликогенапри снижении глюкозы кровинапримерпри голоданиисначалабыстро активируется гликогенолизпозжеболее медленно- глюконеогенезв основном из аминокислота также из лактатаобразующегося в мышцахсвободнаянефосфорилированная) глюкоза выходит в кровь и используется разными тканямив первую очередьнервной.
б. липидный обмен
-
образующиеся в печени желчные кислоты нужны для переваривания и всасывания липидов (эмульгация жировактивация панкреатической липазытранспорт длинноцепочечных жирных кислот
-
происходит синтез жирных кислоттаг преимущественно из глюкозысм. схемуили из жирных кислотпоступающих с кровьюфл сфинголипидовхси его эфировпричем холестерина синтезируется большечем поступает с пищей.скорость синтезафл определяетсялимитируетсяколичеством липотропных факторов; регуляция синтеза холестерина и его метаболизм - см. лекцию.
-
печень распределяет липиды по тканям посредством образования и секреции лпвп -лпилпонппре--лп т.к. помимо липидовздесь синтезируется белковая частьлп - апо а апов и др. Т.о.в норме синтезируемые ТаГ не накапливаются в печениа в составелпонптранспортируются по крови в жировую ткань для хранения.
-
в печени происходит распад таг,окислениежк синтез кетоновых телявляющихся энергетическими субстратами для внепеченочных тканей.
в. обмен белков
i. синтез белков. из 80-100 г белковсинтезируемых в организме человекаполовина образуется в печени.вгепатоцитах образуютсяспецифические белки плазмы крови1) все альбумины13-18 гсут75-90-глобулинов50-глобулинова в купферовских клетках --глобулины; 2) белки свертывающей и антисвертывающей систем кровинапримерфибриноген протромбинпроконвертинпроакцелерин3) транспортные белки: трансферринцерулоплазмин транскортинретинолсвязывающих белоккальциферолсвязывающий белоктироксинсвязывающий глобулин тестостерон-эстрадиол-связывающий глобулин,нртранскобаламиныi и ii и т.д.т.е. белкиучаствующие в переносе минеральных веществвитаминовгормоновнвбилирубина и т.д. 4) ферментыфункционирующие в плазмехолинэстеразалхатпеченочная липаза и др.
ii обмен аминокислотактивно протекают как их собственный синтезтак и использование аминокислот в синтезе других веществкреатинахолинаглутатионаникотиновой кислотыпуриновпиримидиновпорфиринов и т.д. Аминокислоты активно переаминируютсядезаминируютсядекарборсилируютсяих углеродные скелеты либо используются в синтезе глюкозынапример, кетоновых тел, либо сгорают с выделением энергии.при голодании печень первой расщепляет свои резервные белки для снабжения аминокислотами других тканей.
2. Орнитиновый цикл
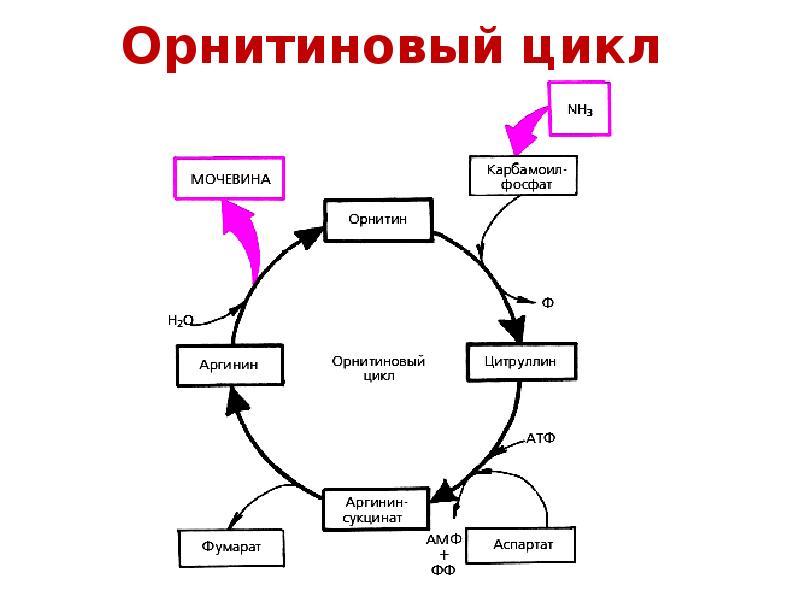
29. 1. Реплика́ция ДНК — процесс синтеза дочерней молекулы дезоксирибонуклеиновой кислоты на матрице родительской молекулы ДНК. В ходе последующего деления материнской клетки каждая дочерняя клетка получает по одной копии молекулы ДНК, которая является идентичной ДНК исходной материнской клетки. Этот процесс обеспечивает точную передачу генетической информации из поколения в поколение. Репликацию ДНК осуществляет сложный ферментный комплекс, состоящий из 15—20 различных белков.
Репликация ДНК — ключевое событие в ходе деления клетки. Репликация проходит в три этапа:
инициация репликации
элонгация
терминация репликации.
Регуляция репликации осуществляется в основном на этапе инициации. Это достаточно легко осуществимо, потому что репликация может начинаться не с любого участка ДНК, а со строго определённого, называемого сайтом инициации репликации. В геноме таких сайтов может быть как всего один, так и много. С понятием сайта инициации репликации тесно связано понятие репликон. Репликон — это участок ДНК, который содержит сайт инициации репликации и реплицируется после начала синтеза ДНК с этого сайта. Геномы бактерий, как правило, представляют собой один репликон, это значит, что репликация всего генома является следствием всего одного акта инициации репликации. Геномы эукариот (а также их отдельные хромосомы) состоят из большого числа самостоятельных репликонов, это значительно сокращает суммарное время репликации отдельной хромосомы. Молекулярные механизмы, которые контролируют количество актов инициации репликации в каждом сайте за один цикл деления клетки, называются контролем копийности. В бактериальных клетках помимо хромосомной ДНК часто содержатся плазмиды, которые представляют собой отдельные репликоны. У плазмид существуют свои механизмы контроля копийности: они могут обеспечивать синтез как всего одной копии плазмиды за клеточный цикл, так и тысяч копий[1].
Репликация начинается в сайте инициации репликации с расплетания двойной спирали ДНК, при этом формируетсярепликационная вилка — место непосредственной репликации ДНК. В каждом сайте может формироваться одна или две репликационные вилки в зависимости от того, является ли репликация одно- или двунаправленной. Более распространена двунаправленная репликация. Через некоторое время после начала репликации в электронный микроскоп можно наблюдать репликационный глазок — участок хромосомы, где ДНК уже реплицирована, окруженный более протяженными участками нереплицированной ДНК[1].
В репликационной вилке ДНК копирует крупный белковый комплекс (реплисома), ключевым ферментом которого является ДНК-полимераза. Репликационная вилка движется со скоростью порядка 100 000 пар нуклеотидов в минуту у прокариот и 500—5000 — у эукариот[3].
Молекулярный механизм репликации
Ферменты (хеликаза, топоизомераза) и ДНК-связывающие белки расплетают ДНК, удерживают матрицу в разведённом состоянии и вращают молекулу ДНК. Правильность репликации обеспечивается точным соответствием комплементарных пар оснований и активностью ДНК-полимеразы, способной распознать и исправить ошибку. Репликация у эукариот осуществляется несколькими разными ДНК-полимеразами. Далее происходит закручивание синтезированных молекул по принципусуперспирализации и дальнейшей компактизации ДНК. Синтез энергозатратный.
Цепи молекулы ДНК расходятся, образуют репликационную вилку, и каждая из них становится матрицей, на которой синтезируется новая комплементарная цепь. В результате образуются две новые двуспиральные молекулы ДНК, идентичные родительской молекуле.
Характеристики процесса репликации
матричный — последовательность синтезируемой цепи ДНК однозначно определяется последовательностью материнской цепи в соответствии с принципом комплементарности;
полуконсервативный — одна цепь молекулы ДНК, образовавшейся в результате репликации, является вновь синтезированной, а вторая — материнской;
идёт в направлении от 5’-конца новой молекулы к 3’-концу;
полунепрерывный — одна из цепей ДНК синтезируется непрерывно, а вторая — в виде набора отдельных коротких фрагментов (фрагментов Оказаки);
начинается с определённых участков ДНК, которые называются сайтами инициации репликации называемый реплисомой
30. 1. Гемоглобин входит в состав группы белков гемопротеины, которые сами являются подвидом хромопротеинов и подразделяются на неферментативные белки (гемоглобин, миоглобин) и ферменты (цитохромы, каталаза, пероксидаза). Небелковой частью их является гем – структура, включающая в себя порфириновое кольцо (состоящее из 4 пиррольных колец) и иона Fe2+. Железо связывается с порфириновым кольцом двумя координационными и двумя ковалентными связями.
Нормальные формы гемоглобина
Существует несколько нормальных вариантов гемоглобина:
-
HbР – примитивный гемоглобин, содержит 2ξ- и 2ε-цепи, встречается в эмбрионе между 7-12 неделями жизни,
-
HbF – фетальный гемоглобин, содержит 2α- и 2γ-цепи, появляется через 12 недель внутриутробного развития и является основным после 3 месяцев,
-
HbA – гемоглобин взрослых, доля составляет 98%, содержит 2α- и 2β-цепи, у плода появляется через 3 месяца жизни и к рождению составляет 80% всего гемоглобина,
-
HbA2 – гемоглобин взрослых, доля составляет 2%, содержит 2α- и 2δ-цепи,
-
HbO2 – оксигемоглобин, образуется при связывании кислорода в легких, в легочных венах его 94-98% от всего количества гемоглобина,
-
HbCO2 – карбогемоглобин, образуется при связывании углекислого газа в тканях, в венозной крови составляет 15-20% от всего количества гемоглобина.
Патологические формы гемоглобина
HbS – гемоглобин серповидно-клеточной анемии.
MetHb – метгемоглобин, форма гемоглобина, включающая трехвалентный ион железа вместо двухвалентного. Такая форма образуется спонтанно, при взаимодействиимолекулы O2 и гемового Fe2+, но обычно ферментативных мощностей клетки хватает на его восстановление.
Hb-CO – карбоксигемоглобин, образуется при наличии СО (угарный газ) во вдыхаемом воздухе. Он постоянно присутствует в крови в малых концентрациях, но его доля может колебаться от условий и образа жизни.
31. 1. Инсулин
Инсулин – это простой белок, состоящий их двух цепей: А (21 аминокислота) и В (30
аминокислот), связанных между собой двумя дисульфидными мостиками, третий S S
мостик находится в А-цепи.
Вырабатывается в виде проинсулина, состоящего из одной полипептидной цепи (84
аминокислотных остатка), активируется частичным протеолизом. Это гормон
избытка – он вырабатывается после приема пищи, таким образом поддерживая
постоянство веса.
Период полураспада - 8-25 мин. Деградация в печени.
Синтез и секреция инсулина регулируется уровнем глюкозы в крови. Глюкоза является
основным энергетическим субстратом. Источниками глюкозы для организма служат
углеводы пищи и эндогенное производство глюкозы (главным образом, печенью) путем
гликогенолиза (распада гликогена) и глюконеогенеза (синтеза глюкозы из неуглеводов).
Концентрация глюкозы в крови зависит от соотношения выброса ее в кровоток и
утилизации тканями.
Концентрация глюкозы в норме жестко регулируется и у здоровых людей редко падает
ниже 2,5 ммоль/л или превышает 8,0 ммоль/л независимо от режима питания. В норме
концентрация глюкозы в крови составляет 3,3 -5,5 ммоль/л.
Ткани-мишени: жировая ткань, скелетные мышцы, печень.
Инсулин находится в двух формах:
свободный инсулин - атакует все ткани-мишени;
связанный (с белками) - действует только на жировую ткань
Углеводный обмен.
Инсулин - единственный гипогликемический гормон, который снижает
концентрацию глюкозы в крови следующими путями:
повышает проницаемость клеточных мембран для глюкозы в жировой ткани и
скелетных мышцах;
повышает проницаемость клеточной мембраны для ионов кальция;
повышает активность фосфодиэстеразы, которая расщепляет цАМФ, благодаря
чему снижается распад гликогена;
стимулирует синтез гликогена путем активации гликогенсинтазы;
повышает активность основных ферментов гликолиза - гексокиназы (снимает с нее
ингибирующий комплекс глюкокортикоидов), глюкокиназы, фосфофруктокиназы,
пируваткиназы;
повышает активность ферментов, участвующих в окислении глюкозы до конечных
продуктов (ЦТК): пируват- и альфа-кетоглутаратдегидрогеназных комплексов,
цитратсинтазы, изоцитратдегидрогеназы;
увеличивает скорость прямого окисления глюкозы - пентозо-фосфатного пути
через активацию глюкозо-6-фосфатдегидрогеназы;
ингибирует ферменты глюконеогенеза, таким образом препятствует накоплению
глюкозы (в результате избирательного ингибирования транскрипции гена,
кодирующего мРНК для основного фермента глюконеогенеза - фосфоенолпируваткарбоксикиназы – ФЕПКК).
Жировой обмен
Инсулин противостоит большинству гормонов, т.к. активирует синтез жира:
повышает активность липопротеинлипазы, которая расщепляет хиломикроны, что
способствует поступлению ресинтезированных в кишечнике жиров в жировую ткань;
поддерживает нормальный уровень регуляторного фермента синтеза ВЖК - ацетилКоА-карбоксилазы, катализирующего превращение ацетил-КоА в малонил-КоА,
который «запускает» синтез ВЖК;
активируют синтез ВЖК (через усиление образования ацетил-КоА и НАДФН2 при
прямом и непрямом окислении глюкозы);
усиливает синтез ТАГ из ВЖК и глицерина, которые образуются из глюкозы ;
снижает активность гормончувствительной липазы жировой ткани, благодаря чему
жир задерживается в депо.
Белковый обмен
Инсулин - сильный анаболик, способствует синтезу белка на всех стадиях:
повышает проницаемость клеточных мембран для аминокислот;
тормозя глюконеогенез, «сохраняет» аминокислоты для биосинтеза белка;
усиливает репликацию, способствует транскрипции, активирует трансляцию.
33. 1. Лактатдегидрогеназа (L‑лактат:НАД‑оксидоредуктаза, ЛДГ, КФ 1.1.1.27) является гликолитическим ферментом и катализирует следующую реакцию:
Лактат
+ НАД ![]() Пируват
+ НАДН
Пируват
+ НАДН
Молекула ЛДГ представляет собой тетрамер, состоящий из одного или двух типов субъединиц, обозначаемых как M (англ: muscle) и H (англ: heart). В сыворотке крови фермент существует в пяти молекулярных формах, различающихся по первичной структуре, кинетическим свойствам, электрофоретической подвижности (ЛДГ‑1 быстрее движется к аноду по сравнению с ЛДГ‑5, то есть более электрофоретичеки подвижна). Каждая форма имеет характерный полипептидный состав: ЛДГ‑1 состоит из 4 H‑субъединиц, ЛДГ‑2 — из 3 H‑субъединиц и 1 M‑субъединицы, ЛДГ‑3 представляет собой тетрамер из 2 H‑субъединиц и 2 M‑субъединиц, ЛДГ‑4 содержит 1 H‑субъединицу и 3 M‑субъединицы, ЛДГ‑5 состоит только из M‑субъединиц.
2. В медицине нашло практическое применение определение активности двух ферментов трансаминирования – аланинаминотрансферазы (АЛТ, АлАТ) и аспартатаминотрансферазы (АСТ, АсАТ).
Оба
фермента обратимо взаимодействуют с
α-кетоглутаровой кислотой и переносят
на нее аминогруппы от соответствующих
аминокислот с образованием глутаминовой
кислоты и кетокислот.
Реакции, катализируемые аланинаминотрансферазой и аспартатаминотрансферазой
Хотя активность обоих ферментов значительно возрастает при заболеваниях сердечной мышцы и печени, при поражении клеток миокарда наибольшая активность в сыворотке крови обнаруживается для АСТ, при нарушении печени (гепатиты различного генеза) – для АЛТ.
32. 1. Бледная поганка Трансляция
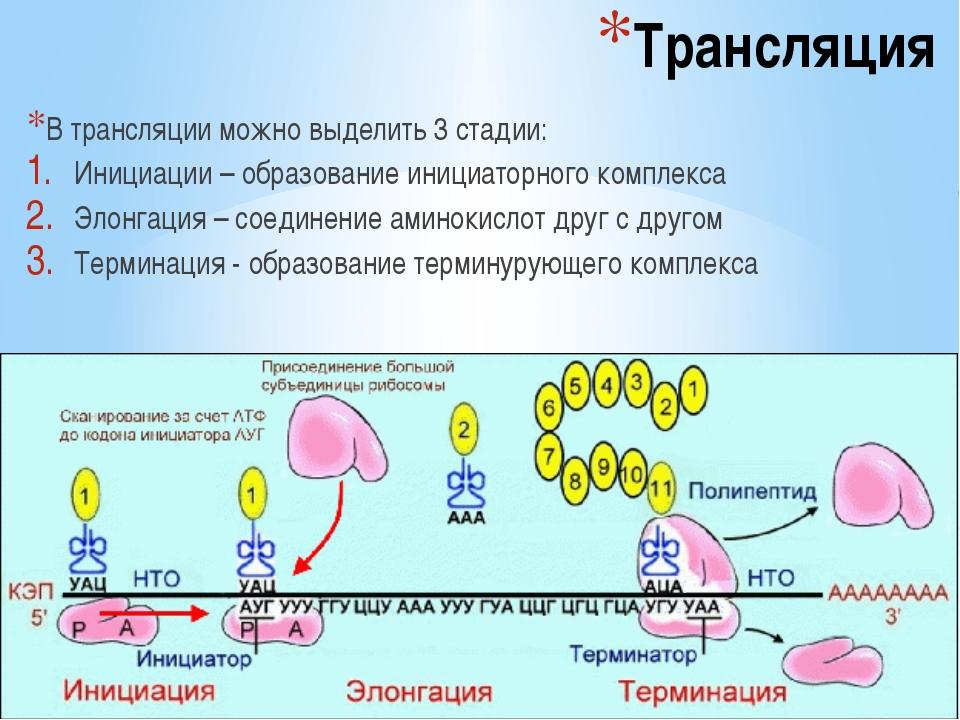
Трансляция
(англ. translation –
перевод) – это биосинтез белка на матрице
мРНК.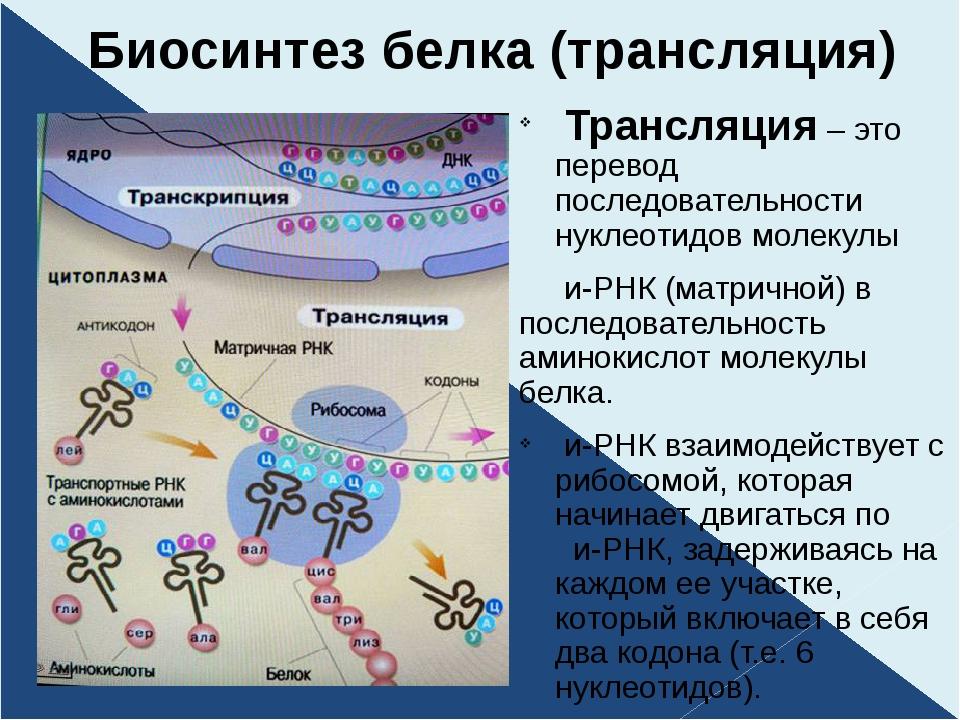
После переноса информации с ДНК на матричную РНК начинается синтез белков. Каждая зрелая мРНК несет информацию только об одной полипептидной цепи. Если клетке необходимы другие белки, то необходимо транскрибировать мРНК с иных участков ДНК.
Биосинтез белков или трансляция происходит на рибосомах, внутриклеточных белоксинтезирующих органеллах, и включает 5 ключевых элементов:
-
матрица – матричная РНК,
-
растущая цепь – полипептид,
-
субстрат для синтеза – 20 протеиногенных аминокислот,
-
источник энергии – ГТФ,
-
рибосомальные белки, рРНК и белковые факторы.
2. Липопротеиды
Липопротеиды (ЛП) - это сферические частицы, состоящие из гидрофобного ядра и амфифильной оболочки. Ядро содержит неполярные триацилглицериды (ТАГ) и эфиры холестерина. Оболочка построена из полярных липидов - холестерина и фосфолипидов, причем заряженные концы этих молекул обращены наружу. Кроме того, в состав оболочки входят белки, нековалентно связанные с фосфолипидами и холестерином, называемые апопротеинами (А, В, С, D,E).

Все липопротеины участвуют в транспорте холестерина и его эфиров по крови и распределении их по органам.
Хиломикроны транспортируют экзогенный холестерин от кишечника через кровь в печень.
ЛПОНП образуются в печени (в небольших количествах – в кишечнике) и транспортируют экзо- и эндогенный холестерин (наряду с другими липидами) через кровь к тканям. Эти формы липопротеинов (ХМ и ЛПОНП) являютмя короткоживущими (полупериод их жизни составляет 1,5 – 2 часа). плазма крови послеприема жирной пищи плазма крови после голодания
Липопротеинлипаза (ЛП-липаза) на поверхности эндотелия сосудов расщепляет ТАГ в составе хиломикронов и ЛПОНП, превращая их в остаточные хиломикроны и остаточные ЛПОНП (называемые ЛППП - липопротеины промежуточной плотности), соответственно. Эти частицы поглощаются печенью путем эндоциоза (через «узнавание» рецепторами).
-
В2 – рибофлавин – витамин роста

Витамин В6 – пиридоксин - антидермитный

Витамин К (нафтохиноны, антигеморрагический)
Выделяют три формы витамина: витамин К1 (филлохинон), витамин К2 (менахинон), витамин К3 (менадион). После всасывания менадион превращается в активную форму – менахинон.

витамин обеспечивает:
1. Синтез факторов свертывания крови в печени – Кристмаса (ф.IX), Стюарта (ф.X), проконвертина (ф.VII), протромбина (ф.II);
2. Синтез белков костной ткани, например, остеокальцина.
3. Синтез протеина C и протеина S, участвующих в работе антисвертывающей системы крови.
Гиповитаминоз K
Причина
Возникает при подавлении микрофлоры лекарствами, особенно антибиотиками, при заболеваниях печени и желчного пузыря. У взрослых здоровая кишечная микрофлора полностью удовлетворяет потребность организма в витамине.
Клиническая картина
Наблюдается кровоточивость, снижение свертываемости крови, легкое возникновение подкожных гематом,
толерантность к глюкозе Изменение толерантности к глюкозе при сахарном диабете
|
|
У больных с СД после приёма пищи концентрация глюкозы в крови может достигать 300-500 мг/дл и сохраняется на высоком уровне в постабсорбтивном периоде, т.е. снижается толерантность к глюкозе. На стадии латентного СД концентрация глюкозы в крови натощак соответствует норме, а нагрузочные пробы уже выявляют снижение толерантности к глюкозе. Определение толерантности к глюкозе Обследуемый принимает раствор глюкозы из расчёта 1 г на 1 кг массы тела (сахарная нагрузка). Концентрацию глюкозы в крови измеряют в течение 2-3 ч с интервалами в 30 мин. 1 — у здорового человека; 2 — у больного сахарным диабетом. |
Серповидно-клеточная анемия
HbS – гемоглобин серповидно-клеточной анемии. При этом нарушении в ДНК в результате точковой мутации триплет ЦТТ заменен на триплет ЦАТ, что влечет за собой включение в 6-м положении β-цепи вместо глутамата аминокислоты валина. Изменение свойств β-цепи влечет изменение свойств всей молекулы и формирование на поверхности гемоглобина "липкого" участка. При дезоксигенации гемоглобина участок "раскрывается" и связывает одну молекулу дезоксигемоглобина S с другими подобными. Результатом является полимеризация гемоглобиновых молекул и образование крупных белковых тяжей, вызывающих деформацию эритроцитов и, при прохождении ими капилляров, гемолиз.
Изоферменты. Часть ферментов состоят не из одной белковой цепочки, а из нескольких субъединиц. Изоферменты – это семейство ферментов, которые катализируют одну и ту же реакцию, но отличаются по строению и физико-химическим свойствам.
Например: лактатдегидрогеназа (ЛДГ) состоит их 4 субъединиц 2хтипов: субъединица Н, выделенная из сер дечной мышцы (heart – сердце), субъединица М, выделенная из скелетных мышц (musculus – мышца). Эти субъединицы кодируются разными генами
ФОЛИЕВАЯ
КИСЛОТА (витамин В9 или Вс) фактор роста
(антианемический)
Гиперпродукция глюкокортикоидов (гиперкортицизм) может быть следствием повышения уровня АКТГ при опухолях гипофиза (болезнь Иценко-Кушинга) и опухолях других клеток (бронхов, тимуса, поджелудочной железы), вырабатывающих кортикотропинподобные вещества, или избыточного синтеза кортизола при гормонально-активных опухолях коры надпочечников (синдром Иценко-Кушинга).
При гиперкортицизме наблюдаются гипергликемия и снижение толерантности к глюкозе, обусловленные стимуляцией глюконеогенеза ("стероидный диабет"), усиление катаболизма белков, уменьшение мышечной массы, истончение кожи, остеопороз, инволюция лимфоидной ткани. Характерно своеобразное перераспределение отложений жира ("лунообразное лицо", выступающий живот).
ВИТАМИН
В12 - кобаламин – антианемический




Энергетическая функция. Образовавшиеся в ЦТК 3 молекулы НАДН2в последующем окисляются в длинной ЦПЭ с образованием 9 молекул АТФ
Образовавшийся в ЦТК ФАДН2 окисляется в короткой ЦПЭ, давая энергию для синтеза 2 молекул АТФ.
В сукцинилтиокиокиназной реакции ЦТК непосредственно образуется 1 макроэрг – ГТФ (1 ГТФ = 1 АТФ).
Анаболическая функциязаключается в том, что некоторые метаболиты цикла Кребса не окисляются в нём, а используются для синтеза новых веществ.



