
- •Кинетическая энергия вращающегося тела
- •Основные положения мкт строения вещества.
- •Идеальный газ.
- •Экспериментальные газовые законы
- •Опыт Эндрюса. Поправка на собственные размеры молекул.
- •Вопросы по электромагнетизму
- •Связь между потенциалом и напряженностью электрического поля.
- •Гармоническое колебание- это периодическое колебание, при котором координата, скорость, ускорение, характеризующие движение, изменяются по закону синуса или косинуса.
Опыт Эндрюса. Поправка на собственные размеры молекул.
 В
1869 году английский ученый Т.Эндрюс
опубликовал результаты своих исследований
свойств углекислого газа при различных
давлениях и температурах. Сжимая газ
под поршнем, Т. Эндрюс обнаружил, что
при уменьшении объема давление газа
увеличивалось, а затем, начиная с
некоторого объема, принимало постоянное
значение. При этом в цилиндре постепенно
происходил процесс конденсации: сначала
жидкость появлялась в виде отдельных
капель, затем, при дальнейшем сжатии,
она постепенно заполняла весь объем.
Опыты Эндрюса, производимые при разных
температурах, показали, что процесс
фазового перехода зависит как от
давления, так и от температуры. В
результате было экспериментально
обнаружено, что жидкое состояние может
существовать только в определенном
диапазоне температур, верхняя граница
которого не может превышать критическую
температуру (Тк),
имеющую определенное значение для
каждого вещества. Например, сжижение
углекислого газа можно осуществить
только при его сжатии при Т <
–31oC
(рис. 3). При температурах же выше Тк вещество
всегда остается в газообразном состоянии
независимо от приложенного давления.
Полученные результаты объяснили
неудачи в опытах ученых 19 века по сжижению
некоторых газов (азот, кислород, водород),
которые имеют низкие значения Тк (–146,
–118, –240
oC,
соответственно), вследствие чего для
сжатия таких газов необходимо
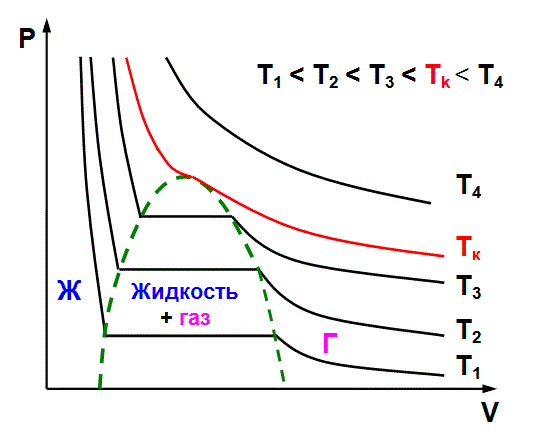
сильное охлаждение. Типичный вид
экспериментальных изотерм однокомпонентного
вещества приведен на (рис. 6 Изотермы
реального газа)
В
1869 году английский ученый Т.Эндрюс
опубликовал результаты своих исследований
свойств углекислого газа при различных
давлениях и температурах. Сжимая газ
под поршнем, Т. Эндрюс обнаружил, что
при уменьшении объема давление газа
увеличивалось, а затем, начиная с
некоторого объема, принимало постоянное
значение. При этом в цилиндре постепенно
происходил процесс конденсации: сначала
жидкость появлялась в виде отдельных
капель, затем, при дальнейшем сжатии,
она постепенно заполняла весь объем.
Опыты Эндрюса, производимые при разных
температурах, показали, что процесс
фазового перехода зависит как от
давления, так и от температуры. В
результате было экспериментально
обнаружено, что жидкое состояние может
существовать только в определенном
диапазоне температур, верхняя граница
которого не может превышать критическую
температуру (Тк),
имеющую определенное значение для
каждого вещества. Например, сжижение
углекислого газа можно осуществить
только при его сжатии при Т <
–31oC
(рис. 3). При температурах же выше Тк вещество
всегда остается в газообразном состоянии
независимо от приложенного давления.
Полученные результаты объяснили
неудачи в опытах ученых 19 века по сжижению
некоторых газов (азот, кислород, водород),
которые имеют низкие значения Тк (–146,
–118, –240
oC,
соответственно), вследствие чего для
сжатия таких газов необходимо
сильное охлаждение. Типичный вид
экспериментальных изотерм однокомпонентного
вещества приведен на (рис. 6 Изотермы
реального газа)


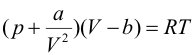
П
 оверхностное
натяжение жидкости
(коэффициент поверхностного
натяжения жидкости) –
это физическая величина,
которая характеризует
данную жидкость и равна отношению
поверхностной энергии к
площади поверхности
жидкости. ( Н/м)
оверхностное
натяжение жидкости
(коэффициент поверхностного
натяжения жидкости) –
это физическая величина,
которая характеризует
данную жидкость и равна отношению
поверхностной энергии к
площади поверхности
жидкости. ( Н/м)
коэффициент
поверхностного натяжения
характеризует удельную
энергию взаимодействия
молекул, а значит факторы,
изменяющие эту энергию,
изменят и коэффициент
поверхностного натяжения
жидкости. Итак, коэффициент
поверхностного
натяжения ![]() зависит
от:
зависит
от:
1. Природы жидкости (у «летучих» жидкостей, таких как эфир, спирт и бензин, поверхностное натяжение меньше, чем у «нелетучих» – воды, ртути и жидких металлов).
2. Температуры (чем выше температура, тем меньше поверхностное натяжение).
3. Наличие поверхностно активных веществ, уменьшающих поверхностное натяжение (ПАВ), например мыла или стирального порошка.
4. Свойства газа, граничащего с жидкостью.
Отметим, что коэффициент поверхностного натяжения не зависит от площади поверхности, так как для одной отдельно взятой приповерхностной молекулы абсолютно неважно, сколько таких же молекул вокруг.
Капиллярные явления, поверхностные явления на границе жидкости с др. средой, связанные с искривлением ее поверхности.
 Искривление
поверхности жидкости на границе с
газовой фазой происходит в результате
действия поверхностного натяжения
жидкости, которое стремится сократить
поверхность раздела и придать ограниченному
объему жидкости форму шара. Поскольку
шар обладает минимальной поверхностью
при данном объеме, такая форма отвечает
минимуму поверхностной энергии жидкости,
т.е. ее устойчивому равновесному
состоянию. В случае достаточно больших
масс жидкости действие поверхностного
натяжения компенсируется силой тяжести,
поэтому маловязкая жидкость быстро
принимает форму сосуда, в который она
налита, а ее своб. поверхность представляется
практически плоской.
Искривление
поверхности жидкости на границе с
газовой фазой происходит в результате
действия поверхностного натяжения
жидкости, которое стремится сократить
поверхность раздела и придать ограниченному
объему жидкости форму шара. Поскольку
шар обладает минимальной поверхностью
при данном объеме, такая форма отвечает
минимуму поверхностной энергии жидкости,
т.е. ее устойчивому равновесному
состоянию. В случае достаточно больших
масс жидкости действие поверхностного
натяжения компенсируется силой тяжести,
поэтому маловязкая жидкость быстро
принимает форму сосуда, в который она
налита, а ее своб. поверхность представляется
практически плоской.
 В
случае смачивания, например, при
соприкосновении жидкости с твердой
стенкой сосуда, силы притяжения,
действующие между молекулами твердого
тела и жидкости, заставляют ее подниматься
по стенке сосуда, вследствие чего
примыкающий к стенке участок поверхности
жидкости принимает вогнутую форму. В
узких каналах, например, цилиндрических
капиллярах, образуется вогнутый мениск
- полностью искривленная поверхность
жидкости (рис. 1).
В
случае смачивания, например, при
соприкосновении жидкости с твердой
стенкой сосуда, силы притяжения,
действующие между молекулами твердого
тела и жидкости, заставляют ее подниматься
по стенке сосуда, вследствие чего
примыкающий к стенке участок поверхности
жидкости принимает вогнутую форму. В
узких каналах, например, цилиндрических
капиллярах, образуется вогнутый мениск
- полностью искривленная поверхность
жидкости (рис. 1).
Рис. 1. Капиллярное поднятие на высоту h жидкости, смачивающей стенки капилляра радиуса r; q - краевой угол смачивания.
