
- •Предисловие
- •4 Практикум по фармакогнозии
- •6 Практикум по фармакогнозии
- •Условные сокращения
- •8 Введение
- •1 0 Введение
- •Монография на лекарственное растительное сырье в PhEur.
- •1 2 Введение
- •1 4 Введение
- •Фармакогностические методы анализа
- •Общие требования к фармакогностическому анализу
- •1 6 Введение
- •1 8 Введение
- •Растворители, часто применяемые в фитохимическом анализе
- •2 2 Введение
- •Хроматографические методы фармакогностического анализа
- •2 6 Введение
- •2 8 Тема 1. Определение подлинности растительного сырья
- •Работа в лаборатории
- •Листья — Folia (гф хi, вып.1, с. 252)
- •Цветки — Flores (гф хi, вып. 1, с. 257)
- •Контрольные вопросы
- •Микроскопический анализ лрс
- •3 2 Тема 1. Определение подлинности растительного сырья
- •3 4 Тема 1. Определение подлинности растительного сырья
- •Работа в лаборатории
- •3 6 Тема 1. Определение подлинности растительного сырья
- •Контрольные вопросы
- •Соединения с гликозидной связью: полисахариды и гликозиды
- •4 0 Тема 2. Соединения с гликозидной связью: полисахариды и гликозиды
- •4 4 Тема 2. Соединения с гликозидной связью: полисахариды и гликозиды
- •Контрольные вопросы
- •Макро? и микроскопический анализ лрс, содержащего полисахариды
- •Корни алтея — Radices Althaeae
- •4 8 Тема 2. Соединения с гликозидной связью: полисахариды и гликозиды
- •Основные отличия алтея лекарственного и алтея армянского
- •5 0 Тема 2. Соединения с гликозидной связью: полисахариды и гликозиды
- •Трава алтея лекарственного — Herba Althaeae officinalis
- •Листья подорожника большого — Folia Plantaginis majoris
- •Семена подорожника блошного — Semina Psyllii
- •Листья мать?и?мачехи — Folia Farfarae (Folia Tussilaginis farfarae)
- •5 8 Тема 2. Соединения с гликозидной связью: полисахариды и гликозиды
- •Семена льна — Semina Lini (Semina Lini usitatissimi)
- •6 0 Тема 2. Соединения с гликозидной связью: полисахариды и гликозиды
- •Слоевища ламинарии (морская капуста) — Thalli Laminariae
- •Ные, волнистые.
- •Контрольные вопросы
- •Анализ жирных масел
- •6 6 Тема 3. Липиды
- •7 2 Тема 3. Липиды
- •7 4 Тема 3. Липиды
- •Приготовление смеси веществ, применяемых для калибровки*
- •7 6 Тема 3. Липиды
- •Контрольные вопросы
- •8 0 Фенольные соединения. Тема 4. Простые фенолы и их производные
- •Листья брусники — Folia Vitis idaeaе
- •Трава фиалки — Herba Violae
- •8 8 Фенольные соединения. Тема 4. Простые фенолы и их производные
- •Корневища и корни родиолы розовой — Rhizomata et radices Rhodiolae roseae
- •9 0 Фенольные соединения. Тема 4. Простые фенолы и их производные
- •Кора ивы — Cortex Salicis
- •9 2 Фенольные соединения. Тема 4. Простые фенолы и их производные
- •Трава эхинацеи пурпурной — Herba Echinaceae purpureae
- •Корневища щитовника мужского (папоротника мужского) — Rhizomata Filicis maris
- •9 4 Фенольные соединения. Тема 4. Простые фенолы и их производные
- •Контрольные вопросы
- •Кумарины
- •9 8 Фенольные соединения. Тема 5. Кумарины
- •Химический анализ лрс, содержащего кумарины
- •1 0 2 Фенольные соединения. Тема 5. Кумарины
- •Плоды амми большой — Fructus Ammi majoris
- •1 0 4 Фенольные соединения. Тема 5. Кумарины
- •Плоды пастернака — Fructus Pastinacae sativae
- •Корневища с корнями дудника обыкновенного — Rhizomata cum radicibus Angelicae
- •1 0 6 Фенольные соединения. Тема 5. Кумарины
- •Листья смоковницы обыкновенной (инжира) — Folia Fici caricae
- •1 0 8 Фенольные соединения. Тема 5. Кумарины
- •Хромоны
- •1 1 0 Фенольные соединения. Тема 6. Хромоны
- •1 1 2 Фенольные соединения. Тема 6. Хромоны
- •25 Мл раствора фильтруют и измеряют оптическую плотность на фото-электроколориметре в кювете с толщиной слоя 10 мм при длине волны 465 нм.
- •Контрольные вопросы к темам «кумарины и хромоны»
- •Ксантоны и лигнаны
- •1 1 6 Фенольные соединения. Тема 7. Ксантоны и лигнаны
- •1 1 8 Фенольные соединения. Тема 7. Ксантоны и лигнаны
- •5 Мл элюата прибавляют 5 мл спиртового раствора алюминия хлорида
- •Плоды расторопши — Fructus Silybi
- •1 2 0 Фенольные соединения. Тема 7. Ксантоны и лигнаны
- •Корневища и корни элеутерококка — Rhizomata et radices Eleutherococci
- •Корневища с корнями подофилла — Rhizomata cum radicibus Podophylli
- •1 2 4 Фенольные соединения. Тема 7. Ксантоны и лигнаны
- •Контрольные вопросы
- •Флавоноиды
- •1 2 6 Фенольные соединения. Тема 8. Флавоноиды
- •1 2 8 Фенольные соединения. Тема 8. Флавоноиды
- •1 3 0 Фенольные соединения. Тема 8. Флавоноиды
- •Контрольные вопросы
- •Макро? и микроскопический анализ лрс, содержащего флавоноиды
- •Бутоны софоры японской — Alabastrae Sophorae japonicae
- •Отличительные признаки софоры японской и сходных видов
- •Плоды софоры японской — Fructus Sophorae japonicae
- •1 См, шириной 0,4—0,7 см; большая часть семян недоразвита. Запах отсут-ствует. Вкус горький.
- •Цветки василька синего — Flores Centaureae cyani
- •1 3 6 Фенольные соединения. Тема 8. Флавоноиды
- •Плоды аронии черноплодной свежие — Fructus Aroniae melanocarpae recentes
- •Трава пустырника — Herba Leonuri
- •1 3 8 Фенольные соединения. Тема 8. Флавоноиды
- •Отличительные признаки видов пустырника и сходных видов
- •Трава горца перечного (водяного перца) — Herba Polygoni hydropiperis
- •Отличительные признаки горца перечного и сходных с ним видов
- •Трава горца почечуйного — Herba Polygoni persicariae
- •Трава горца птичьего (спорыша) — Herba Polygoni avicularis
- •1 4 6 Фенольные соединения. Тема 8. Флавоноиды
- •Трава сушеницы топяной — Herba Gnaphalii uliginosi
- •1 4 8 Фенольные соединения. Тема 8. Флавоноиды
- •Цветки бессмертника песчаного — Flores Helichrysi arenarii
- •Цветки пижмы — Flores Tanaceti
4 4 Тема 2. Соединения с гликозидной связью: полисахариды и гликозиды
Образовавшиеся в результате гидролиза сахара восстанавливают реактив Фелинга с образованием осадка меди (I) оксида. В спиртовом извлечении из листьев ландыша содержатся свободные сахара в количестве, недостаточном для окислительно-восстановительной реакции.
Пронаблюдайте за образованием осадка и запишите в лабораторный журнал его цвет.
Опыт 17. Ферментный гидролиз. Смочите горчичник или горчичный по-рошок в фильтр-пакете водой с температурой 38—40 °С. Приложите пакет или горчичник к руке в области запястья.
Отметьте появление через некоторое время запаха горчичного эфирного масла
раздражение кожи. Запишите химизм энзиматического гидролиза синигрина в лабораторный журнал:
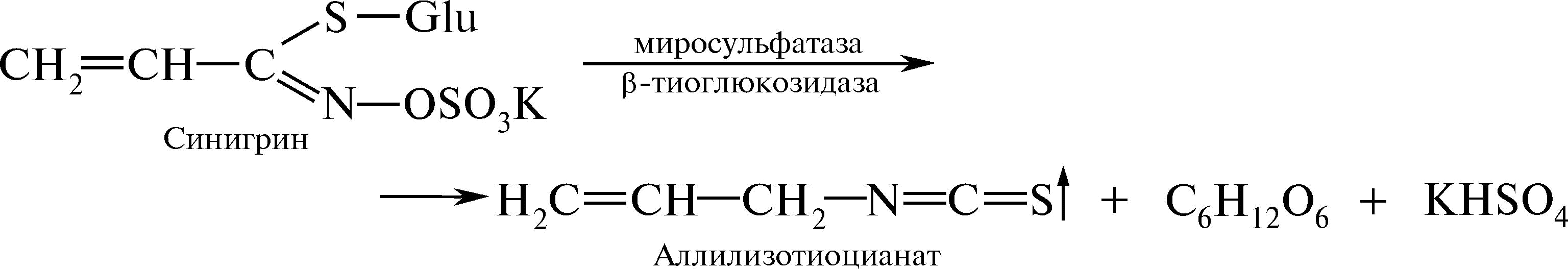
Задание 3. Выделите полисахариды из лекарственного растительного сырья.
Для выполнения задания используют извлечение, которое получают
процессе количественного определения полисахаридов в листьях подорож-ника.
Методика (ст. 20 ГФ ХI). Аналитическую пробу сырья измельчают до час-тиц, проходящих сквозь сито с отверстиями диаметром 2 мм. Около 10 г (точная навеска) измельченного сырья помещают в колбу со шлифом вмес-тимостью 250 мл, прибавляют 200 мл воды, колбу присоединяют к обрат-ному холодильнику и кипятят при перемешивании на электрической плитке в течение 30 мин. Экстракцию повторяют еще 2 раза, используя пер-вый раз 200 мл, второй раз — 100 мл воды. Водные извлечения объединяют, центрифугируют с частотой вращения 5000 об/мин в течение 10 мин, де-кантируют в мерную колбу вместимостью 500 мл через 5 слоев марли, вложенной в стеклянную воронку диаметром 55 мм и предварительно про-мытой водой. Фильтр промывают водой и доводят объем раствора водой до метки (раствор А).
25 мл раствора А помещают в колбу вместимостью 200 мл, прибавляют
75 мл 96 %-ного спирта, перемешивают, подогревают на водяной бане в те-чение 3 мин для лучшей коагуляции осадка. Появляются хлопьевидные сгус-тки, которые образуют осадок при отстаивании. Осадок представляет собой сложный комплекс полисахаридов, связанных с белками и минеральными веществами.
Осадок фильтруют через бумажный фильтр и делят на две части для об-наружения восстанавливающих и кислых моносахаридов.
Задание 4. Установите качественный моносахаридный состав полисахари дов. Результаты реакции и вывод запишите в лабораторный журнал. Подумайте, почему реакция на восстанавливающие сахара проводится после гидролиза по лисахаридов.
Опыт 18. Обнаружение восстанавливающих моносахаридов. Половину осад-ка (см. задание 3) переносят в колбу вместимостью 25 мл, перемешивают
Химический анализ ЛРС, содержащего соединения с гликозидной связью |
4 5 |
|
|
|
|
|
|
|
5 мл кислоты хлористоводородной разведенной (или 10 мл 10 %-ного рас-твора кислоты серной) и нагревают на водяной бане в течение 20 мин. К охлажденному гидролизату прибавляют 10 мл реактива Фелинга и нагре-вают на водяной бане в течение 5 мин. Появляется кирпично-красный осадок меди (I) оксида.
Опыт 19. Обнаружение кислых моносахаридов. Вторую часть осадка рас-творяют в 5 мл 0,1 моль/л раствора натрия гидроксида. К 1 мл полученного раствора прибавляют 0,25 мл 0,5 %-ного раствора карбазола и 5 мл кислоты серной концентрированной, перемешивают и нагревают на кипящей водя-ной бане в течение 10 мин.
Появляется красно-фиолетовая окраска при наличии кислоты галактуро-новой или глюкуроновой.
Реактив. 0,5 г карбазола растворяют в очищенном 95 %-ном спирте в мерной кол-бе вместимостью 100 мл и доводят объем раствора этим же спиртом до метки.
Задание 5. Проведите хроматографический анализ моносахаридов в семе нах подорожника блошного методом, описанным для семян подорожника исфагу ла — Plantago isphagula (Plantago ovata) и адаптированным к лабораторным заня тиям. Зарисуйте схему хроматограммы, рассчитайте величину Rf моносахаридов, сделайте заключение.
Методика. 10 мг порошка семян подорожника (сито 355) помещают
ампулу, прибавляют 5 мл (230 г/л) раствора кислоты трихлоруксусной и перемешивают. Ампулу запаивают и нагревают смесь в сушильном шкафу при 120 °С в течение 1 ч. Гидролизат центрифугируют, переносят надосадоч-ную жидкость в колбу вместимостью 50 мл, прибавляют 10 мл воды и выпа-ривают раствор под вакуумом до сухого остатка (азеотропная перегонка). Рас-творяют осадок в 10 мл воды и снова выпаривают под вакуумом досуха. Ра-створяют остаток в 2 мл спирта.
Приготовление растворов стандартных образцов: 10 мг арабинозы раство-ряют в минимальном количестве воды и приливают к 10 мл спирта. Так же готовят стандартные образцы ксилозы и галактозы.
На линию старта хроматографической пластинки размером 7×15 см, по-крытой слоем силикагеля, наносят по 10 мкл гидролизата и растворов стан-дартных образцов арабинозы, ксилозы и галактозы. Пластинку помещают
камеру со смесью растворителей вода—ацетонитрил (15 : 85) и хроматогра-фируют. Когда фронт растворителей пройдет 15 см от линии старта, пластин-ку вынимают, высушивают на воздухе, обрабатывают реактивом и нагревают
сушильном шкафу при 100 °С в течение 5 мин. Анализируют при дневном свете.
гидролизате семян подорожника обнаруживают два красноватых пятна (арабиноза и ксилоза) и желтое пятно (галактоза), совпадающих с пятнами стандартных образцов.
Реактивы: 3 г кислоты фталевой и 0,3 г кислоты аминогиппуровой растворяют
100 мл спирта; или 1,23 г n-анизидина (анилина) и 1,66 г кислоты фталевой раство-ряют в 100 мл спирта.
Задание 6. Определите количество полисахаридов в листьях подорожника большого гравиметрическим методом, используя извлечение, полученное при выполнении задания 3. Произведите расчет, сравните результат с требованиями АНД. Сделайте заключение о доброкачественности анализируемого образца листьев подорожника.
4 6 Тема 2. Соединения с гликозидной связью: полисахариды и гликозиды
Методика (ст. 20 ГФ ХI). 25 мл раствора А, полученного при выполнении задания 3, помещают в центрифужную пробирку, прибавляют 75 мл 96 %-ного
спирта, перемешивают, подогревают на водяной бане до 30 °С в течение
5 мин. Через 1 ч содержимое центрифугируют с частотой вращения
5000 об/мин в течение 30 мин. Надосадочную жидкость фильтруют под вакуумом при остаточном давлении 13—16 кПа через высушенный до посто-янной массы при температуре 100—105 °С стеклянный фильтр ПОР 16 диа-метром 40 мм. Осадок количественно переносят на фильтр и последовательно промывают 15 мл раствора 96 %-ного спирта в воде (3:1), 10 мл ацетона, 10 мл этилацетата. Фильтр с осадком высушивают сначала на воздухе, затем при температуре 100—105 °С до постоянной массы.
Содержание полисахаридов в пересчете на абсолютно сухое сырье Х, %, вычисляют по формуле
(m2 – m1) · 500 · 100 · 100
Х = ———————————————,
m · 25 · (100 – W)
где m1 — масса фильтра, г;
2 — масса фильтра с осадком, г;
— масса сырья, г;
W — потеря в массе при высушивании сырья, %.
?

