- •Теорія будови органічних сполук бутлерова
- •Характеристики ковалентного зв’язку
- •Вуглеводні
- •Лабораторні методи
- •Хімічні властивості алканів
- •Радикально-ланцюговий мехнізм
- •Хімічні властивості
- •1,2 Буде 80% 20%
- •Етери. Прості ефіри. R-o-r
- •Альдегіди і кетони
- •Методи одержання
- •Оксосинтез
- •Хімічні властивості альдегідів і кетонів
- •Утворення ацеталів (взаємодія із спиртами):
- •Окиснення карбонільних сполук
- •Реакція «срібного дзеркала»:
- •Карбонові кислоти
- •Хімічні властивості карбонових кислот
- •Функціональні похідні карбонових кислот
- •Методи добування хлорангідридів
- •Принцип мікроскопічної зворотності
- •Ненасичені двохосновні карбонові кислоти
- •Добування
- •Оксокислоти
- •Вуглеводи
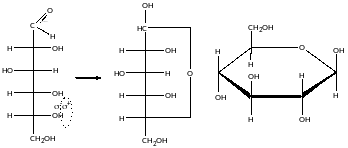
- •Утворення напівацеталей:
- •Бродіння глюкози
- •Дисахариди
- •Для сірчаної кислоти (80%) на нітросполуки
- •Реакція Неффе утворюється ацеформа
- •Методи добування
- •Амінокислоти
- •Методи добування
- •Ізомерія
- •Номенклатура
- •Хімічні властивості фенолів
- •Хімічні властивості
- •Хімічні властивості
Оксокислоти
(де є карбонільна група)

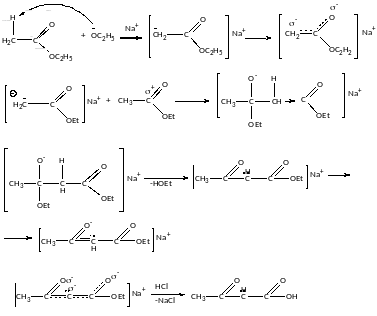
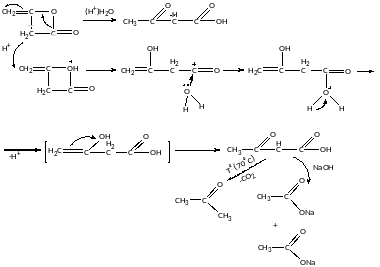
Механізм конденсації Кляйзена:
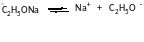
Вуглеводи
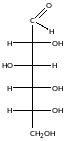
Вуглеводи Cn(H2O)m – природні сполуки, які є полігідроксикетонами та полігідроксиальдегідами, а також продукти їх конденсації.

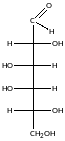
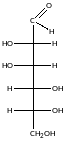
Відносяться до альдоз |
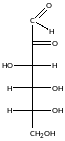
До кетоз |
||
|
|
|
|
D-глюкоза |
D-галактоза |
D-маноза |
D-фруктоза |
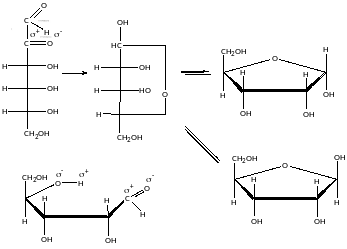
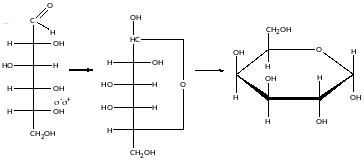
Вуглеводні здатні утворювати циклічні форми.
Утворення напівацеталей:
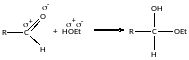
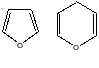 5-членний
цикл – фураноз ний
5-членний
цикл – фураноз ний
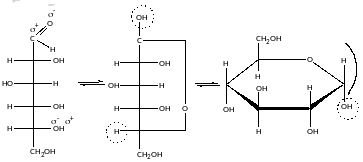
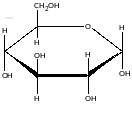
Ізомери, які відрізняються розташуванням глікозидного гідроксилу називаютьяс аномерами.
В речовині відкритої форми 0, 002%, β-форми – 64%, α-форми – 36%.
Мутаротація – зміна кута обертання площини плоскополяризованого світла при проходженні через розчин аномера. Цей кут α=53◦.
Фуранозний:
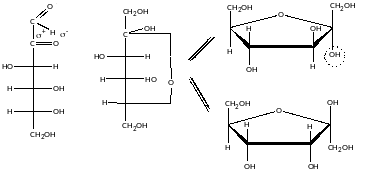 D-рибоза
D-рибоза
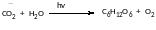
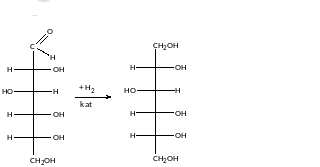
Добувають гідролізом крохмалю:

Окиснення:
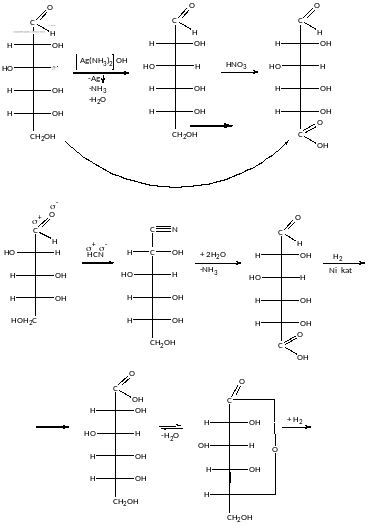
Зменшення ланцюга з гексоз до пентоз:
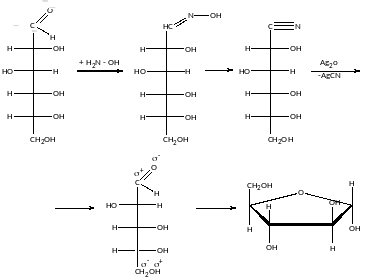
Епімери – ізомери, які відрізняються конфігурацією першого асиметричного атома С.
Епімеризація відбувається в лужних розчинах:

Взаємодія з феніл-гідразином:
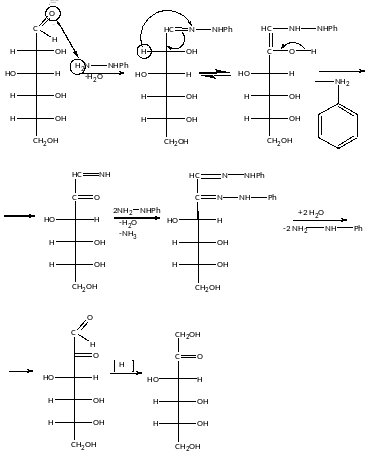
Озазон за звичайних умов існує в кристалічному вигляді і застосовується для ідентифікації вихідних речовин.
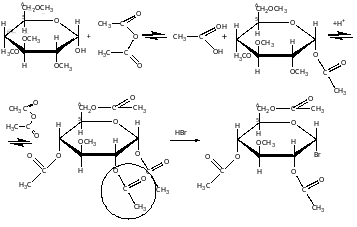
Алкілування глюкози:
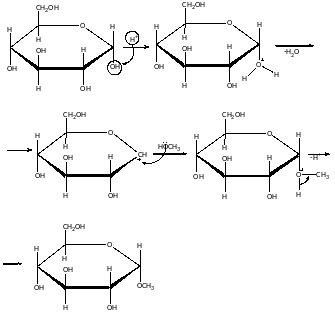
При гідролізі в м’яких умовах спочатку гідролізується група:
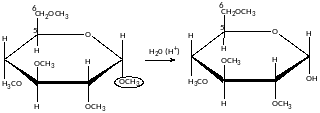

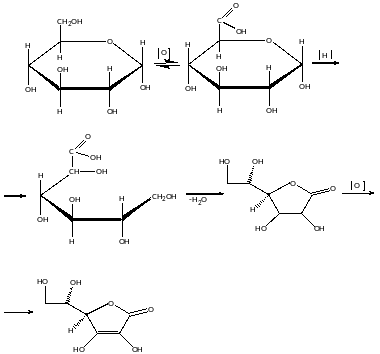
Вітамін С
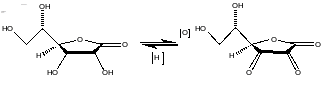
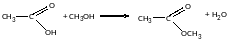
Бродіння глюкози
Анаеробне бродіння
Молочно-кисле
Спиртове
Гліцеринове
Бутиратно-кисле
Пропіонове
Ацетоново-бутанове
Реакція утворення ацеталів:


Дисахариди
Відновлюючи (ті, що вступаютьвреакції окиснення)
Невідновлюючі
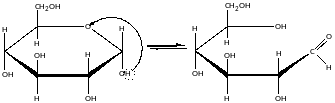
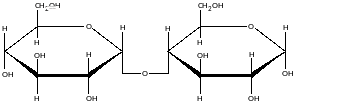
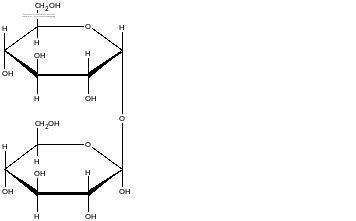
Невідновлюючі
Сахароза утворена залишками α-D-глюкози і β-D-фруктози. Не дає реакцію срібного дзеркала.

Відновлюючі дисахариди
Мальтоза
– з залишків 1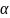 -
D
– глюкози(глікозидний гідроксил) і 1
-
D
– глюкози(глікозидний гідроксил) і 1
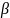 -
D
– глюкози(по 4 положенню)
-
D
– глюкози(по 4 положенню)

Метилювання
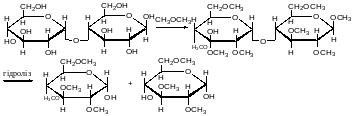
Мальтоза є проміжний продуктом при гідролізі крохмалю.
Целобіоза
Приймає участь в реакції срібного дзеркала, утворює залишки - D – глюкози (1 гідрокс; утв пол. 4).

Є проміжним продуктом при гідролізі целюлози. Всі властивості характерні для відновлюючих дисахаридів.
Лактоза
–
залишками
-
D
– галактози і
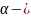 D
– глюкози.
D
– глюкози.

Відновлюючий дисахарид(для нього характерні реакції): метилювання, реакція срібного лзеркала.
ПОЛІСАХАРИДИ
Крохмаль,целюлоза,глікоген. Крохмаль складається з амілози і амілопектину.

1,4 – амілоза з - D – глюкози
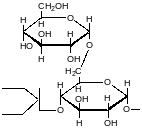
Целюлоза утворює залишки - D – глюкози(метилювання, нітрування, ацелювання).

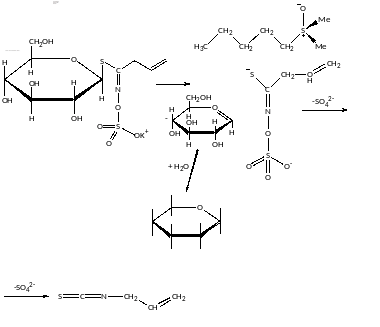
Віскоза утворюється:
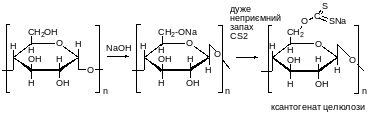
АЗОТОВМІСНІ СПОЛУКИ. Нітросполуки
 R
– O
– N
= O
(похідне нітритної кислоти HNO2)
R
– O
– N
= O
(похідне нітритної кислоти HNO2)
семіполярний зв’язок(утворюється спільною парою
електронів і додатково зв’язується потилежними зарядами)
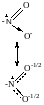
Tут
були часткові заряди( )
)
СH3 – CH2 – NO2
Первинні нітросполуки – коли NO2 приєднується до первинного атома С .
 –
вторинні
і третинні.
–
вторинні
і третинні.
Відрізняються нітросполуки від естеру нітритної кислоти
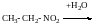 нітроетан
нітроетан
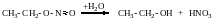 етиловий
естер нітритної кислоти
етиловий
естер нітритної кислоти
Реакції відновлення(взаємодія з воднем на каталізаторі)

ДОБУВАЮТЬ
реакцією Коновалова
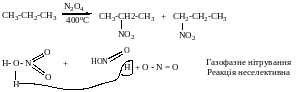

При заміні первинних галогенах на NO2 утворюються нітросполуки за механізмом SN2 . Коли третинне галогенпохідне – первинний утворює естер нітритної кислоти.
SN1
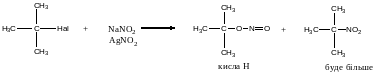
ХІМІЧНІ ВЛАСТИВОСТІ
1)Реакція відновлення – утворються аміни
2)Утворення ациформи (коли відбувається таутомеризація за рахунок перемішування атома водню)
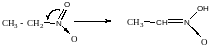
Взаємодія з NaOH - характерна для кислот.
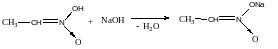
В лугах розчиняються первинні і вторинні нітросполуки через утворення солей відповідних ацеформ. У третинних немає атома Н біля атома С – вони в лугах не розчиняються.
Кисень – більш дорстка основа.
М’яка з м’якою, жорстка з жорсткою.

Ацеформа