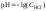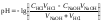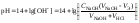- •Кислотно-основное титрование
- •Действие индикаторов
- •Кривые титрования
- •Кривая титрования сильной кислоты щёлочью
- •Кривая титрования сильного основания кислотой
- •Кривая титрования слабой одноосновной кислоты щёлочью
- •Кривая титрования слабого однокислотного основания сильной кислотой
- •Кривая титрования слабой многоосновной кислоты
- •Кривая титрования смеси сильной и слабой кислот
- •Кривая титрования раствора соли слабого электролита
Кислотно-основное титрование
Аналитическая реакция – нейтрализация кислоты щёлочью или, наоборот, щёлочи кислотой. Эквивалентную точку определяют обычно с помощью цветных индикаторов.
Действие индикаторов
Индикаторами являются слабые органические кислоты или основания, у которых ионная и молекулярная формы имеют различную окраску. Например, фенолфталеин содержит фенольную функциональную группу, метилоранж – ароматическая сульфокислота с функциональной группой SO3H. Процесс их диссоциации в общем виде можно представить уравнением:
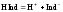 .
.
Константа диссоциации индикатора определяется уравнением:
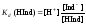 .
.
Концентрации ионной и молекулярной форм в середине области перехода окраски индикатора равны между собой и рН перехода окраски индикатора равен логарифму константы диссоциации:
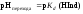 .
.
При
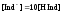 цвет раствора будет обусловлен окраской
ионной формы индикатора и, наоборот,
при
цвет раствора будет обусловлен окраской
ионной формы индикатора и, наоборот,
при
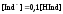 раствор будет окрашен молекулярной
формой индикатора. Поэтому переход
окраски происходит в области
раствор будет окрашен молекулярной
формой индикатора. Поэтому переход
окраски происходит в области
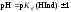 .
.
Фенолфталеин является очень слабой кислотой, поэтому он изменяет окраску от бесцветной к малиновой в слабощелочной области, при рН = 8,3 – 10. Метиловый оранжевый – кислота средней силы, изменяет окраску от красной к жёлтой в слабокислой области при рН = 3,7 – 5,1. Лакмус изменяет окраску от красной к синей в нейтральной области при рН около 7.
Кривые титрования
Кривые титрования – графические зависимости концентрации участника реакции, протекающей при титровании от объёма добавленного титранта. Для реакций кислотно-основного взаимодействия показателем концентрации участника реакции является рН раствора.
Различают теоретические и экспериментальные кривые титрования. Теоретический расчёт кривых титрования проводится по уравнению реакции и исходным концентрациям реагирующих веществ. Теоретические кривые титрования нужны для обоснованного выбора индикатора в данном титровании. Экспериментальные кривые титрования получают при измерении какого-либо свойства системы в ходе титрования (ЭДС, электропроводность и т.п.) в зависимости от объёма титранта. Экспериментальные кривые титрования нужны для определения точки эквивалентности.
Кривые кислотно-основного титрования позволяют проследить за качественными и количественными изменениями титруемого раствора и выбрать наиболее подходящий индикатор для определения точки эквивалентности (конца титрования).
При построении теоретических кривых титрования рассчитывают рН четырёх основных этапов:
1) до начала титрования;
2) титрование до точки эквивалентности;
3) точка эквивалентности;
4) после точки эквивалентности.
Кривая титрования сильной кислоты щёлочью
Аналитическая реакция – реакция нейтрализации
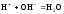 .
.
1 этап. В растворе присутствует только сильная кислота, рН раствора определяется её концентрацией:
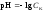 ,
,
где СK – нормальная концентрация кислоты.
2 этап. Процесс титрования. Происходит постепенная нейтрализация кислоты щёлочью:
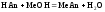 .
.
рН вычисляется по уравнению:
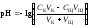 ,
,
где VK – объём пробы кислоты, взятый для титрования (аликвота), СЩ – нормальная концентрация раствора щёлочи, VЩ – объём раствора щёлочи, добавленного в процессе титрования.
3 этап. Точка эквивалентности. В системе находится только негидролизующаяся соль. рН = 7. На нейтрализацию кислоты затрачен эквивалентный объём щелочи VЭ.
4 этап. Добавление избытка титранта после точки эквивалентности. рН определяется только количеством добавленной щёлочи и вычисляется по уравнению:
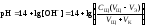 .
.
Пример. Рассчитать кривую титрования 10 мл 0,1 н. соляной кислоты 0,1 н. раствором гидроксида натрия.
|
VNaOH, мл |
Система |
Расчётная формула |
рН |
|
0 |
0,1 н. раствор HCl |
|
1,00 |
|
1 |
Титрование соляной кислоты. |
|
1,09 |
|
5 |
1,48 |
||
|
7 |
1,75 |
||
|
9 |
2,28 |
||
|
9,5 |
2,59 |
||
|
9,9 |
3,30 |
||
|
10 |
NaCl |
Точка эквивалентности, VЭ = 10 мл, VΣ = 20 мл |
7,00 |
|
10,1 |
Избыток щёлочи |
|
10,70 |
|
11 |
11,68 |
||
|
12 |
11,96 |
||
|
15 |
12,30 |
||
|
20 |
12,52 |
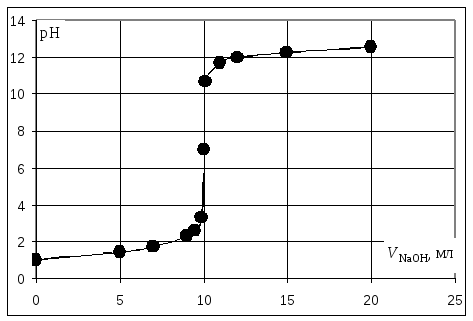
Кривая титрования сильной кислоты щелочью
Точка эквивалентности соответствует объёму титранта 10 мл. Обращает внимание резкий скачок величины рН в этой области. Объём одной капли раствора обычно составляет 0,01-0,02 мл. В области эквивалентной точки при добавлении капли щёлочи рН возрастает на 3-6 единиц. Поэтому эквивалентную точку можно определить с помощью любого цветного индикатора, изменяющего окраску в области значений рН от 4 до 10.