
- •2. Наземные экосистемы как источник и сток парниковых газов.
- •3. Биологический цикл азота.
- •Азотфиксация
- •Нитрификация
- •Денитрификация
- •4. Таксономическое разнообразие микроорганизмов цикла азота, осуществляемые ими процессы и продукты реакций.
- •5. Условия протекания процессов в экосистемах.
- •6. Таксономическое разнообразие микроорганизмов цикла углерода, осуществляемые ими процессы и продукты реакций.
- •7. Условия протекания процессов в экосистемах.
- •Процесс разложения растительных остатков и формирование подстилки
- •Образование и разложение гумуса
- •Участие почв-х мо в разрушении и новообразовании минералов
- •8. Микробная трансформация углерода и азота в почвенных агрегатах.
- •9. Формирование анаэробных зон внутри почвенных агрегатов.
- •10. Влияние размера почвенных агрегатов на продукты микробного метаболизма.
- •11. Участие микроорганизмов в «парниковом эффекте».
- •17. Постулат Бейеринка, Правило Гаузе, Триада Гузева.
- •18. Экологические (функциональные) и филогенетические классификации почвенных микроорганизмов.
- •19. Вертикальная ярусность микробов и их функции в различных экосистемах (бгц).
- •20. Филогенетическая структура метаболически активных прокариот в пространственно-сукцессионном (вертикально-ярусном) ряду.
- •2. Свойства покоящихся клеток.
- •3. Пролиферативный и метаболический покой.
- •4. Репродуктивные покоящиеся формы микроорганизмов.
- •5. Этапы формирования покоящихся форм.
- •6. Механизмы катаболитной репрессии и репрессии конечным продуктом.
- •7. Роль микроорганизмов в формировании и разложении почвенного гумуса.
- •8. Автохтонная и зимогенная микрофлора.
- •9. Микробная популяция как многоклеточный организм.
- •10. Экологическая роль антибиотиков в почве.
- •11. Примеры микробных сукцессий в почве.
- •2. Полифазная таксономия.
- •3. Основные филумы домена Bacteria и Archaea, обнаруживающиеся в почве.
- •2. Строение бактериофагов и их геном.
- •3. Генетический аппарат эукариотических микроорганизмов (грибов).
- •4. Лизогения у бактерий. Специфическая трансдукция: особенности и механизмы.
- •5. Конъюгация у бактерий.
- •6. Сравнительные особенности процесса конъюгации у разных типов бактерий.
- •7. Плазмиды и мигрирующие элементы.
- •8. Биологическое значение плазмид и мигрирующих элементов в изменчивости и эволюции микроорганизмов.
- •9. Сообщества бактерий – биопленки: их структура, экспрессия бактериальных генов в состоянии биопленок.
- •Фототрофы
- •Хемосинтез
- •2. Миксотрофия.
- •4. Современные представления о роли микроорганизмов в образовании и разрушении глинистых (почвообразующих, вторичных) минералов.
- •5. Роль микроорганизмов в образовании и деградации гумусовых веществ, основные группы организмов, механизмы процессов.
- •6. Понятие о «затравочном» эффекте.
- •7. «Вторая (подземная) биосфера» принципы ее функционирования.
- •8. Микробное фракционирование стабильных изотопов в природе.
- •9. Основные методы изучения геохимической деятельности микроорганизмов.
- •10. Современные биогеотехнологии с использованием микроорганизмов.
- •2. Микроорганизмы и ксенобиотики.
- •3. Почвы, загрязненные нефтью и нефтепродуктами.
- •4. Биологическая индикация загрязнения почвенной среды, самоочищение и самовосстановление почв, санитарное почвоведение.
- •5. Микроорганизмы почв и современные почвенные биотехнологии.
- •6. Микроорганизмы и охрана почв.
- •2. Современные методы, направленные на определение видового и функционального разнообразия почвенного микробного сообщества.
- •3. Методы для определения биомассы почвенных микроорганизмов.
Оглавление.
1. Микробная трансформация азота
2. Гидролитическая деятельность почвенных микроорганизмов
3. Основы биологической систематики
4. Генетика микроорганизмов
5. Геохимическая деятельность микроорганизмов
6. Почвенная биотехнология
7. Современные методы биологии почв
1. Микробная трансформация азота.
Содержание.
1. Цикл углерода в почвах
2. Наземные экосистемы как источник и сток парниковых газов
3. Биологический цикл азота
4. Таксономическое разнообразие микроорганизмов цикла азота, осуществляемые ими процессы и продукты реакций
5. Условия протекания процессов в экосистемах
6. Таксономическое разнообразие микроорганизмов цикла углерода, осуществляемые ими процессы и продукты реакций
7. Условия протекания процессов в экосистемах
8. Микробная трансформация углерода и азота в почвенных агрегатах
9. Формирование анаэробных зон внутри почвенных агрегатов
10. Влияние размера почвенных агрегатов на продукты микробного метаболизма
11. Участие микроорганизмов в «парниковом эффекте»
12. Специфика почвы как среды обитания микроорганизмов (гетерогенность)
13. Влияние почвенной воды, температуры и воздуха на развитие микроорганизмов
14. Экологическое значение адсорбции (адгезии) клеток микроорганизмов почвенными частицами
15. Активность адгезированных клеток
16. Экологические стратегии у микроорганизмов
17. Постулат Бейеринка, Правило Гаузе, Триада Гузева
18. Экологические (функциональные) и филогенетические классификации почвенных микроорганизмов
19. Вертикальная ярусность микробов и их функции в различных экосистемах (БГЦ)
20. Филогенетическая структура метаболически активных прокариот в пространственно-сукцессионном (вертикально-ярусном) ряду
1. Цикл углерода в почвах.
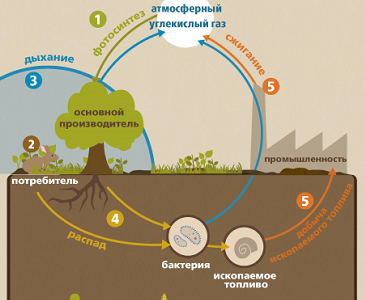
В атмосфере углерод в основном представлен С02, который составляет 0,03% от ее объема. В гидросфере его на порядок больше, но основным источником углекислого газа является почва (до 9-15% по Ремезову), т.к. здесь сосредоточена деятельность микроорганизмов, разлагающих органические остатки, и осуществляется дыхание растений. В совокупности данные процессы носят название «почвенного дыхания».
-
Растения используют атмосферный СО2 в процессе фотосинтеза, который становится входит в их состав и становится их частью.
-
Животные, питающиеся растениями, передают соединения углерода по пищевой цепи.
-
Большая часть углерода, потребляемого животными, в процессе их дыхания преобразуется в СО2 и возвращается в атмосферу.
-
Когда животные и растения погибают, бактерии и грибы, обитающие в почве, разлагают их остатки, и углерод вновь возвращается в атмосферу в виде СО2.
-
Некоторые органические остатки остаются в почве и превращаются в ископаемые виды топлива (нефть, уголь, газ, торф), при сжигании которых также СО2 возвращается в атмосферу. Гумус также является формой захоронения углерода.
-
В воде основным продуцентом СО2 являются водоросли. В морской воде углерод содержится в виде угольной кислоты и ее растворимых солей, но накапливается он в форме карбоната кальция СаС03 (мел, известняки, кораллы). Часть углерода в виде карбонатов надолго исключается из круговорота, образуя осадки на дне водоемов. Однако с течением времени в процессах горообразования осадочные массы поднимаются на поверхность в виде горных пород.
-
Также СО2 поступает в атмосферу в результате вулканической деятельности и с выхлопными газами машин, заводов.
В цикле углерода можно выделить два звена, имеющих планетарные масштабы и связанных с выделением и поглощением кислорода: 1) связывание С02 в процессе фотосинтеза и генерация кислорода; 2) минерализация органических веществ с выделением С02 и затратой кислорода. Первый осуществляют высшие растения, водоросли и цианобактерии. Второй – микроорганизмы.
2. Наземные экосистемы как источник и сток парниковых газов.

цию фотосинтеза.




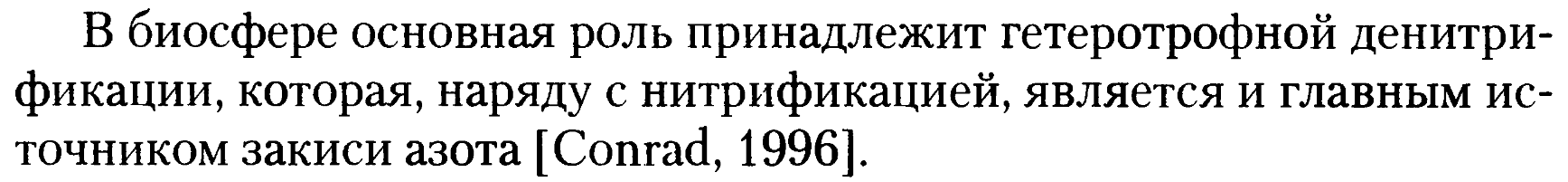
3. Биологический цикл азота.
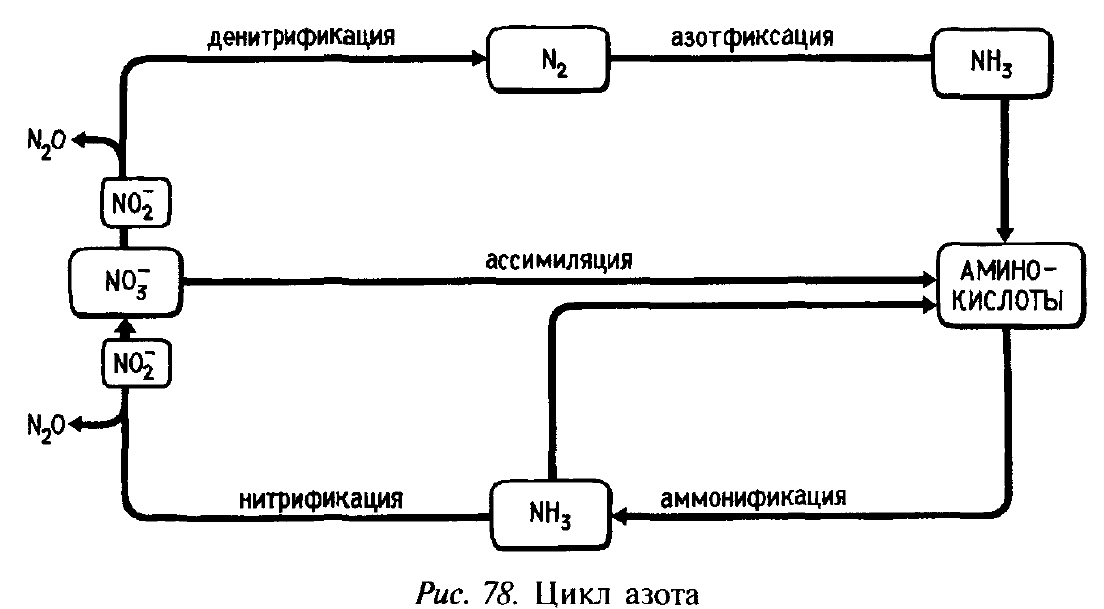
В цикле азот участвует в газообразной форме, в виде минеральных и органических соединений. При фиксации азота микроорганизмами происходит его восстановление до аммиака с последующим включением в аминокислоты; разложение органических азотсодержащих соединений (аммонификация) приводит к освобождению азота в форме аммиака, который далее окисляется последовательно до нитритов и нитратов (нитрификация). Окисленный азот вновь восстанавливается до N2 в процессе денитрификации. Аммонийные и нитратные формы соединений азота ассимилируются растениями и микроорганизмами, что приводит к временному закреплению азота в органических веществах, его иммобилизации в микробной биомассе. В процессах нитрификации и денитрификации возможны газообразные потери азота в форме его закиси — N20.
Азотфиксация
«Биологический азот» – азот, включенный в растения благодаря азотфиксации. Бактерии, которые связывают молекулярный азот – азотфиксаторы (диазотрофы). Растения используют азот из: минеральных форм, органических веществ – также и из гумуса после его разложения микроорганизмами и от бактерий азотфиксаторов, связывающих молекулярный азот, который в форме аммония и аминокислот поступает в клетки корня. В агроценозах растения дополнительно получают азот из вносимых в почву минеральных и органических удобрений. Доля биологического азота в урожае – 20-90%. Много N получают бобовые (симбиоз с клубеньковыми азотфиксаторами). Относительно вносимого N в с/х: метод Габера-Боша. Суть: синтез аммиака из молек. N и H на катализаторах при высоких температуре и давлении.
В
молекуле N тройная связь
(благодаря ей газообразный N
инертен). Чтобы N2 -> NH4,
нужно 225 ккал:
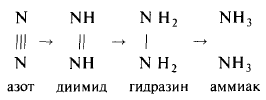
В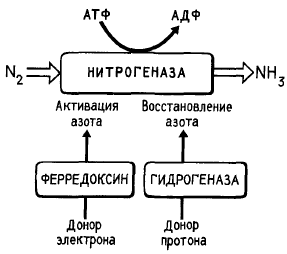 восстановлении N главную
роль играет фермент нитрогеназа. Активный
центр этого фермента состоит из комплекса
двух белков, содержащих железо, серу и
молибден в соотношении Fe : S : Mo = 6 : 8 : 1.
Выделена также ванадийсодержашая
нитрогеназа, уровень активности которой
на 30% ниже, чем у Мо-нитрогеназы.
восстановлении N главную
роль играет фермент нитрогеназа. Активный
центр этого фермента состоит из комплекса
двух белков, содержащих железо, серу и
молибден в соотношении Fe : S : Mo = 6 : 8 : 1.
Выделена также ванадийсодержашая
нитрогеназа, уровень активности которой
на 30% ниже, чем у Мо-нитрогеназы.
Азот, растворенный в воде, поступает в азотфиксирующий центр, где в его активации участвуют два атома молибдена. После взаимодействия с азотом молибден восстанавливается за счет электронов, поступающих в активный центр через Fe-белок и Mo-Fe-белок. Этот перенос сопряжен с реакцией разложения АТФ, т.е. он идет с затратой энергии. В передаче электронов нитрогеназе участвует железосодержащий водорастворимый белок — фермент ферредоксин, а в активации водорода воды и переносе протонов — фермент
гидрогеназа.
Образование нитрогеназы у бактерий связано с наличием особых nif-генов, содержащихся или в ядерной ДНК или в плазмиде, ответственной за синтез этих специфических ферментных белков. Гены диазотрофности консервативны. В то же время диазотрофы не встречаются среди эукариот. Долго не обнаруживали азотфиксаторов среди архебактерий. Однако в последнее время стало известно, что метаногены имеют особую термостабильную ферментную систему азотфиксации, отличную от термолабильной системы эубактерий. Т.е., хотя свойство фиксировать азот присуще многим организмам, оно ограничено только царством прокариот.
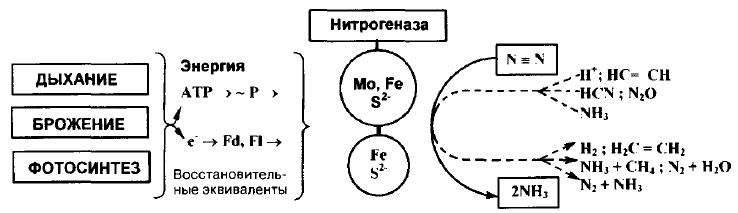 Строение
нитрогеназы
Строение
нитрогеназы
Среди бактерий-азотфиксаторов есть все типы метаболизма: 1) аэробы с дыхат-м энерг-им обменом; 2) анаэробы с брожением; 3) хемоорганотрофы; 4) автотрофы-фотосинтетики и 5) хемолитоавтотрофы. Для них фиксация N не обязательна: если есть минеральный или органический N, они используют этот связанный N. Важна концентрация O2: нитрогеназа подавляется молекулярным кислородом. У МО есть механизмы нитрогеназного комплекса от O2.
Примеры: аэробы (азотобактер) связывают кислород за счёт повышения уровня дыхания при азотфиксации. Чтобы быстро расходовать кислород, часть органических молекул сжигается «непроизводительно», т.е. окисление без запасания энергии. Еще мех-м защиты: конформационное изменение ферментных белков, которые чувствительны к O2, и эти белки связываются в стабильные комплексы с помощью FeS-белков. Цианобактерии: т.к. они выделяют O2 внутриклеточно, азотофиксация у них идет в нефотосинтезирующих гетероцистах, которые изолированы от O2. Клубеньковые бактерии: защищены от O2 тканью клубенька, а также имеют леггемоглобин, который транспортирует O2 для дыхания к бактероидам (грам «-») в менее активном связанном виде.
Азотфиксаторы
|
Свободноживущие |
Симбиотические |
|
|
Которые не связаны с корневыми системами непосредственно |
Ассоциативные, обитают в сфере прямого влияния растений; в ризосфере (почва, прилегающая к корням), в ризоплане (на пов-ти корней) и филлоплане (листьев). |
Которые живут в тканях растения, стимулируют образование клубеньков на корнях или листьев. |
Первый диазотроф нашел в (1898 г.) С.Н. Виноградский среди анаэробных маслянокислых бактерий рода Clostridium. Он назвал его в честь Пастера Clostridium pasteurianum. Вскоре (1901 г.) М. Бейеринк в Голландии выделил аэробный азотфиксатор, получивший за свою морфологию и цвет (кокковидные бактерии, колонии которых с возрастом темнеют до шоколадного цвета) название Azotobacter chroococcum.
Ассоциативная азотфиксация – накопление азота микроорганизмами, ассоциированными с продуцентами органики (растениями, водорослями, цианобактериями). Активность нитрогеназы у них высока, т.к. от фототрофов к МО идёт легкодоступные C и энергия с экссудатов листьев, корней, слизей цианобактерий, корневого отпада/опада. Связующее звено между фотосинтезом и азотфиксацией: прижизненные выделения органики корнями (сахара, орг. к-ты, полисахаридные слизи «муцигель» и др экссудаты). Поступление N не только активизирует диазотрофов, но и МО-разлагателей гумуса. Когда вносим N-удобрения, МО переходят от азотфиксации к связыанию (иммобилизации) р-римых форм N (и тут из-за денитрификации часть N2 теряется в атмосферу). Вывод: чем выше C:N, тем активнее азотфиксация; чем активнее фотосинтез, тем выше степень минерализации гумуса.
Пример ассоциативной азотфиксации у животных: род Escherichia как комменсалы в пищ. тракте человека (а также др позвоночных и беспозвоночных).
Симбиотическая азотфиксация – азотфиксирующие симбионты проникают в ткани растения и вызывают образ-я клубеньков на корнях, стеблях. Первым в чистую культуру бактерии из клубеньков выделил Бейеринк (из клевера, гороха, сои, люпина, люцерны – род бактерий Rhizobium).
-
Rhizobium, например Rhizobium leguminosarum bv trifolii (клевер), bv viceae (горох), bv meliloti (люцерна). Это быстрорастущие бактерии;
-
Sinorhizobium (вика, люцерна, соевые, у сесбании клубеньки образуются на стебле);
-
Mezorhizobium;
-
Bradyrhizobium, например Bradyrhizobium japonicum (соя). Это медленнорастущие бактерии.
Обозначение bv — биовариант (т.е. МО внутри вида различаются по биологич-м св-м). Гены азотфиксации располагаются на плазмиде, у других — на хромосоме. Благодаря азотфиксирующим симбионтам бобовые обогащают почву азотом. В зависимости от условий роста растений бобовые накапливают 60-300 кг N/га в год.
Роль клубеньковых в накоплении азота => надо использовать их для обработки семян бобовых перед посевом => созд-е препаратов. 1896 г, Германия – «нитрагин»; 1906 г – Англия, 1907г – США. Чехословакия – «нитразон», Австралия – «нитрофикс». Россия 1930-35 гг, первые партии нитрагина, называется «ризоторфин» (торфяной нитрагин). На 1га нужно 200 г ризоторфина.
Изготовление нитрагина: 1) выбор и выделение подходящего штамма, непосредственно из клубенька. Розовый клубенек (т.к. окрашен леггемоглобином) стерилизуют сулемой (или др. антисептиком), разрезают, извлекают растит.ткань и шпателем растирают в Петри.
Штамм должен обладать: 1) специфичностью к растению, 2) генетической устойчивостью, 3) доминировать (быстро размножаться и захватывать территорию у диких почвенных штаммов), 4) инвазивность (проникать в корни растений), 5) активность (к азотфиксации), 6) эффективность (повышать урожай). Редкие розовые клубеньки – всё удачно, много мелких белых – штамм не годится.
Аммонификация белков – внеклеточное расщепление белков до аминокислот. С помощью протеаз бактерий и грибов. Аминокислоты далее поступают в клетки МО или в хим. реакции почвы. В клетках аминокислоты: участвуют в синтезе белков, переаминируются, декарбоксилируются, дезаминируются (в последнем выделяется свободный NH3). Чем меньше C:N, тем эффективнее аммонификация.
Аммонификация нуклеиновых кислот с помощью внеклеточных ДНК-аз и РНК-аз. Аммонификация мочевины и мочевой к-ты с помощью уреаз. Аммонификация хитина (полимера ацетилглюкозамина) хитиназами. Продукты аммонификации: 1) потребляются МО как источник N, 2) иммобилизируются (ассимилируются), 3) окисляются в нитриты и нитраты.
