
Рекомендуемая литература:
Основная:
Харитонов, Ю.Я. Аналитическая химия (аналитика) / Ю.Я. Харитонов.- М.: Высшая школа, 2001.- Кн. 1.
Лекционный материал.
Дополнительная:
Харитонов Ю.Я. Практикум (электронный ресурс): учебное пособие/ Ю.Я. Харитонов, В.Ю. Григорьева, 2009.
Харитонов Ю.Я. Примеры и задачи по аналитической химии (электронный ресурс): учебное пособие/ Ю.Я. Харитонов, В.Ю. Григорьева, 2009.
Основы аналитической химии / под ред. Ю.А. Золотова.- М.: Высшая школа, 1999.- Кн. 1.
Основы аналитической химии / под ред. Ю.А. Золотова.- М.: Высшая школа, 1999.- Кн. 2.
Государственная фармакопея РФ ХII изд., часть 1, М., НЦЭСМП, М., 2007 г
Занятие № 11
Тема: Нитритометрия.
Цель изучения темы. Нитритометрия – титриметрический метод анализа, применяемый для количественного определения первичных и вторичных ароматических аминов, их ацилированных производных (после предварительного гидролиза), а также ароматических нитропроизводных, гидразидов и др. В основе нитритометрии лежат реакции диазотирования (при определении первичных ароматических аминов) и нитрозирования (вторичных ароматических аминов и гидразидов). Для проведения нитритометрического титрования необходимо знать титрант метода, условия проведения, определение конечной точки титрования. Знание методов нитритометрического титрования необходимо для дальнейшего изучения фармацевтической химии.
Задачи. Освоить метод нитритометрического титрования.
Студент должен знать:
1.до изучения темы
правила техники безопасности работы в химической лаборатории и с физической аппаратурой;
химические свойства элементов и их соединений;
растворы и процессы, протекающие в водных растворах;
основные начала термодинамики, термохимия;
химическое равновесие, способы расчета констант равновесия;
2.после изучения темы
основные законы, лежащие в основе окислительно-восстановительных методов титрования, нитритометрии;
методы, приемы и способы выполнения нитритометрического титрования;
Студент должен уметь:
проводить количественное определение веществ методом нитритометрического титрования.
Студент должен владеть:
простейшими операциями при выполнении нитритометрического титрования.
Задание для самостоятельной аудиторной работы студентов по указанной теме:
1) Ознакомиться с теоретическим материалом по теме занятия с использованием конспектов лекций, рекомендуемой учебной литературы.
2) Ответить на вопросы для самоконтроля:
Окислительные и восстановительные свойства нитрита натрия.
Нитритометрическое титрование. Сущность метода, химизм.
Титрант нитритометрии, его приготовление и стандартизация.
Определение конечной точки титрования в нитритометрии (инструментальными методами, визуально). Индикаторы метода: внешние (йодкрахмальная бумага), внутренние (тропеолин 00, нейтральный красный, смесь тропеолина 00 с метиленовым синим).
Условия проведения нитритометрического титрования: температура, среда, катализатор, скорость титрования.
Применение нитритометрии для определения веществ, содержащих первичную ароматическую аминогруппу. Химизм.
Применение нитритометрии для определения веществ, содержащих вторичную ароматическую аминогруппу. Химизм.
Применение нитритометрии для определения веществ, содержащих ароматическую нитрогруппу Химизм.
УИРС. Применение нитритометрии для определения гидразидов. Химизм.
3) Проверить свои знания с использованием тестового контроля:
1. Титрантом в методе нитритометрии является
А) перманганат калия
Б) йод
В) тиосульфат натрия
Г) бромат калия
Д) нитрит натрия
Ответ: Д
2. При выборе индикатора по кривой титрования интервал изменения окраски должен лежать
А) до скачка титрования
Б) в пределах скачка титрования
Ответ: Б
3. При нитритометрическом титровании органических соединений, имеющих в молекуле первичную ароматическую аминогруппу реакция среды должна быть
А) кислая
Б) нейтральная
В) щелочная
Ответ: А
4. Для установления конечной точки титрования в методе нитритометрии в качестве индикатора используют
А) метиловый оранжевый
Б) метиловый красный
В) крахмал
Г) тропеолин 00
Ответ: Г
5. Количественное определение органических соединений, содержащих вторичную ароматическую аминогруппу можно проводить методом
А) алкалиметрии
Б) йодометрии
В) комплексонометрии
Г) нитритометрии
Д) броматометрии
Ответ: Г
Типовые задачи:
Н
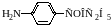 апишите
химизм, рассчитайте титр соответствия
при количественном определении
анестезина методом нитритометрии с
использованием в качестве титранта
0,1 М раствора нитрита натрия.
М.м.(анестезина) = 165,19.
апишите
химизм, рассчитайте титр соответствия
при количественном определении
анестезина методом нитритометрии с
использованием в качестве титранта
0,1 М раствора нитрита натрия.
М.м.(анестезина) = 165,19.
Н
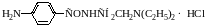 апишите
химизм, рассчитайте титр соответствия
при количественном определении
новокаинамида методом нитритометрии
с использованием в качестве титранта
0,1 М раствора нитрита натрия.
М.м.(новокаинамида) = 271,79.
апишите
химизм, рассчитайте титр соответствия
при количественном определении
новокаинамида методом нитритометрии
с использованием в качестве титранта
0,1 М раствора нитрита натрия.
М.м.(новокаинамида) = 271,79.
Рассчитайте предварительный объем титранта 0,02 М раствора натрия нитрита при количественном определении 0,25% раствора новокаина методом нитритометрии, если на титрование взята навеска 2,0 мл. 1 мл 0,02 М раствора натрия нитрита соответствует 5,456 мг новокаина.
Рассчитайте процентное содержание левомицетина, если на титрование 2,0 мл исследуемого раствора (после восстановления цинковой пылью) израсходовали 0,78 мл 0,02 М раствора натрия нитрита (Кп=1,0231). Объем контрольного опыта – 0,05 мл. 1 мл 0,02 М раствор натрия нитрита соответствует 6,462 мг левомицетина.
Формы контроля освоения заданий по самостоятельной аудиторной работе по данной теме
Типовой вариант выходного контроля.
Нитритометрическое титрование. Сущность метода. Окислительные и восстановительные свойства нитрита натрия.
Применение нитритометрии в фарманализе для определения веществ, содержащих первичную и вторичную ароматическую аминогруппу. Химизм.
Задача.
