
- •1. Теория химического строения а.М. Бутлерова. Электронное строение атома углерода и виды гибридизации.
- •2.Классификация и номенклатура органических соединений. Виды изомерии.
- •4.Конформации молекул алифатического ряда : этана, бутана, этаноламина. Проекции Ньюмена. Энергетика образования конформеров.
- •7. Молекулы с двумя центрами хиральности (диастереомерия). Оптическая изомерия винных кислот.
- •8. Электронные эффекты в молекулах: виды и механизм передачи. Классификация органиче-ских реакций.
- •Вопрос 9
- •1. Зависимость кислотности от гетероатома.
- •2. Влияние углеводородного радикала и присутствующих в нем заместителей
- •10. Спирты. Номенклатура и классификация спиртов. Химические свойства предельных одноатомных спиртов.
- •12. Фенолы.Общая характеристика.
- •14. Реакции присоединения – отщепления (реакции с гидроксиламином, аминами, гидразином и его производными). Реакции окисления, восстановления, полимеризации карбонильных со-единений.
- •18.Аминоспирты: аминоэтанол (коламин), холин, ацетилхолин. Аминофенолы: дофамин, норадреналин, адреналин. Биологическая роль этих соединений.
- •20. Оксокислоты. Характерные хим. Свойства.
- •23. Пептиды. Строение пептидной связи. Гидролиз пептидов. Первичная структура белка и методы её установления. Вторичная и третичная структура белка.
- •24. Моносахариды и их классификация. D- и l-стереохимические ряды. Формулы Фишера и Хéуор-са. Фуранозы и пиранозы; α- и β-формы. Циклооксотаутомерия. Конформации пиранозных форм.
- •25. Строение наиболее важных пентоз (рибоза, ксилоза), гексоз (глюкоза, манноза, галактоза, фрук-тоза), аминосахаров (глюкозамин, маннозамин), дезоксисахаров (2-дезоксирибоза). Их биороль.
- •27. Олигосахариды. Дисахариды: мальтоза, лактоза, целлобиоза, сахароза. Строение, циклооксотаутомерия. Восстановительные свойства, гидролиз, биологическая роль.
- •29. Салициловая кислота и её производные (ацетилсалициловая кислота, фенилсалицилат). П-амино-бензойная кислота и её производные (новокаин, анестезин). Биологическая роль этих соединений.
- •31. Гетероциклы с несколькими гетероатомами. Пиразол, имидазол, пиразин, пиримидин, тиазол, пурин. Барбитуровая кислота и её производные. Гидроксипурины (ксантин, мочевая кислота, витамин в1).
- •33. Лактим-лактамная таутомерия
- •34.Нуклеозиды и их гидролиз. Строение и гидролиз мононуклеотидов. Первичная структура нуклеиновых кислот. Фосфодиэфирная связь. Днк и рнк: состав и гидролиз. Вторичная структура рнк и днк
- •35Строение атф, адф, амф
- •36. Омыляемые липиды (жиры). Понятие о фосфолипидах. Их биороль.
- •37. Неомыляемые липиды. Понятие о терпенах (мирцен, гераниол, цитраль, лимонен, ментол, пинены, камфора). Сопряжённые полиены (витамин а). Их биороль.
- •21. Стероиды.
31. Гетероциклы с несколькими гетероатомами. Пиразол, имидазол, пиразин, пиримидин, тиазол, пурин. Барбитуровая кислота и её производные. Гидроксипурины (ксантин, мочевая кислота, витамин в1).
Пятичленные гетероциклы с двумя гетероатомами , один из которых азот, имеют общее название азолы. Важнейшими представителями являются пиразол, имидазол, пиразин, пиримидин, тиазол, пурин.
Пиразол.( C3H4N2O) Производные пиразола в природе не обнаружены. Наиболе известным производным пиразола является пиразолон. На основе пиразолона созданы анальгетические средства – анальгин, бутадион и др.

Имидазол.(С3Н4N2)Этот гетероцикл является структурным фрагментом белковой аминокислоты гистидина и продукта ее дикарбоксилирования – биогенного амина гистамина. Имидазол, конденсированный с бензольным кольцом – бензимидазол – входит в состав ряда природных веществ, в частности витамина В12, а также вазодилатируещего средства дибазола.

Пиразин.(C4H4N2) Шестичленное гетероциклическое органическое соединение с двумя атомами азота. Ароматичен. Хорошо растворим в воде, этаноле, этоксиэтане. Вступает в реакции нуклеофильного и электрофильного замещения. При аминировании амидом натрия в жидком аммиаке превращается в 2-аминопиразин. При окислении смесью уксусный ангидрид — перекись водорода, дает N-оксиды по одному или обоим азотам.

Пирамидин.(C4N2H4) Гетероциклическое соединение, имеющее плоскую молекулу, простейший представитель 1,3-диазинов. Производные пиримидина широко распространены в живой природе, где участвуют во многих важных биологических процессах. В частности, такие производные как цитозин, тимин, урацил входят в состав нуклеотидов, являющихся структурными единицами нуклеиновых кислот, пиримидиновое ядро входит в состав некоторых витаминов группы B, в частности B1, коферментов и антибиотиков. Пиримидиновая структура — как ароматическая, так и гидрированная, входит в состав многих биологически активных веществ и лекарственных препаратов — например, барбитуратов — производных 1,3,5-тригидроксипиридина, обладающих снотворным, противосудорожным и наркотическим действием.

Тиазол. (C3H3SN) В цикле тиазола содержатся два разных гетероатома. Структура тазола встречается в составе важных биологически активных веществ-тиамина и ряде сульфаниламидных препаратов, например, противомикробного средства фталозола. Цикл полностью гидрированного тиазола – тиазолидин – является структурным фрагментом пенициллиновых антибиотиков.

Пурин.(C5N4H4) Простейший представитель имидазо[4,5-d]пиримидинов. Бесцветные кристаллы, хорошо растворимые в воде, горячем этаноле и бензоле, плохо растворимые в диэтиловом эфире, ацетоне и хлороформе. Производные пурина играют важную роль в химии природных соединений (пуриновые основания ДНК и РНК; кофермент NAD; алкалоиды, кофеин, теофиллин итеобромин; токсины, сакситоксин и родственные соединения; мочевая кислота) и, благодаря этому, в фармацевтике.

К производным пирамидина относится барбитуровая кислота, которая может существовать в нескольких таутомерных формах. В кристаллическом состоянии барбитуровая кислота имеет строение триоксопроизводного, которое преобладает и в растворе. Барбтуровая кислота легко образует соли при действии щелочей. Её высокая кислотность, обусловлена эффективной днлокализацией отрицательного заряда в барбитурат-ионе с участием двух атомов кислорода.
Гипоксантин, ксантин и мочевая кислота образуются в организме при метаболизме нуклеиновых кислот. У гидроксипуринов возможна как лактим-лактамная таутомерия, так и таутомерия азолов, связанная с миграцией атома водорода от атома N-7 к N-2. Мочевая кислота конечный продукт метаболизма пуриновых соединений к организме. Мочевая кислота двухосновна , плохо растворима в воде, но легко растворяется в щелочах. Соли мочевой кислоты называются уратами. Ксантин по химическому поведению во многом аналогичен мочевой кислоте.
32.Алкалоиды - это азотсодержащие гетероциклические основания, обладающие сильной и специфической биологической активностью. Хорошо растворяются в воде. Содержание алкалоидов в растениях, как правило, невелико - от следов до нескольких процентов (на сухой вес растения). В цветковых растениях чаще всего представлено одновременно несколько групп алкалоидов, различающихся не только по химической структуре, но и по биологическим эффектам.
Алкалоиды: метилированные ксантины (кофеин, теофиллин, теобромин
содержатся в зернах кофе и чае, шелухе какао-бобов, в орехах кола. Кофеин, теобромин и теофиллин широко применяются в медицине. Кофеин используется преимущественно как психостимулятор, теобромин и теофиллин — как сердечно-сосудистые средства.

В отличие от других алкалоидов у метилированных ксантинов основные свойства выражены очень слабо, их соли с минеральными кислотами гидролизованы. За счет пиррольного атома азота теофиллин и теоброминобладают кислотными свойствами, они способны образовывать нерастворимые соли с ионами некоторых металлов, что используется для их идентификации и количественного определения в фармацевтическом анализе.
Так, водонерастворимый теофиллин, предварительно превращенный в растворимую натриевую соль, осаждается ионами кобальта(II) в виде солисветло-розового цвета.


Теобромин при такой же обработке дает соль серовато-голубогоцвета; анион этой соли представлен ниже в виде резонансных структур, соответствующих лактамной и лактимной формам теобромина. Кофеин, не обладающий кислотными центрами, подобной соли не образует.
На использовании кислотных свойств пуриновых алкалоидов основано получение водорастворимых препаратов. Примером может служить эуфиллин — соль теофиллина с этилендиамином.
Следует отметить, что все три метилированных ксантина устойчивы к щелочам только при обычной температуре, а при нагревании подвергаются частичному (теобромин) или полному разрушению с раскрытием пиримидинового кольца.
Пуриновые алкалоиды извлекают из отходов переработки чая (содержание кофеина до 5%) или из низкосортного кофе (содержание кофеина до 1,5%). Однако большую часть пуриновых алкалоидов получают синтетически из доступной и дешевой мочевой кислоты (см. 29.3.2).
Алкилированиексантина диметилсульфатом при pH 8—9 приводит преимущественно к образованию кофеина, при рН 4—7 — теобромина.

Атомы азота в молекуле ксантина подвергаются алкилированию в последовательности N-3,N-7,N-1, поэтому теофиллин прямым алкилированием ксантина синтезировать не удается, его получают другими методами.
Алкалоиды: никотин, анабазин
В эту группу входят алкалоиды относительно простого строения, довольно давно выделенные в чистом виде.

Никотин основной алкалоид табака и махорки, представляет собой жидкость с характерным табачным запахом.
Из двух атомов азота в молекуле никотина большей основностьюобладает атом азота насыщенного пирролидинового кольца, что объясняется их разной гибридизацией.
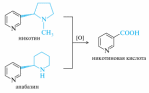
Анабазин— алкалоид ежовника безлистного, из которого его выделяют в промышленности. В небольшом количестве содержится в табаке. Анабазин представляет собой бесцветную жидкость. Анабазин по фармакологическому действию похож на никотин. Используется как средство, облегчающее отвыкание от курения табака, применялся еще как инсектицид, но в настоящее время снят с производства из-за высокой токсичности.
При окислении никотина и анабазина образуется никотиновая кислота:
Хинин— алкалоид, выделенный из коры хинного дерева (Cinchona oficinalis) — представляет собой бесцветные кристаллы очень горького вкуса.


Содержащиеся в его молекуле два атома азота различаются по основности, поэтому хинин образует два ряда солей: первым протонируется более основный атом азота хинуклидиновой системы.
Сульфат хинина в водном растворе дает синюю флуоресценцию. Флуоресценция настолько интенсивна, что заметна даже в очень разбавленных растворах хинина, например в прохладительных напитках, в которые небольшие количества хинина добавляются для горечи.
Хинин используется в медицине в качестве противомалярийного средства, однако к настоящему времени из-за многих негативных побочных эффектов применение его ограничено.
Общей реакцией на хинин является так называемая талейохинная проба. Она заключается в окислении хинина бромной водой до образования бесцветного раствора орто-хинона. Последующее действие раствором аммиака приводит к образованию дииминопроизводных орто-хиноидной структуры, окрашенных визумрудно-зеленый цвет.
Морфин— важнейший из опиумных алкалоидов. Морфин, кодеин и тебаин относятся к морфинановым алкалоидам. Морфин обладает сильным анальгезирующим действием, благодаря чему долгое время использовался в медицине в качестве обезболивающего средства. Морфин, его производные и синтетические аналоги, относящиеся к классу наркотических анальгетиков, называются опиатами.
Крайне негативным побочным действием морфина является возникновение в результате даже непродолжительного применения болезненного привыкания (наркозависимости). Некоторые синтетические производные морфина обладают более сильным наркотическим действием, чем сам морфин. Диацетат морфина — героин — наиболее распространенный наркотик. Вещество Бентли (синтетический аналог морфина) примерно в 10 000 раз активнее морфина.
