
- •Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
- •Оптические свойства полимерных композиционных покрытий
- •1 Оптические свойства наполненных полимерных систем
- •1.1 Отражение света
- •1.2 Рассеяние и поглощение света
- •1.3. Оптимизация процесса диспергирования с использованием функции гкм
- •1.4 Влияние объемного содержания пигментов на оптические свойства композиционных материалов
- •1.5 Определение укрывистости
- •Визуальный метод.
- •Метод контрастных отношений.
- •1.6 Красящая и разбеливающая способность пигментов
- •1.7 Влияние дисперсного состава и формы частиц на оптические свойства пигментированных лакокрасочных материалов
- •2 Механизм зрения
- •3 Цвет пигментированных лакокрасочных материалов
- •3.1 Причины окрашенности органических и неорганических соединений
- •Переход электрона с катиона более низкой валентности на катион более высокой валентности
- •Электронные переходы, вызванные дефектами кристаллической структуры
- •Электронные переходы, обуславливающие цвет органических соединений.
- •3.2 Источники света. Цветовая температура
- •4 Метрология цвета
- •4.1 Основные понятия и определения цветометрии
- •4.2 Неравноконтрастные колористичекие системы
- •4.2.1 Система r, g, в
- •4.2.2 Колористическая система xyz
- •4.3 Колористическая система ciel*a*b*
- •4.4 Определение цветовых характеристик спектрофотометрическим методом
- •4.4.1 Расчет координат цвета по способу взвешенных ординат
- •4.4.2 Расчет координат цвета по способу избранных ординат
- •4.5 Расчет цветового различия
- •4.6 Оценка белизны
- •4.7 Оценка желтизны
- •4.9 Оценка черноты
- •4.9 Аддитивное и субстрактивное смешение цветов
- •4.10 Расчет рецептур лакокрасочных материалов заданного цвета и колеровка
- •5 Средства измерения цвета
- •5.1 Геометрия измерения
- •5.2 Аппаратура
- •5.3 Измерение блеска
- •Задачи для самостоятельной подготовки студентов
- •Список использованных источников
- •Электронный ресурс:http://allchem.Ru/pages/inorganic/8
Электронные переходы, обуславливающие цвет органических соединений.
В соответствии с теорией молекулярных орбиталей, образование σ- и π-связей в молекуле в общем случае приводит к реализации набора молекулярных орбиталей, характеризующихся различным распределением электронных плотностей между ядрами атомов. Орбитали с максимальной электронной плотностью между атомами обладают меньшей энергией, нежели орбитали с минимальной электронной плотностью. Орбитали с меньшей энергией называют связывающими (σ, π), орбитали с большей энергией - разрыхляющими (σ*, π*). В первую очередь происходит заполнение связывающих орбиталей. Если в молекуле имеются атомы со свободными электронными парами, не принимающими участия в образовании связей, то они находятся на несвязывающей орбитали (n). Энергетические уровни соответствующих орбиталей возрастают в следующем порядке:
σ< π < n < π*< σ*.
Поглощение света молекулой вызывает переход электронов в ней на более высокий энергетический уровень. Вещество будет поглощать свет в видимой части спектра, если возможны переходы электрона под действием электромагнитного излучения соответствующей энергии. Переход σ - σ*, наиболее характерный для насыщенных углеводородов, совершается с поглощением энергии, соответствующей дальней УФ-области спектра. π - π*- переходы, характерные для ненасыщенных органических соединений, требуют меньших энергий. Однако в случае изолированных двойных связей поглощение света происходит в УФ-области, и лишь при наличии сопряжения повышение энергии π - уровня может привести к такому снижению энергии π - π*-перехода, что он будет происходить под действием света видимой части спектра. Удлинение системы сопряжения вызывает батохромный эффект.
В гетероорганических соединениях неподеленные электроны азота, кислорода, серы способны к π - π*- и π - σ*-переходам, требующим сравнительно малых энергий. По этой причине большинство гетероорганических соединений поглощают свет в видимой и ближней УФ-области.
Присоединение к системе сопряжения поляризующих заместителей, смещающих σ-электроны в невозбужденном состоянии по цепи сопряжения, приводит к снижению энергии π - π*-перехода и вызывает батохромный эффект (рисунок 18). Такие заместители могут быть электронодонорными (например, -ОН, NH2, -SH) и электроноакцепторными ( например, -NO2, -NO, >C=O). Введение в молекулу таких заместителей кроме смещения полосы поглощения в длинноволновую область вызывает также и повышение максимума абсорбции света (гиперхромный эффект). Причиной батохромного эффекта является и образование комплексных и внутрикомплексных соединений красителей с металлами. Реакции комплексообразования оксиантрахинонов (ализарина, пурпурина) с ионами трехвалентных (Al, Fe, Сг) и двухвалентных (Са, Ва, Со) металлов лежат в основе получения крапплаков. Внедрение в комплекс трехвалентного металла дает возможность варьировать цвет пигмента. Комплексообразование имеет место при получении фталоцианиновых и азопигментов.
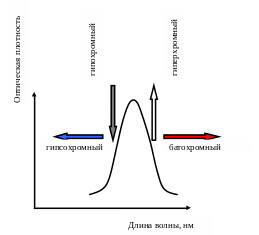
Рисунок 18 –Смещения спектра отражения
На цвет органических соединений оказывают влияние и пространственные факторы. Так, искажение формы молекулы (углов между направлениями связей) повышает энергетический уровень молекулы в основном состоянии, снижает энергию перехода в возбужденное состояние и вызывает тем самым батохромный эффект. Однако, если возможен поворот одной части молекулы относительно другой, и введение какого-либо заместителя нарушает плоскостную структуру молекулы красителя, то это приводит к гипохромному эффекту из-за разобщения отдельных участков цепи сопряжения [2,7].
