
- •1.2.1. Применение ионной флотации для извлечения тяжёлых металлов из техногенных вод
- •1.2.2. Обзор современных методов рационального подбора реагентов-собирателей для ионной флотации
- •2.5. Методы проведения расчётов квантово-химических параметров субстратов, реагентов-собирателей и систем «субстрат-реагент»
- •4.5. Квантово-химические исследования параметров реакционной способности субстратов меди, цинка, железа и марганца и установление их эффективных извлекаемых форм
- •Выводы по главе 4
- •5.1. Квантово-химический метод выбора реагентов-собирателей для флотационного извлечения катионов меди (II) и цинка из техногенных вод горных предприятий
- •5.1.1. Исследование квантово-химических прс молекул известных реагентов-собирателей, применяемых для флотационного извлечения катионов тяжелых и цветных металлов из техногенных вод
При добыче и переработке руд на горно-обогатительных медно-цинковых предприятиях Уральского региона образуются значительные объёмы техногенных вод, таких как подотвальные, карьерные и шахтные воды, характеризующиеся различным поликомпонентным составом тяжелых и цветных металлов с минерализацией от долей до сотен мг в 1 дм3 с приоритетным содержанием меди, цинка, марганца и железа. Эти воды являются одним из основных источников поступления металлов в поверхностные и подземные водоемы, оказывая сильное токсичное воздействие на экосистемы районов недропользования; в прилегающих поверхностных водоемах рыбохозяйственного назначения ПДК по этим металлам значительно превышает фоновые значения. По различным данным для меди и цинка это превышение составляет 80-500 раз, для марганца – до 1000 раз, для железа – 50-60 раз [46, 58, 74, 108-110].
Вынос рудничными водами значительных количеств указанных компонентов продолжается после завершения эксплуатации месторождения в течение десятков лет, что приводит не только к загрязнению атмосферы, почвы, поверхностных и подземных вод, но также к потере ценных компонентов: ежегодно с кислыми рудничными водами на предприятиях, занимающихся добычей и переработкой медно-колчеданных руд, безвозвратно теряется около 15 тыс. т меди, столько же цинка, порядка 40 тыс. т железа, десятки тыс. т марганца и других металлов, истощая источники природного минерального сырья [125, 126, 351]. Следовательно, горно-обогатительные комбинаты, разрабатывающие медно-колчеданные месторождения, должны создавать дополнительные технологические переделы с целью организации процессов комплексного извлечения загрязняющих компонентов из техногенных вод с получением безопасных твёрдых отходов.
Переведение любых отходов в качественное сырье для других отраслей и их превращение в новые продукты (реутилизация) является концептуальной основой теории и практики комплексного использования гидротехногенного сырья.
Практически все медно-цинковые горные предприятия Уральского регтона для очистки техногенных вод в настоящее время используют метод нейтрализации для выделения металлов в виде гидролитических осадков без их дальнейшего разделения и реутилизации. При применении таких методов извлечения металлов, как сорбция и экстракция сталкиваются с такими их недостатками как невысокая скорость ионного обмена, большие потери органической фазы, высокие капитальные и эксплуатационные затраты, пожароопасность, сложность организации природоохранных мероприятий.
Наиболее перспективным, высокоэффективным и экономически обоснованным представляется флотационный метод, характеризующийся простотой технологических операций, высокой производительностью, низкой потерей органического реагента, хорошей сочетаемостью с другими способами переработки техногенных рудничных вод низкой концентрации, комбинирующий преимущества методов сорбции, экстракции и химического осаждения с возможностью удаления взвешенных частиц, что позволяет проводить глубокую переработку минерализованных техногенных вод. Возможно применение напорной флотации и электрофлотации в зависимости от способа газонасыщения, условий селективного выделения и концентрирования полезных компонентов из техногенных вод в дисперсную фазу.
Научное обоснование, разработка и использование флотационных методов в составе комплексных технологий переработки гидротехногенного сырья невозможны без предварительно проведенных исследований химических, физико-химических, квантово-химических и технологических свойств как самих извлекаемых субстратов (тяжелых металлов), так и извлекающих агентов (осадителей, окислителей и реагентов-собирателей), без изучения механизма процессов флотационного извлечения, без управления эффективностью этих процессов с помощью направленного выбора реагентов-собирателей при применении ионной флотации и внедрения энергосберегающего оборудования при проведении электрофлотации.
Таким образом, создание на горно-обогатительных предприятиях экологически безопасных ресурсовоспроизводящих комплексных технологий селективного глубокого извлечения тяжелых металлов из техногенного гидроминерального сырья с получением высоколиквидных полезных компонентов, сохранением водных ресурсов и предупреждением токсичных загрязнений окружающей среды отвечает современным условиям развития практики обогащения полезных ископаемых, является актуальной научной и важной хозяйственной проблемой, влияющей на развитие отрасли в целом и имеющей социальное значение. Внедрение таких технологий позволит достичь значительных технико-экономического и экологического эффектов.
Работа основана на результатах НИОКР, выполненных в Магнитогорском государственном техническом университете по грантам РНП 2.1.2.6594, РФФИ 10-05-00108а и Государственному контракту № 02.740.11.0038, а также по прямым хоздоговорам с ОАО «Гайский ГОК» (г. Гай, Оренбургская область), ОАО «Учалинский ГОК» (г. Учалы, Башкортостан), ОАО «Башмедь» (г. Сибай, Башкортостан) в 2007-2011 г.г. при непосредственном участии автора.
Основные научные положения, выносимые на защиту:
1. Методология создания ресурсовоспроизводящих технологий переработки техногенных вод, основанная на иерархическом построении последовательно осуществляемых уровней - информационно-аналитическом, инструментальном, технологическом и эколого-экономическом, имеющих внутренний итерационный порядок выполнения и анализа условий реализуемости.
2. Квантово-химические расчёты параметров реакционной способности субстратов тяжёлых и цветных металлов, реагентов-собирателей и продуктов их взаимодействия, и квантово-химическое моделирование энергетически выгодных и конформационно устойчивых флотационных систем «субстрат-реагент».
3. Использование принципа «структура - свойство/активность - свойство» позволяет квалифицированно выбирать реагенты-собиратели с заранее заданными свойствами, определёнными в зависимости от квантово-химических, физико-химических и структурных параметров реакционной способности извлекаемых ценных компонентов.
4. Новый класс перспективных реагентов-собирателей для ионной флотации цинка и меди (II) - сложные эфиры терефталевой кислоты, обладающие оптимальным набором параметров реакционной способности (ПРС).
5. Глубокое селективное извлечение марганца методом электрофлотации предопределяется условиями осуществления процесса окисления марганца (II), использованием электрохимически генерированного «активного хлора», предварительной электрокоагуляцией образующихся труднорастворимых гидрофильных осадков MnO(OH), MnO(OH)2, их устойчивостью и последующим извлечением в пенный продукт по электростатическому механизму.
6. Ресурсовоспроизводящая технология комплексной переработки гидротехногенного минерального сырья медно-колчеданных месторождений с приоритетным содержанием цинка и меди включает следующие стадии: извлечение цинка (при рН 2-3) и меди (при рН 7-8) методом ионной флотации в ходе поэтапной нейтрализации технологических растворов с использованием реагента-собирателя РОЛ, имеющего оптимальный набор ПРС; получение гидролитических осадков при рН 10-11; их кондиционирование в процессах коагуляции и флокуляции; реутилизацию металлсодержащих шламов и регенерацию реагента – собирателя РОЛ.
7. Ресурсовоспроизводящая технология комплексной переработки гидротехногенных ресурсов медно-колчеданных месторождений с приоритетным содержанием марганца включает проведение предварительного выделения меди цементацией, осаждение железа методом нейтрализации в виде гидроксида при рН 4,0 - 4,3, последующее окислительное электроосаждение, электрокоагуляцию и электрофлотационное извлечение марганца с целью получения кондиционных товарных продуктов и очищенной воды.
Флотационные методы переработки техногенных промышленных вод наиболее перспективны, высокоэффективны и экономически обоснованы. Они характеризуются простотой технологических операций, возможностью использования имеющегося на обогатительных фабриках оборудования, высокой производительностью, низким расходом органических реагентов, хорошей сочетаемостью с другими способами переработки техногенных рудничных вод низкой концентрации, комбинируют преимущества методов сорбции, экстракции и химического осаждения с возможностью удаления взвешенных частиц, что позволяет проводить глубокую переработку минерализованных техногенных вод с одновременным получением чистой, очищенной до требований ПДК воды, с отсутствием вторичного загрязнения, возможностью извлечения ионов тяжелых металлов до 96 %. А.М. Когановский [150] относит флотационную переработку сточных промышленных вод к самым эффективным и доступным методам.
Процесс флотации заключается в формировании во флотаторе флотокомплексов частица–пузырек газа, последующем всплывании данных комплексов и удалении образовавшегося пенного слоя осадка с поверхности сточной воды. В зависимости от способа получения пузырьков газа в жидкости различают следующие методы флотации:
- механическая флотация пузырьками, образующимися при диспергировании воздуха механическими перемешивающими устройствами;
- напорная флотация (вакуумная флотация) пузырьками, выделяющимися из пересыщенных растворов газов в воде соответственно при атмосферном давлении либо разрежении;
- пневматическая флотация пузырьками, образующимися при пропускании сжатого воздуха через пористые материалы (пластины фильтров, керамические мембраны и пр.);
- электрофлотация – флотация пузырьками электролитических газов, образующимися при электролизе воды.
В практике водоочистки наиболее широко используется три варианта данного метода – пневматическая флотация, напорная флотация и электрофлотация, в зависимости от способа газонасыщения растворов, условий селективного выделения и концентрирования полезных компонентов из техногенных вод в дисперсную фазу. Эффективность процесса флотации колеблется в довольно широких пределах: от 20 до 99 %. Флотационный процесс протекает в 4-6 раз быстрее отстаивания при одинаковом эффекте удаления загрязнений. Интенсификацию процесса флотации возможно повысить, используя реактор-сепаратор, который может работать как в циркуляционном, так и в прямоточном режимах [145], применяемых в зависимости от исходного содержания загрязняющих веществ.
Ионная флотация тяжелых металлов из техногенных вод может быть осуществлена как методом пневматической, так и напорной флотации. Она обладает высокой производительностью и наиболее эффективна при низких концентрациях извлекаемых ионов (меньше 10-3-10-2 моль/дм3).
Применение ионной флотации и электрофлотации для извлечения тяжелых металлов из техногенных вод детально рассмотрены ниже, в разделах 1.2.1-1.2.3.
1.2.1. Применение ионной флотации для извлечения тяжёлых металлов из техногенных вод
Термин «ионная флотация» введен в 1959 г. Феликсом Себба (F. Sebba) [293] для обозначения процесса флотационного извлечения находящихся в растворе ионов и других агрегатных форм металлов (так называемых коллигендов) с помощью реагентов-собирателей. Коллигенды в процессе ионной флотации реагируют с добавляемыми в раствор реагентами - веществами, обладающими поверхностно-активными свойствами (ПАВ) [103, 115, 290], в результате образуются малорастворимые соединения (сублаты), которые адсорбируются и концентрируются на границе раздела фаз «раствор - газ», активированной поверхностно-активными веществами. Условия процесса подбираются таким образом, чтобы барботируемые через раствор пузырьки газа флотировали образовавшиеся сублаты. На поверхности раствора возникает небольшой (не более нескольких сантиметров) слой неустойчивой пены, разрушающейся в разделительном аппарате, верхняя часть которого содержит гидрофобные сублаты [103, 293]. В большинстве случаев для флотации ионов и других агрегатных форм металлов из растворов необходим газ как инертная фаза для образования межфазной поверхности жидкость - газ. Известно использование воздуха, азота, аргона и других инертных газов, но в промышленных масштабах обычно ориентируются на воздух 141, 272.
В отличие от флотации минералов, где эффективно извлекаются частицы размером от десятков до сотен микрометров, для оптимальных условий ионной флотации характерно извлечение крупных рыхлых хлопьевидных агрегатов, содержащих 97-99 % воды.
В трудах зарубежных учёных F. Sebba, N. W. Rice, D.C. Dorman, R. Lemlich, T. Sasaki, Pinfold, E.J. Mahne и многих других приведены варианты процессов, используемых для разделения и концентрирования полезных компонентов техногенных вод 7, 17-19, 32, 33. Наряду с ионной флотацией, известен ряд других родственных способов выделения и концентрирования ценных компонентов из растворов [86, 87, 179, 190, 290]: пенное и пузырьковое фракционирование, обратная ионная флотация, флотация осадков, флотоэкстракция и др. Классификация и номенклатура пенных флотационных процессов, используемых в гидрометаллургии и очистке сточных вод, представлены также в работах А.М. Гольмана, И.А. Диброва, Н.Н. Воронина, В.В. Свиридова и др. [87, 104, 119, 291].
Теоретические основы и практика переработки технологических растворов различного происхождения с целью извлечения тяжёлых и цветных металлов методом ионной флотации изложены в трудах Б.Н. Ласкорина, А.М. Гольмана, Л.Д. Скрылёва, С.Г. Мокрушина, Р.Е. Баарсона, А.К. Поднека, А.И. Мацнева, В.В. Пушкарёва, Ю.Б. Рубинштейна, Н.Н. Воронина, А.В. Радушева, В.Ф. Сазоновой и др.
Данный метод в настоящее время получил широкое распространение при переработке техногенных вод ряда отраслей промышленности (бумажной, нефтяной) [190, 266, 291], при извлечении редких металлов из рассолов [128-130], для извлечения из технических растворов заводов цветной металлургии и гальванических производств таких тяжёлых металлов, как Cu2+, Co2+, Ni2+, Zn2+, Fe3+, Cr+3 и др. [220, 250, 268-271]. Обычно ионная флотация применяется при переработке низкоконцентрированных техногенных вод и бедных технологических растворов 105, 150, 290. Учитывая, что в будущем, ввиду ограниченности запасов высококачественного минерального сырья, в сферу промышленного производства будут вовлекаться все большие количества бедных и труднообрабатываемых руд, это неизбежно приведет к расширению сферы применения данного метода [87, 260, 354].
Известно, что применение ионной флотации в сочетании с другими химическими и физико-химическими методами переработки техногенных вод обеспечивает настолько глубокое извлечение тяжелых металлов из растворов, что очищенные воды могут быть повторно использованы в оборотном водоснабжении горных предприятий, а их излишки - сбрасываться на рельеф без нанесения экологического ущерба районам недропользования [266, 290, 291]. Утилизация получаемых осадков гидроксидов металлов и пенного продукта ионной флотации, т.е. их квалифицированное применение, могло бы снизить стоимость затрат на переработку растворов и сделать технологическую схему рентабельной [95].
Эффективность процесса ионной флотации исследователи чаще всего оценивают следующими параметрами:
- степенью извлечения металла и ПАВ из раствора, % [32, 86, 271, 314];
- степенью гидрофобности осадка [298-302];
- временем протекания процесса t [32, 33];
- растворимостью сублата [165, 190]: чем меньше растворимость сублата, тем выше степень флотационного выделения ионов тяжелого металла;
- коэффициентом распределения D извлекаемого коллигенда между гидрофобным сублатом, находящимся в верхней части неустойчивой пены, и раствором [290, 302]:
 ,
,
где
 - концентрация коллигенда в гидрофобном
сублате;
- концентрация коллигенда в гидрофобном
сублате;
 -
концентрация коллигенда в растворе.
-
концентрация коллигенда в растворе.
У становлено,
что степень извлечения тяжелых
металлов из растворов с помощью кислотных
собирателей
тем больше, чем меньше растворимость
сублата, чем выше
концентрация выделяемых из раствора
коллигендов [190]. При прогнозировании
максимально возможной степени
флотационного извлечения тяжелых
металлов по величине
растворимости их сублата авторы считают,
что прогноз справедлив лишь в том случае,
когда:
становлено,
что степень извлечения тяжелых
металлов из растворов с помощью кислотных
собирателей
тем больше, чем меньше растворимость
сублата, чем выше
концентрация выделяемых из раствора
коллигендов [190]. При прогнозировании
максимально возможной степени
флотационного извлечения тяжелых
металлов по величине
растворимости их сублата авторы считают,
что прогноз справедлив лишь в том случае,
когда:
- флотация ведется «до конца» и осуществляется в том диапазоне значений рН растворов, в котором сублат представляет собой труднорастворимый осадок;
- собиратель вводят в раствор в количестве, незначительно превышающем стехиометрически необходимое количество для образования осадка сублата, оптимальный расход собирателя несколько превышает стехиометрически необходимый, т.к. собиратель в ионной флотации чаще всего выполняет еще и роль пенообразователя (в случае использования пневматической флотации).
При расходе собирателя меньшем, чем стехиометрическое, степень флотационного выделения ионов тяжелых металлов снижается, так как не все ионы металла связываются собирателем в малорастворимый сублат. При расходе собирателя, значительно превышающем стехиометрическое соотношение, резко возрастает конкуренция между частицами сублата и молекулами собирателя за место на поверхности пузырьков воздуха. Кроме того, избыточный расход собирателя нежелателен с экономической и экологической точек зрения. Он приводит к потере собирателя и загрязнению собирателем отработанных растворов.
Среди многих факторов, существенно влияющих на процесс флотационного выделения ионов тяжелых металлов и широко используемых для его регулирования, особое место принадлежит рН. Как правило, исследователи действие рН на процесс флотации связывают с его влиянием на диссоциацию ионогенных групп собирателя, растворимость сублата, форму нахождения ионов коллигенда в растворе, электроповерхностные свойства частиц сублата [266, 290]. Анализируя влияние рН на результаты и селективность флотации сублатов, необходимо учитывать, что, параллельно с изменением концентраций Н+ и ОН-, происходит [299, 300, 302]: 1) Изменение концентраций вводимых с регуляторами рН катионов (К+, Na+ и др.) или анионов (CI-, SO42- и др.). Эти ионы могут конкурировать с коллигендом за собиратель, изменять форму сублата и т. д. 2.) Изменение ионной силы раствора. Гидратация неорганических ионов, нарушая ориентацию молекул воды вокруг сублата, может привести к его дегидратации, т.е. к увеличению поверхностной активности и скорости адсорбции.
Модельные представления о процессе ионной флотации [73, 103, 290] позволили проанализировать влияние комплека основных физических параметров процесса: расхода регента-собирателя, времени пребывания раствора во флотомашине, высоты и объема флотационной камеры, расхода газа и размера пузырьков. Показано, в частности, что при выборе высоты флотационной камеры следует исходить из времени, необходимого для установления стационарного значения адсорбции на всплывающих пузырьках.
В работах С.Ф. Кузькина и А.М. Гольмана 103, 165 подробно рассмотрены сущность и особенности ионной флотации, представлены количественное описание химических закономерностей, методика выбора реагентов-собирателей, а также кинетическая модель процесса. Отмечается, что потери органических реагентов с отработанными растворами ионной флотации при правильно выбранном реагентном режиме не превышают нескольких миллиграммов на литр переработанного раствора. Степень извлечения металла, содержащегося в растворе с исходной концентрацией в интервале 10÷500 мг/дм3, составляет 90-99 %, влажность полученного пенного продукта обычно - 10-20 %.
По мнению А.М. Гольмана 103, ионную флотацию целесообразно применять при исходных концентрациях извлекаемого компонента 10-5–10-2 моль/дм3. При больших концентрациях слишком велик объемный выход пенного продукта, т.к. увеличивается захват частицами осадка маточного раствора, а при меньших – возрастает время, необходимое для достаточного полного извлечения ионов, а также стоимость потерь ПАВ с отработанными растворами и затраты на очистку последних. Оптимальными же, с точки зрения кинетических возможностей, а также соотношения выхода пенного продукта и стоимости потерь ПАВ или затрат на очистку, являются исходные концентрации металла на уровне десятков - сотен миллиграммов в литре. В более поздней работе А.В. Радушева 269-271 доказано, что ионная флотация может быть эффективно применена в более широком интервале концентраций металлов в технологических растворах - от десятых долей грамма до десятков граммов в литре.
Промышленное освоение ионной флотации и связанные с ним обстоятельные исследования процесса начались после 1970 г. 103. В качестве примеров исследований тех лет можно привести: 1) Разработку и внедрение технологии ионной флотации молибдена на Балхашском комбинате, эксплуатация которой позволила технологически просто и экономически эффективно утилизировать в виде товарного продукта молибден, терявшийся ранее со сбросными растворами производства молибдата кальция. Кроме того, снизилась до санитарных норм концентрация молибдена в сливе хвостохранилища комбината. 2) Разработку и внедрение в производство технологии ионной флотации вольфрама из отвальных продуктов Нальчикского гидрометаллургического завода и Узбекского комбината тугоплавких металлов.
Практическое внедрение метода ионной флотации на предприятиях затруднено из-за ограниченного ассортимента поверхностно-активных веществ, используемых в качестве собирателей. Выбор реагентов для ионной флотации носит часто эмпирический характер, не учитывает особенности строения их молекул и распределения электронной плотности [268]. В ряде работ отмечается недостаточность изучения химических и физико-химических закономерностей процесса [105, 271, 354].
Рассмотрим основные направления современных научных исследований в области извлечения тяжёлых металлов из техногенных минерализованных вод методом ионной флотации.
Исследования по созданию новых способов выделения ценных и токсических компонентов технологических растворов, интегрирующих процессы флотации (основной процесс), сорбции, экстракции и коагуляции, и по практическому внедрению методов ионной флотации в практику очистки сточных вод гальванических производств ведутся под руководством В.Ф. Сазоновой в Одесском национальном университете им. И.И. Мечникова.
Разработке физико-химических основ очистки сточных вод промышленных предприятий от истинно- и коллоидно-растворённых веществ и созданию новых реагентов-собирателей для ионной флотации посвящены работы профессора Л.Д. Скрылёва и его учеников.
В работах Л.Д. Скрылева с соавторами [298-302] продемонстрирована принципиальная возможность извлечения ионов тяжелых металлов (свинца, ртути, хрома, никеля, меди, цинка и др.) из техногенных вод путем их осаждения ферроцианидом калия с последующей пенной сепарацией образовавшегося осадка желатином. Те же авторы предложили способ выделения ионов цинка из промышленных технологических растворов производства вискозного волокна предварительным осаждением цинка в виде сульфида с последующей флотацией в присутствии хлористого лауриламмония. Кроме того, в работах Л.Д. Скрылёва, Т.Ф. Полтораниной, К.А. Разумова [259, 260, 272], Н.Н. Тетериной [314], R.E. Baarson и C.L. Ray [2] показано, что, используя в качестве собирателя натриевые и калиевые мыла синтетических жирных кислот фракции С10-26, можно извлекать методом ионной флотации медь, цинк, кобальт, никель, железо и другие тяжелые металлы. Так, например, согласно результатам проведённых авторами исследований, флотационная очистка технологических растворов с помощью лаурата калия, содержащих от 80 до 380 мг/дм3 ионов никеля (II), снижает их концентрацию в среднем до 0,4 мг/дм3 179.
Т.Ф. Полторанина, К.А. Разумов и другие исследователи разработали [259, 260, 272, 314] селективно-коллективную технологическую схему, включающую предварительную флотацию железа при рН 2,2-2,6 и последующую флотацию цветных металлов в коллективный концентрат при повышении рН до 8,5-9,0 с регенерирацией высокомолекулярных карбоновых кислот и получением концентрированных сульфатных растворов железа и цветных металлов. По этой схеме была проведена, например, флотация металлов из хлоридного раствора, полученного при выщелачивании хлоридных возгонов из огарка пиритного концентрата. Раствор имел следующий состав: железо 0,89 г/дм3, кобальт 0,625 г/дм3, никель 0,21 г/дм3, медь 1,075 г/дм3, цинк 0,13 г/дм3. В результате флотации было извлечено 97,5 % железа, 2,5 % меди и по 0,2-0,45 % цинка, никеля и кобальта. С переработанным раствором терялось до 30 мг собирателя на 1 г извлеченных металлов.
Е. Маhne и N. Pinfold [19] продемонстрировали принципиальную возможность извлечения железа, меди, цинка, свинца, никеля, кобальта, палладия, ванадия, марганца, церия и селена из разбавленных (10-5-10-4 М) водных растворов методами флотации гидрофобных осадков. В качестве осадителей использовались диаминобензиин, гидроксихинолин, α-нитрозо-β-нафтол, купферрон, оксимы, в качестве собирателей — хлористый додецилпиридиний и Arquad 2HT (R(CH3)2NCl, где R — длинноцепочечный алкил).
В работах [272, 314] предложены технологические схемы глубокой переработки технологических растворов, содержащих ионы тяжелых металлов Cu2+, Co2+, Ni2+, Zn2+, Fe3+, Cr+3, включающие стадию ионной флотации.
В работе Н.Н.Тетериной и С.М. Адеева с сотрудниками исследованы флотационные свойства собирателя ЭМКО, представляющего собой смесь натриевых мыл карбоновых кислот с длиной углеводородного радикала более С21 [314]. Установлено, что при флотационном извлечении ионов металлов Cu2+, Ni2+, Cr3+, Fe3+, после предварительного переведения их в нерастворимые гидроксиды, эффективнее применять ЭМКО совместно с пенообразователем НК-82. Степень извлечения металлов в пенную фракцию при оптимальных условиях процесса флотации (при значениях рН для Fe3+ - 6,0-8,0, Cr3+ - 7,0-8,3, Ni2+ - > 10,0, Cu2+ - 8,0-10,0; мольном соотношении [ЭМКО]:[Ме]=1:(8÷15); времени флотации З-5 мин; концентрации пенообразователя НК-82 15-20 мг/дм3) составляет для Fe3+ - 99,5 %; Cu2+ - 93,3 %, Ni2+ - 97,9 %, Cr3+ - 100 %.
R.E Baarson. и C.L. Ray [2, 63] сообщают о возможности концентрирования и разделения находящихся в растворе металлов (Сu, Fе, Zn, Mg, Ni, Co, Cr) путем ионной флотации предварительно осажденных гидроксидов этих металлов. Большая часть исследований была проведена на растворах сульфата меди (II). Установлено, что гидроксид меди (II) может быть сфлотирован как анионными, так и катионными собирателями. Наиболее эффективными оказались жирные кислоты, алифатические первичные амины и диамины, содержащие 12-14 атомов углерода в углеводородной цепи. Во всех случаях оптимальным для флотации гидроксида меди (II) является интервал рН 7 ÷ 8. Высокая скорость флотации при достаточно низком объемном выходе пенного продукта была получена при концентрациях меди в исходном растворе от 0,01 до 5 г/дм3 (оптимальным является интервал 0,1÷1,0 г/дм3). Авторы подчеркивают, что селективное выделение различных металлов возможно путем ступенчатого повышения рН.
В качестве примера R.E. Baarson и C.L. Ray приводят результаты коллективной флотации меди и железа из осветленного раствора, полученного в результате сернокислотного выщелачивания аризонской медной руды. Раствор имел рН 2,6, содержал 0,5 г/дм3 меди и 0,08 г/дм3 железа. После повышения рН до 7,5, добавления собирателя NeO-Fat 265 (натриевые мыла жирных кислот кокосового масла) и пенообразователя изопропанола проводилась непрерывная коллективная флотация гидроксидов железа и меди (II) в специально сконструированной пневматической четырехкамерной флотомашине емкостью 2 дм3. При расходах собирателя и пенообразователя 20-30 мг/дм3 и времени пребывания во флотомашине около 4 мин. извлечение железа и меди достигло 97-99 %. Стоимость реагентов составила примерно 100 долларов на 1 т меди в концентрате или 18 центов на 1 м3 исходного раствора.
А. Рубин с сотрудниками [29-31] изучали раздельное извлечение железа и меди из растворов методами, сочетающими флотацию растворенных в растворе ионов и флотацию предварительно осажденных гидроксидов. Было установлено, что флотация гидроксидов имеет ряд технологических преимуществ: меньший расход собирателя, высокую скорость процесса, низкую чувствительность к присутствующим электролитам и др.
Распространен метод удаления ионов тяжелых металлов из сточных вод сульфгидрильными собирателями, такими, как ксантогенаты, дитиофосфаты, тиокарбаматы, диалкилдитиофосфаты, первичные алифатические амины, алкиларилсульфокислоты, додецилбензосульфонат натрия [39, 259].
В Пражском институте исследования руд был разработан процесс флотации гидрофобных осадков, позволяющий концентрировать и разделять находящиеся в растворе металлы [5]. В качестве собирателей использовали органические вещества, имеющие полярно-аполярную структуру молекул (алкилксантогенаты, алкил- и арилдитиокарбаматы, дитизон), осаждающие катионы большинства цветных и редких металлов в виде труднорастворимых соединений (ПР = 10-6÷10-40), обладающих высокой гидрофобностью.
T. Sasaki [32] изучал возможность применения метилового и этилового ксантогенатов для извлечения кобальта и никеля из растворов, полученных после выщелачивания пиритного огарка. После цементации железным скрапом раствор, содержащий 0,25 г/дм3 кобальта, 6,50 г/дм3 железа, 3,00 г/дм3 цинка, 0,17 г/дм3 алюминия и 0,22 г/дм3 марганца, перемешивался с метиловым ксантогенатом калия (в молярном соотношении количества вещества собирателя и металла 3 моля :1 моль) при рН 4,5. Флотация гидрофобного осадка ксантогенатов осуществлялась во флотомашине Денвер. Извлечение кобальта составило 90 %. Чистота концентрата увеличивалась при промывке разбавленной серной кислотой. Разделение кобальта и никеля осуществлялось при обработке концентрата раствором аммиака, который селективно растворяет ксантогенат никеля.
Д.Б. Холикулов, Н.М. Рахмонов, С.И. Кодиров, В.С. Стрижко и др. рекомендуют использовать в качестве собирателей ионной флотации катионов меди, молибдена из сернокислых растворов амиловый, этиловый, изопропиловый ксантогенаты, ДЭДТКН (диэтилдитиокарбомат натрия) 141, 336. Достоинством перечисленных собирателей является образование «сухого» сублата, сочетающееся с высоким извлечением меди и молибдена. Установлено, что извлечение меди, молибдена, железа и цинка из раствора происходит в определённом интервале рН. При рН~5,0-5,5 флотируется медь, железо и молибден - при рН~3,0-3,5. Выделенный в процессе флотации медный продукт после сушки можно перерабатывать в конверторе, молибденовый - использовать как добавку для получения высококачественных сталей.
В работе [290] для флотации катионов рекомендуется применение собирателей анионного типа: например, R-COO-(карбоксилат), R-SO3- (сульфонат), R-OSO3- (сульфат), R-C6H5-SO3--(бензосульфат), R-OPO32- (фосфат), R-CHSO3COO- (сульфокарбоксилат), где R – углеводородный радикал CnH2n+1 (n=10-16).
В работе Н.Н. Воронина [87] подробно изучены закономерности ионной флотации меди и цинка с помощью раствора нафтеновой кислоты в керосине.
Специалисты института технической химии Уральского отделения РАН (г. Пермь) занимаются разработкой органических комплексообразующих реагентов для ионной флотации Cu2+, Ni2+, Co2+ и Fe3+. Так, А.В. Радушев и Л.Г. Чеканова с сотрудниками [271] в процессе исследования установили принципиальную возможность применения 1,2-диацилгидразинов (ДАГ) в качестве флотационных собирателей ионов Cu2+, Ni2+, Co2+и Fe3+. В работах Г.И. Зубаревой, С.М. Адеева, А.В. Радушева [134, 135] исследованы закономерности извлечения ионов тяжелых металлов из модельных и реальных кислых сточных вод флотацией с применением в качестве собирателя гидразина октановой кислоты. А в работах [121, 342] рассмотрено использование 1,2-диацилгидразинов, 1,2-дибензоил- и 1-бензоил-2-ацетилгидразинов как возможных реагентов-собирателей.
Наиболее перспективными для ионной флотации считаются хелатообразующие реагенты [173]: они селективнее, обеспечивают глубокую очистку растворов в одну ступень, при правильной дозировке не требуют дополнительной очистки. Известен способ извлечения металлов из промышленных растворов в виде хелатов с водорастворимым гидразидом полиакриловой кислоты.
Для
извлечения из водных растворов ионов
 методом ионной флотации в качестве
собирателя используется анионное ПАВ
− сульфанол. При этом максимальные
показатели извлечения ионов
в
пену
наблюдаются
при рН > 2,0. Концентрирование
методом ионной флотации в качестве
собирателя используется анионное ПАВ
− сульфанол. При этом максимальные
показатели извлечения ионов
в
пену
наблюдаются
при рН > 2,0. Концентрирование
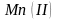 в пену происходит в виде соли состава
в пену происходит в виде соли состава
 ,
образующейся в результате ионообменной
реакции, протекающей по следующей схеме
[243] (где
,
образующейся в результате ионообменной
реакции, протекающей по следующей схеме
[243] (где
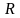 – анион
– анион
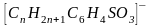 ):
):

Ограниченность
применения ионной флотации для извлечения
ионов
из техногенных растворов объясняется
тем, что используемые флотореагенты
токсичны и нормируются по показателю
вредности. Кроме того, данный метод
эффективен только для низкоконцентрированных
растворов
( - до 5 мг/дм3)
[90].
- до 5 мг/дм3)
[90].
На основе вышесказанного можно сделать следующие выводы: 1) В настоящее время развитие метода ионной флотации для извлечения тяжелых металлов из техногенных вод горных предприятий тормозится тем, что ассортимент реагентов, эффективно реагирующих с этими металлами, ограничен солями высших жирных кислот, сульфгидрильными и азотсодержащими соединениями, которые, как правило, являются дорогостоящими веществами с низкими значениями ПДК. Методы регенерации этих реагентов практически не разработаны, что приводит к вторичному загрязнению перерабатываемых вод. 2) Процесс ионной флотации может быть применен для разделения металлов. Для этого удобно использовать то обстоятельство, что при постепенном ступенчатом изменении значений рН растворов происходит селективное осаждение отдельных металлов. Флотируя образующиеся осадки, можно добиться разделения гидроксидов металлов. Однако, в большинстве случаев эффективность процесса разделения мала из-за адсорбции на осадках гидроксидов значительных количеств не осажденных ионов металлов [89, 103, 105]. 3) Ионная флотация является технологичным процессом переработки гидроминеральных месторождений. Так, при промышленных испытаниях флотационных установок механического типа (импеллерных и со струйным диспергированием воздуха) с использованием в качестве флотореагента 5 - 10 мг/дм3 четвертичных солей аммония было установлено, что эффективность очистки от катионов тяжелых металлов за 5-6 минут достигает 92-97 % при исходной концентрации металла 100 мг/дм3. 4) Флотация хорошо сочетается с другими способами извлечения тяжелых металлов.
Тем не менее, отмечается, что в результате флотационной очистки происходит вторичное загрязнение окружающей среды трудноразлагаемыми ПАВ, для удаления которых необходима доочистка, увеличивающая капитальные затраты [114].
Большинство авторов, изучавших закономерности флотационного разделения компонентов растворов, пришли к выводу о целесообразности выделения истинно-растворенных веществ в виде сублата или коллигенда коллоидной или более грубой степени дисперсности. Обоснование этого вывода дано в работах F. Sebba [293], А. Rubin [29-31], В. Кarger [12], Е. Маhne, N. Pinfold [19]. Флотация коллигенда коллоидной и суспензионной степени дисперсности включает в себя все процессы, при которых ионы или молекулы извлекаемого вещества переводятся в малорастворимые соединения с помощью органических или неорганических осадителей.
При рассмотрении процессов осадительной флотации выделяют следующие основные стадии: образование в растворе фазы новых химических соединений вследствие протекания реакций ионного обмена, гидролиза, комплексообразования и др.; формирование отдельных частиц и структур дисперсной фазы в растворе; гетерокоагуляционное взаимодействие частиц дисперсной фазы с поверхностью всплывающих пузырьков воздуха; ламинарная коагуляция частиц в поверхностных слоях пены или органической жидкости [12, 103].
Обоснование этих процессов возможно только на базе количественной теории. Между тем, несмотря на довольно значительное количество публикаций, в которых рассматриваются физико- и коллоидно-химические аспекты ионной флотации и родственных процессов, в подавляющем большинстве полученные из них экспериментальные зависимости трактуются качественно или предположительно.
Основными технологическими параметрами, определяющими эффективность извлечения тяжелых металлов из технологических растворов методом ионной флотации, являются расход собирателя, рН растворов, концентрация коллигенда и время процесса. Селективное выделение отдельных металлов данным методом возможно путем ступенчатого повышения рН.
Недостатками флотационного метода извлечения ионов и других агрегатных форм тяжелых металлов являются: достаточно ограниченный ассортимент реагентов-собирателей, отсутствие методики выбора реагентов для ИФ, сложности при регенерации реагентов-собирателей и, как следствие, вторичное загрязнение перерабатываемых вод ПАВ.
Необходима разработка универсального инновационного способа подбора перспективных реагентов–собирателей нового поколения с заранее заданными свойствами, селективно действующих, адаптированных к условиям ведения процесса и физико-химическому состоянию перерабатываемых техногенных вод.
