

МИНОБРНАУКИ РОССИИ
Федеральное государственное бюджетное образовательное учреждение высшего образования
«МИРЭА – Российский технологический университет»
РТУ МИРЭА
|
|
Институт тонких химических технологий им. М.В. Ломоносова |
|
(наименование Института)
|
|
Кафедра Биотехнологии и промышленной фармации |
|
(наименование кафедры)
Реферат на тему:
Производные пиридина. Производные пиридинметанола, оксипиридина и дигидропиридина
Работу выполнила
Студентка группы ХББО-02-16
Иванова Елена Анатольевна
Москва, 2020
Оглавление
ВВЕДЕНИЕ 3
Производные пиридинметанола и оксипиридина 4
Производные дигидропиридина 16
Рассмотрение схемы синтеза пиридоксина с типами реакций стадий 20
ЛИТЕРАТУРА 21
Введение
К производным пиридина относятся лекарственные средства как природного, так и синтетического происхождения, обладающие различными фармакологическим эффектом. По химическому строению все производные пиридина разделяют на 4 подгруппы:
-
Производные придин-4-карбоноыой (изоникотиновой) кислоты;
-
Производные приридин-3-карбоновой (никотиновой) кислоты;
-
Производные пиридинметанола и оксипиридина;
-
Производные дигидропиридина [1].
В данном реферате будут рассмотрены представители двух последних подгрупп, а именно производные пиридинметанола и оксипиридина (пиридоксина гидрохлорид, пиридоксальфосфат, пиридитол, пармидин, эмоксипин) и дигидропиридина (нифедипин, форидон, амплодипин).
В конце работы представлено рассмотрение синтеза пармидина с типами реакций каждой стадии.
Производные пиридинметанола и оксипиридина
Пиридоксина гидрохлорид (2-метил-3-гидрокси-4,5-дигидроксиметилпиридина гидрохлорид) – белый, мелкокристаллический порошок, легко растворимый в воде, трудно растворимый в спирте [1]. Химическая структура представлена на рис. 1.
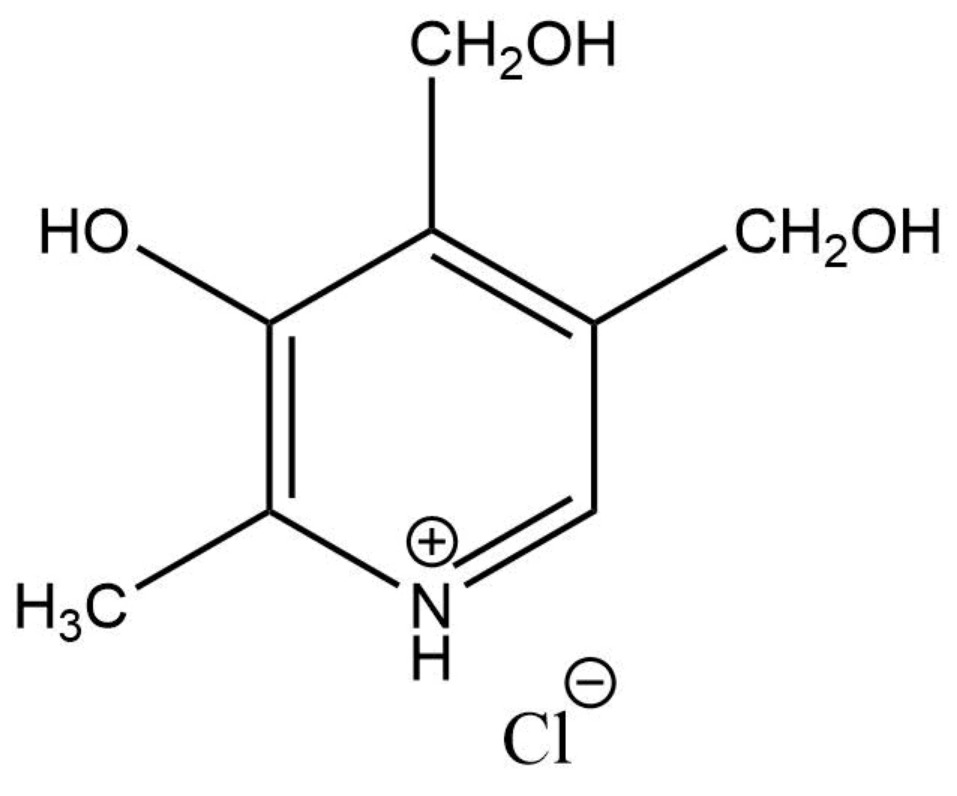
Рис. 1. Химическая структура пиридоксина гидрохлорида
Синтез пиридоксина
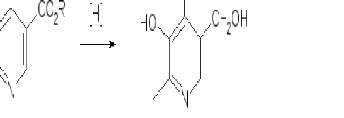
Рис. 2. Схема синтеза пиридоксина
Качественное и количественное определения [1,2].
Реакция на подлинность.
Идентифицировать пиридоксин можно по образованию индофенольного красителя с 2,6-дихлорхинонхлоримином. Образующийся окрашенный в голубой цвет продукт извлекают бутиловым спиртом:
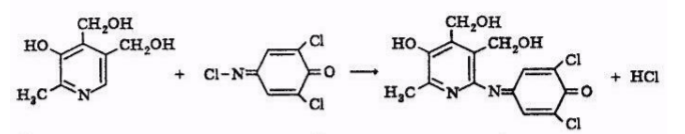
Рис. 3. Качественная реакция пиридоксина с 2,6-дихлоххинонхлоримином
В присутствии борной кислоты образование индофенольного красителя не происходит, так как пиридоксин связывается в боратный комплекс. Отсутствие положительной реакции в этих условиях служит подтверждением подлинности пиридоксина гидрохлорида.
Реакция с диазосоединениями.
Наличие фенольного гидроксила в молекуле пиридоксина и в пара-положении по отношению к нему незамещенного атома водорода создает возможности для получения азокрасителей с различными диазосоединениями. А.М. Алиевым предложен способ идентификации и фотоколориметрического определения пиридоксина с помощью этой реакции. Для повышения стойкости образующихся окрашенных азосоединений им разработан способ, основанный на получении металлокомплекса пиридоксина с азокрасителем. В качестве реактива использована стабилизированная хлоридом цинка соль диазония. Образование металлокомплекса пиридоксина с азокрасителем происходит по схеме:

Рис. 4. Образование металлокомплекса пиридокксина с азокрасителем
Эта реакция специфична для витаминов группы В6 и позволяет их дифференцировать по различной окраске. Пиридоксина гидрохлорид образует стойкое красно-фиолетовое окрашивание, пиридоксамина дигидрохлорид — красное, пиридоксаль — желто-оранжевое.
Другие специфичные реакции.
Фенольный гидроксил обнаруживают с помощью иона железа (III) (красное окрашивание, исчезающее от добавления разведенной серной кислоты).
Из других реактивов используют для идентификации гидрохлорида пиридоксина гетерополикислоты — кремневольфрамовую и фосфорновольфрамовую. Они образуют белые осадки кремневольфрамата или фосфорновольфрамата пиридоксина.
При действии на кристаллы пиридоксина гидрохлорида 1%-ным раствором ванадата аммония в концентрированной серной кислоте образуется сине-фиолетовое окрашивание, обусловленное восстановлением ванадия (V) до ванадия (IV) (синего цвета) или ванадия (II) (фиолетового цвета).
Характеристические полосы в УФ-спектре (зависит от pH среды): водная кислота – 290 нм, фосфатный буфер – 254, 324 нм.
Характеристические полосы в ИК-спектре: 1540, 1277, 1212, 1086, 1015, 870 см-1.
Характеристические пики в масс-спектре (m/z): 151, 150, 149, 122, 106, 94, 53, 51.
Количественно пиридоксина гидрохлорид определяют двумя способами. Первый основан на использовании метода неводного титрования:
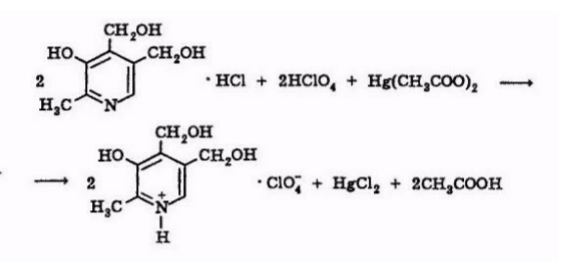
Рис. 5. Неводное титрование пиридоксина
Второй способ заключается в нейтрализации связанной соляной кислоты в препарате 0,1 М раствором гидроксида натрия (индикатор бромтимоловый синий):

Рис. 6. Алкалиметрическое титрование пиридоксина
Фармакологическое действие. Пиридоксин играет важную роль в обмене веществ. Он необходим для нормального функционирования центральной и периферической нервной системы. Поступая в организм, он фосфорилируется, превращаясь в пиридоксаль-5-фосфат и входит в состав ферментов, осуществляющих декарбоксилирование и переаминирование аминокислот. Пиридоксин участвует в процессах жирового обмена, улучшает липидный обмен при атеросклерозе [2].
Показания к применению. Пиридоксин применяют при различных заболеваниях: гиповитаминозе В6, токсикозах беременных, анемиях, заболеваниях нервной системы (паркинсонизм, невриты, радикулиты и др.), при острых и хронических гепатитах. В дерматологической практике применяют при дерматитах и нейродерматитах, опоясывающем лишае, псориазе и др. [2,3]
Форма выпуска: таблетки, растворы для инъекции [1,3].
Пиридоксальфосфат (5-(2-метил-3-гидрокси-4-формилпиридил)-метилфосфорная кислота) – светло-желтый кристаллический порошок, неустойчивый на свету. Мало растворим в воде, практически нерастворим в спирте [1]. Структурная формула изображена на рис. 7.

Рис. 7. Химическая структура пиридоксальфосфата
Качественное и количественное определения [1,2].
Из-за схожего строения, многие реакции, характерные для пиридоксина гидрохлорида, характерны и для пиридоксальфосфата. Так, фенольный гидроксил также обнаруживают с помощью иона железа (III) (красное окрашивание, исчезающее от добавления разведенной серной кислоты).
Отличительной реакцией на альдегидную группу в молекуле пиридоксальфосфата служит взаимодействие с фенилгидразина гидрохлоридом, добавление которого в виде солянокислого раствора вызывает образование желтого хлопьевидного остатка фенилгидразона:

Рис. 8. Реакция пиридоксальфосфата с фенилгидразин гидрохлоридом
При этом осадок растворяется при добавлении 0,1 М раствора гидроксида натрия.
Установить подлинность пиридоксальфосфата также можно по УФ-спектрам. Растворы препарата в фосфатном буферном растворе (рН 7) имеют максимумы поглощения при 330 и 388 нм.
Содержание пиридоксальфосфата определяют также, как и пиридоксина гидрохлорид методом неводного титрования, но без добавления ацетата ртути (II) (см. рис. 5). При этом используют растворитель – смесь уксусного ангидрида и муравьиной кислоты, а в качестве индикатора раствор Судана III.
Фармакологическое действие. Пиридоксальфосфат является коферментной формой витамина В6, обладает его свойствами. Отличается тем, что оказывает быстрый терапевтический эффект и может применяться в случаях, когда нарушено фосфорилирование пиридоксина и он не дает терапевтического эффекта [2].
Показания к применению пиридоксальфосфата такие же, как для пиридоксина гидрохлорида (см. выше) [3,4].
Форма выпуска – лиофилизированный порошок в ампулах [1] или таблетки, покрытые оболочкой [3].
Пиридитол (пиритинол) (бис-(2-метил-3-гидрокси-4-гидроксиметил-5-метилпиридил)-дисульфида дигидрохлорид, гидрат) – белый или белый со слегка желтоватым оттенком кристаллический порошок, легко растворимый в спирте, мало растворимый в спирте [1]. Структурная формула представлена на рис. 9.

Рис.9. Химическая структура пиридитола
Синтез пиридитола.
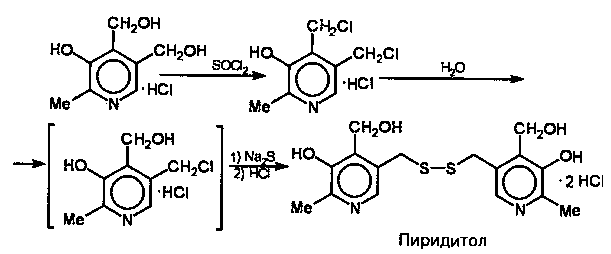
Рис. 10. Схема синтеза пиридитола
Качественный и количественный анализ [1].
Характерной в пиридитоле является дисульфидная группа, которую качественно идентифицируют после нагревания препарата с цинковой пыль на водяной бане. Получившийся в результате реакции сульфид цинка взаимодействует с фосфорно-молибденовой кислотой в присутствии концентрированного раствора аммиака с образованием продукта синего цвета.
Количественное определение пирилитола сводится к кислотно-основному титрованию в неводной среде, при этом в качестве растворителя используют ледяную уксусную кислоту, а в качестве титранта – 0,1 М раствор хлорной кислоты.
Фармакологическое действие. Пиридитол относится к ноотропным препаратам и обладает способностью вызывать эффекты, подобные ацетилхолину (холиномиметик). Он усиливает обменные процессы в мозговой ткани, повышает усвоение и метаболизм глюкозы, обмен нуклеиновых кислот, активность ряда ферментов и медиаторных систем мозга, устойчивость мозга к гипоксии [3].
Показания к применению. Пиридитол применяют при расстройствах памяти, мышления, при задержке психического развития, церебрастеническом синдром и др. [3]
Форма выпуска – таблетки.
Пармидин (пиридинолкарбамат, продектин) (бис-N-метилкарбаминовый эфир 2,6-бис-оксиметилпиридина) – белый кристаллический порошок, мало растворимый в воде и трудно – в спирте [1]. Химическая формула представлена на рис. 11.

Рис. 11. Химическая структура пармидина
Синтез пармидина.

Рис. 12. Схема синтеза пармидина
Качественный и количественный анализ [1,2].
При испытании подлинности устанавливают в молекуле препарата наличие третичного атома азота с помощью цветной реакции, которую проводят при нагревании смеси препарата с лимонной кислотой и уксусным ангидридом. Появляется желтое окрашивание, постепенно переходящее в красное (с различными оттенками). Наличие N-метилуретановой группировки устанавливают, гидролизуя пармидин при кипячении в присутствии гидроксида натрия. Выделяющийся метиламин обнаруживают по запаху или по изменению в синий цвет окраски красной лакмусовой бумаги:
R-CO-NH-CH3 + NaOH → R-COONa + NH2CH3 ↑
Указанные химические реакции не являются специфичными для пармидина. Более объективно его подлинность подтверждают методами ИК- и УФ-спектроскопии. ИК-спектр, снятый в вазелиновом масле в области от 3700 до 400 см-1, должен полностью совпадать с прилагаемым к ФС спектром, а УФ-спектр 0,002%-ного раствора пармидина в соляной кислоте должен иметь максимум поглощения при 268 нм.
Количественно пармидин определяют методом неводного титрования в среде ледяной уксусной кислоты с использованием в качестве титранта 0,1 М раствора хлорной кислоты (индикатор кристаллический фиолетовый).
Фармакологическое действие. Пармидин относится к классу ангиопротекторов. Он уменьшает проницаемость сосудов, способствует восстановлению нарушенной микроциркуляции, снижает агрегацию тромбоцитов, стимулирует фибриногенез. Имеются данные о положительном действии препарата на состояние желудка и поджелудочной железы при сахарном диабете, а также о целесообразности применения пармидина в комплексном лечении больных туберкулезом легких [2,4].
Показания к применению. Используется как средство комплексной терапии при лечении атеросклероза сосудов мозга, сердца, конечностей, тромбозевен сетчатки, облитерирующем эндартериите, трофических язвах конечностей. Эффективен пармидин при лечении распространенных нейродермитов [2-4].
Форма выпуска – таблетки.
Эмоксипин (3-гидрокси-6-метил-2-этилпиридина гидрохлорид) – белый с кремовым оттенком кристаллический порошок, легко растворимый в воде [1]. Структурная формула представлена на рис. 13.

Рис. 13. Химическая структура эмоксипина
Качественное и количественное опредление.
Подлинность эмоксипина устанавливают с помощью УФ-спектроскопии: 0.001% раствор препарата в буферном растворе с рН 8.0 имеет максимумы поглощения при 250 и 325 нм и минимумы при 230 и 270 нм.
Присутствие у эмоксипина связанного хлороводорода подтверждают с помощью реакции на хлориды.
Количественно эмоксипин определяют методом неводного титрования в среде безводной муравьиной кислоты и уксусного ангидрида с использованием в качестве титранта 0,1 М раствора хлорной кислоты (индикатор кристаллический фиолетовый).
Фармакологическое действие. Эмоксипин является антиоксидантом, обладающим антигипоксической, ангиопротекторной, антиагрегационной активностью. Применяется в офтальмологии для лечения внутриглазных кровоизлияний, тромбоза центральной вены, световых ожогов глаз. В кардиологии – при остром инфаркте миокарда и при нестабильной стенокардии. В неврологии – при ишемических и геморрагических нарушениях мозгового кровообращени [2].
Показан к применению при внутриглазном и посттравматическом, кровоизлиянии, тромбозе центральной вены сетчатой оболочки глаза и ее ветвей, осложненная миопатия, глаукома, острые и хронические нарушения мозгового кровообращения ишемического и геморрагического характера. Так же назначается для защита сетчатой оболочки глаза от воздействия света высокой интенсивности (лазерные и солнечные ожоги, лазеркоагуляция) [3].
Форма выпуска – раствор для инъекций.
