
- •Домашнє завдання вивчення діаграми стану системи залізо-цементит та класифікації і призначення сталей та чавунів Мета та завдання .
- •Стислі теоретичні відомості
- •Діаграма стану залізо- вуглець
- •Точки діаграми.
- •Кристалізація сплавів
- •Порядок виконання завдання
- •Методичні вказівки до виконання завдання
- •Варіанти завдань
- •Література
Домашнє завдання вивчення діаграми стану системи залізо-цементит та класифікації і призначення сталей та чавунів Мета та завдання .
При виконанні домашнього завдання студенти повинні засвоїти теоретичні знання з розділу програми, який стосується залізовуглецевих сплавів. Це має бути чітке знання ліній та точок діаграми залізо-цементит, суті первинної та вторинної кристалізації сталей та чавунів, структур, які утворюються при цьому. Студенти повинні також набути практичних навичок побудови кривих охолодження різних залізовуглецевих сплавів та перевірки їх по правилу фаз. Крім того, треба чітко знати класифікацію сталей та чавунів по всім ознакам та їх маркірування.
В результаті виконання даного домашнього завдання студенти повинні добре знати суть, структури та марки різних сталей та чавунів, вміти розшифровувати їх та чітко визначити призначення для виготовлення деталей машин.
Стислі теоретичні відомості
В промисловості найбільш широко використовуються сплави заліза з вуглецем. Близько 93% конструкційних матеріалів, які застосовуються для виготовлення деталей машин, складають сталі та чавуни. Для одержання різних експлуатаційних властивостей в сталі та чавуни вводять легувальні елементи.
Компоненти та фази в системі залізо-вуглець.
Компоненти – залізо та вуглець.
Чисте
залізо.
Це метал сріблясто- білого кольору.
Чисте залізо, яке може бути одержано в
теперішній час, містить 99,999% Fe. Технічні
сорта заліза містять 99,8…99,9% Fe. Температура
плавлення заліза – 1539º. Залізо має дві
поліморфні модифікації -
![]() і
і
![]() .
Модифікація
існує при температурі нижче 768˚.
Кристалічна гратка
-заліза
– ОЦК. До 768º
-залізо
магнетно. Критичну точку 768º, відповідну
магнетному перетворенню, т. е. переходу
від ферромагнетного до парамагнетного
стану, називають точкою Кюрі та позначають
А2.
В інтервалі температур від 768˚ до 911˚
існує β-залізо. Ця модифікація також
має кристалічну гратку ОЦК, але з другим
параметром. При високих температурах
від 1392˚ до 1539˚ існує модифікація δ-заліза
з кристалічною граткою ОЦК та іншим
параметром.
.
Модифікація
існує при температурі нижче 768˚.
Кристалічна гратка
-заліза
– ОЦК. До 768º
-залізо
магнетно. Критичну точку 768º, відповідну
магнетному перетворенню, т. е. переходу
від ферромагнетного до парамагнетного
стану, називають точкою Кюрі та позначають
А2.
В інтервалі температур від 768˚ до 911˚
існує β-залізо. Ця модифікація також
має кристалічну гратку ОЦК, але з другим
параметром. При високих температурах
від 1392˚ до 1539˚ існує модифікація δ-заліза
з кристалічною граткою ОЦК та іншим
параметром.
При
температурі 911…1392ºС існує
-залізо.
Його гратка – ГЦК, воно парамагнетно.
Критичну точку
![]() перетворення при 911º позначають Ас3
при нагріві та Аr3
при охолодженні. Критичну точку переходу
γ→δ при 1392º позначають Ас4
при нагріві та Аr4
при охолодженні.
перетворення при 911º позначають Ас3
при нагріві та Аr3
при охолодженні. Критичну точку переходу
γ→δ при 1392º позначають Ас4
при нагріві та Аr4
при охолодженні.
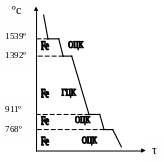
δ
γ
β
α
Крива охолодження чистого заліза.
Щільність -железа 7,68 г/см3.
Щільність -железа вище та складає 8,0…8,1 г/см3.
Вуглець. Являється неметалічним елементом II періоду IV групи. Температура плавлення 3500ºС. Вуглець поліморфний. В звичайних умовах він знаходиться у вигляді модифікації графіту, но може існувати і у вигляді метастабільної модифікації алмаза.
Вуглець розчиняється в залізі в рідкому та твердому стані, а також може бути у вигляді хімічної сполуки – цементита, а у високовуглецевих сплавах і в вигляді графіту.
Фази. В системі Fe-C розрізняють наступні фази: рідка фаза, тверді розчини – ферит та аустеніт, а також цементит та графіт.
Ферит (Ф) – твердий розчин вуглецю в -залізі.
Атом вуглецю розміщується в гратці ферита в центрі грані куба, а також в вакансіях та на дислокаціях.
Розрізняють
низькотемпературний
-ферит
з розчинністю вуглецю до 0,025% та
високотемпературний
![]() -ферит
з гранічною розчинністю вуглецю 0,1% при
температурі 1499ºС.
-ферит
з гранічною розчинністю вуглецю 0,1% при
температурі 1499ºС.
При
кімнатній температурі ферит розчиняє
0,006% С та має низькі механічні властивості:
НВ 80…90,
=50%,
![]() =25
кгс/мм2.
Під мікроскопом ферит виглядає у вигляді
однорідних світлих зерен.
=25
кгс/мм2.
Під мікроскопом ферит виглядає у вигляді
однорідних світлих зерен.
Аустеніт (А) – твердий розчин вуглецю в -залізі.
Атом вуглецю в гратці -заліза розміщується в центрі елементарної комірки та в дефектних областях металу.
Гранічна розчинність вуглецю в -залізі 2,14% при температурі 1147º і 0,8% при температурі 727ºС.
Аустеніт м’який, пластичний, НВ 160…200, =40…50%.
Під мікроскопом виглядає у вигляді світлих зерен.
Цементит. Це хімічна сполука заліза з вуглецем – карбід заліза Fe3С. В ньому міститься 6,67% С. Цементит має сложну ромбічну гратку з щільним пакуванням атомів. Температура плавлення приблизно 1600ºС. До температури 210ºС (т. А0) цементит ферромагнетний. До характерних особливостей цементита відноситься його висока твердість НВ 800…850 та дуже мала пластичність =0%. Цементит являється метастабільною фазою. В умовах рівноваги в сплавах з високим складом вуглецю утворюється графіт.
_Графіт. Кристалічна гратка графіта гексагональна шарувата. Графіт м’який та має низьку міцність.
